Clear Sky Science · es
La deficiencia de 2’-5’ oligoadenilato sintetasa‑like 1 (OASL1) en ratones favorece la protección antiviral frente a la infección por el virus de la pseudorrabia asociada a una mayor producción de interferón tipo I
Por qué importa para personas y animales
El virus de la pseudorrabia puede parecer una curiosidad de la vida agrícola, pero es un gran causante de mortalidad en lechones, una amenaza para la industria mundial del cerdo y un origen ocasional de infecciones cerebrales graves en humanos. Este estudio revela cómo una de las propias proteínas “freno” del organismo, llamada OASL1, puede en realidad empeorar la peligrosidad de este virus al modular a la baja las defensas antivirales tempranas. Al eliminar este freno en ratones, los autores muestran que es posible mejorar de forma notable la supervivencia, reducir el daño cerebral y disminuir los niveles virales, ofreciendo pistas para mejores tratamientos y vacunas contra el virus de la pseudorrabia y herpesvirus relacionados.
Un virus duro y de amplio alcance
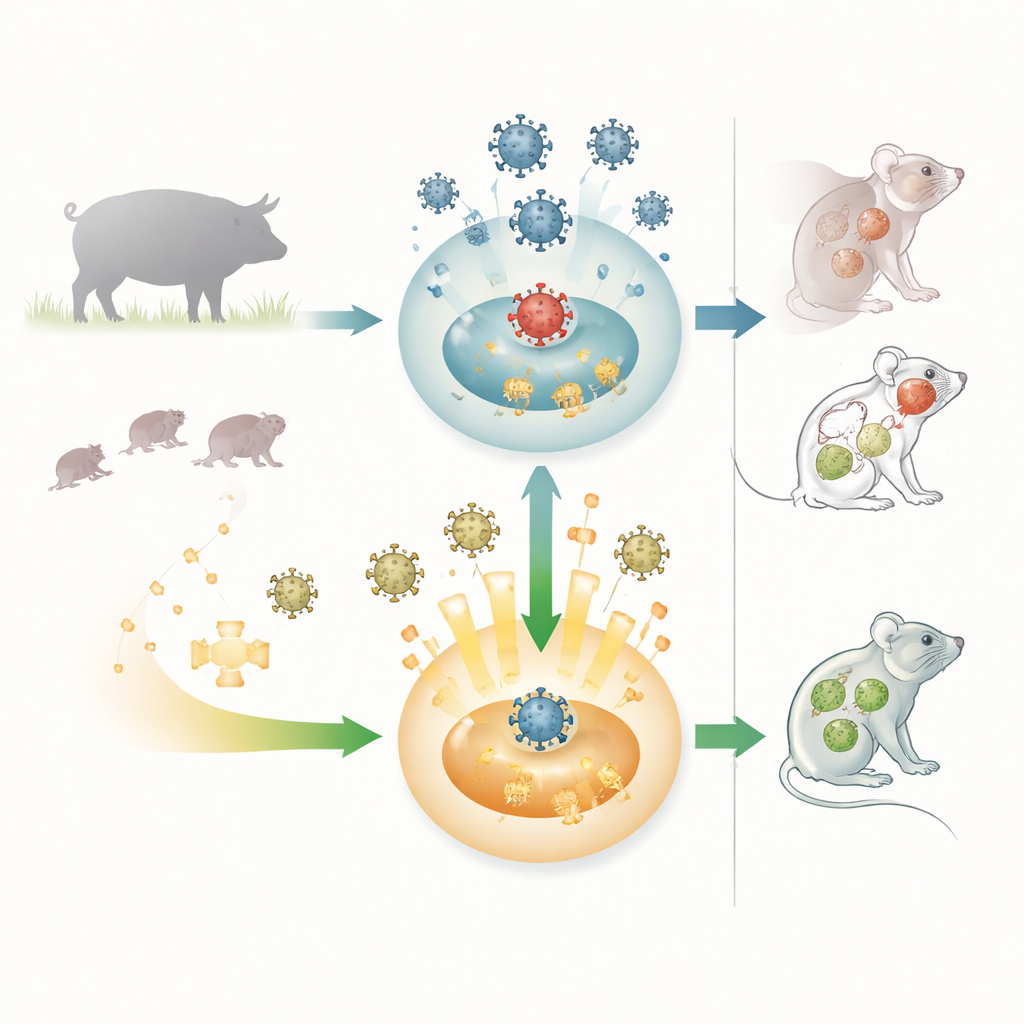
El virus de la pseudorrabia es un herpesvirus cuyo hospedador natural son los cerdos, donde puede causar problemas respiratorios, fallos reproductivos y la muerte casi segura de los lechones recién nacidos. El virus también puede infectar a muchos otros mamíferos, incluidos animales de granja, mascotas y ratones de laboratorio, y casi todos estos hospedadores accidentales mueren. Informes recientes de infecciones cerebrales humanas vinculadas a variantes del virus de la pseudorrabia han despertado la preocupación de que este patógeno animal pueda ocasionalmente saltar a las personas. Debido a este amplio rango de hospedadores y a la gravedad de la enfermedad, los investigadores están interesados en entender cómo la primera línea de defensa del organismo, el sistema inmunitario innato, combate este virus —y cómo el virus contraataca.
El sistema de alarma del cuerpo y un freno incorporado
Cuando un virus de ADN como el de la pseudorrabia entra en las células, sensores especializados detectan el material genético viral y desencadenan la producción de interferones tipo I, una familia de potentes moléculas de alarma antiviral. Estos interferones activan cientos de genes defensivos. Entre ellos se encuentra OASL1, una proteína que no destruye directamente a los virus sino que ajusta la respuesta. Trabajos anteriores mostraron que OASL1 puede frenar la producción de IRF7, un regulador clave de la producción de interferón, formando un bucle de retroalimentación negativa que impide que el sistema de alarma permanezca encendido demasiado tiempo. La cuestión central de este estudio fue qué ocurre durante la infección por el virus de la pseudorrabia si se elimina este freno, OASL1.
Quitar el freno protege a los ratones
Los investigadores compararon ratones normales con ratones modificados genéticamente para carecer de OASL1. Ambos grupos recibieron una dosis de virus de la pseudorrabia que suele ser letal. Todos los ratones normales desarrollaron picor intenso, lesiones cutáneas, convulsiones y parálisis, y murieron. En marcado contraste, la mayoría de los ratones deficientes en OASL1 sobrevivieron y mantuvieron el peso corporal con síntomas mucho más leves. Cuando el equipo midió los niveles virales en el bazo, los pulmones y el cerebro, encontraron que los ratones sin OASL1 presentaban cargas virales mucho más bajas. Análisis sanguíneos mostraron que estos ratones produjeron cantidades mayores de interferones tipo I en las fases tempranas de la infección, lo que sugiere que una respuesta de alarma más rápida y robusta ayudó a controlar el virus antes de que se difundiera ampliamente.
Menos inflamación descontrolada, menos daño orgánico
Las infecciones virales graves pueden desencadenar una “tormenta de citoquinas”, una reacción inflamatoria abrumadora que daña los órganos. Los científicos midieron varias moléculas inflamatorias clave en tejidos y sangre. Los ratones normales infectados con el virus de la pseudorrabia mostraron altos niveles de estos factores en bazo, pulmones y cerebro, junto con una intensa infiltración de células inflamatorias. En contraste, los ratones deficientes en OASL1 presentaron niveles mucho más bajos de estas señales inflamatorias. Al microscopio, sus bazos conservaron las células inmunitarias en lugar de perderlas por muerte celular, sus pulmones mostraron cambios inflamatorios más leves y sus cerebros presentaron mucha menos degeneración neuronal en el hipocampo, una región crítica para la memoria. Así, eliminar OASL1 no solo ayudó a eliminar el virus, sino que también previno una inflamación y lesión tisular excesivas.
Acercándose al interruptor de control clave
Para entender cómo OASL1 configura esta respuesta, el equipo examinó IRF7, el interruptor que impulsa la producción de interferón. En ratones sin OASL1, los niveles de IRF7 fueron consistentemente mayores en bazo, pulmones, cerebro y en células inmunitarias cultivadas como macrófagos y microglía tras la infección, mientras que un factor relacionado, IRF3, cambió poco. Estas células secretaron más interferones tipo I y sostuvieron menos replicación viral. Cuando los investigadores utilizaron ARN de interferencia para reducir específicamente IRF7 en macrófagos deficientes en OASL1, la respuesta aumentada de interferón desapareció y los niveles virales repuntaron. Este experimento mostró que el efecto protector de perder OASL1 depende principalmente de liberar a IRF7 para activar plenamente el programa antiviral.
Qué implica esto de cara al futuro
En términos sencillos, OASL1 actúa como un freno de seguridad interno que impide que la alarma antiviral suene durante demasiado tiempo. Durante la infección por el virus de la pseudorrabia, ese freno se activa demasiado pronto y con demasiada intensidad, dando espacio al virus para multiplicarse y contribuyendo a la enfermedad grave. Los ratones que carecen de OASL1, o en los que OASL1 se silencia temporalmente en células inmunitarias clave, montan una respuesta interferón impulsada por IRF7 más rápida y enérgica que elimina el virus con mayor eficacia mientras evita una tormenta de citoquinas dañina. Estos hallazgos sugieren que fármacos administrados con el tiempo adecuado que aflojen cuidadosamente este freno —solo durante la ventana temprana crítica de la infección— podrían ayudar a proteger a los cerdos y posiblemente a humanos frente a la pseudorrabia y herpesvirus relacionados. Sin embargo, cualquier terapia así tendría que ajustarse con precisión para evitar pasar de una respuesta inmune insuficiente a otra excesiva.
Cita: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Palabras clave: virus de la pseudorrabia, inmunidad innata, interferón tipo I, OASL1, IRF7