Clear Sky Science · de
2’-5’ Oligoadenylat-Synthetase-ähnliches 1- (OASL1-) defiziente Mäuse fördern antiviralen Schutz gegen Pseudowutvirus-Infektion in Verbindung mit erhöhter Produktion von Typ‑I‑Interferon
Warum das für Menschen und Tiere relevant ist
Pseudowutvirus klingt vielleicht nach einer Kuriosität vom Bauernhof, ist aber ein bedeutender Killer von Ferkeln, eine Bedrohung für die globale Schweinewirtschaft und gelegentlich Ursache schwerer Hirninfektionen beim Menschen. Diese Studie zeigt, wie eines der körpereigenen „Brems“-Proteine, genannt OASL1, das Virus tatsächlich gefährlicher machen kann, indem es frühe antivirale Abwehrmechanismen dämpft. Durch das Entfernen dieser Bremse bei Mäusen zeigen die Autorinnen und Autoren, dass Überleben deutlich verbessert, Hirnschäden reduziert und Virustiter gesenkt werden können — Hinweise, die für bessere Behandlungen und Impfstoffe gegen Pseudowutvirus und verwandte Herpesviren nützlich sind.
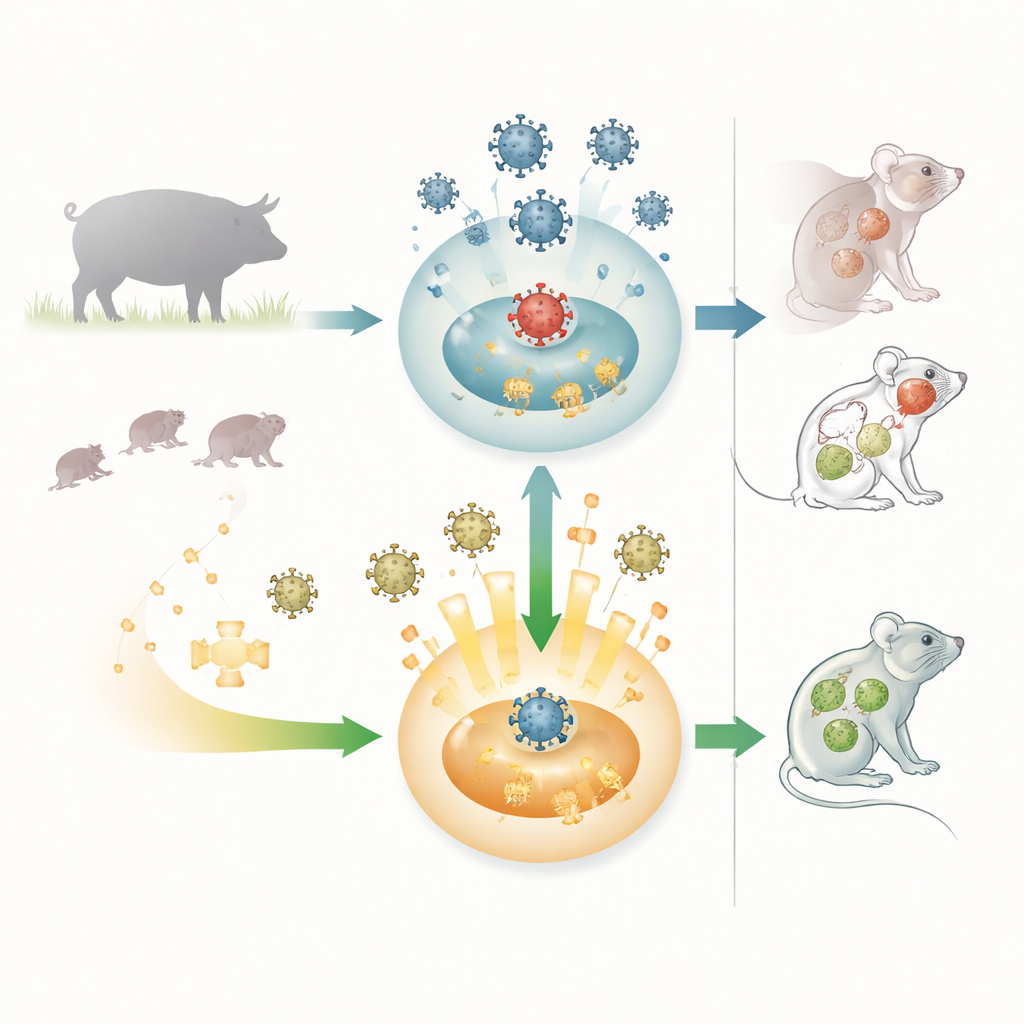
Ein hartnäckiges Virus mit breiter Wirtsreichweite
Das Pseudowutvirus ist ein Herpesvirus, dessen natürlicher Wirtsbereich Schweine sind, wo es Atemprobleme, Fortpflanzungsstörungen und nahezu sicheren Tod bei neugeborenen Ferkeln verursachen kann. Das Virus kann auch viele andere Säugetiere infizieren, darunter Nutztiere, Haustiere und Labormäuse — und fast alle diese Fehlwirte sterben. Jüngste Berichte über menschliche Hirninfektionen, die mit Varianten des Pseudowutvirus in Verbindung gebracht werden, haben die Besorgnis erhöht, dass dieser Erreger gelegentlich auf Menschen überspringen kann. Wegen dieser breiten Wirtsreichweite und der schweren Erkrankungen sind Forschende daran interessiert zu verstehen, wie die erste Verteidigungslinie des Körpers, das angeborene Immunsystem, dieses Virus bekämpft — und wie das Virus dagegenhält.
Das körpereigene Alarmsystem und eine eingebaute Bremse
Wenn ein DNA‑Virus wie das Pseudowutvirus in Zellen eindringt, erkennen spezialisierte Sensoren virales Erbgut und lösen die Produktion von Typ‑I‑Interferonen aus, einer Familie starker antiviraler Alarmmoleküle. Diese Interferone schalten Hunderte von Abwehrgenen ein. Eines davon ist OASL1, ein Protein, das Viren nicht direkt zerstört, sondern die Reaktion fein abstimmt. Frühere Arbeiten zeigten, dass OASL1 die Produktion von IRF7 zurückhalten kann, einem zentralen Schalter für die Interferonproduktion, und damit eine negative Rückkopplung bildet, die verhindert, dass das Alarmsystem zu lange aktiv bleibt. Die zentrale Frage dieser Studie war, was bei einer Pseudowutvirus‑Infektion passiert, wenn diese Bremse, OASL1, entfernt wird.
Die Bremse zu entfernen schützt Mäuse
Die Forschenden verglichen normale Mäuse mit genetisch veränderten Mäusen, die kein OASL1 besitzen. Beide Gruppen erhielten eine normalerweise tödliche Dosis Pseudowutvirus. Alle normalen Mäuse entwickelten starken Juckreiz, Hautwunden, Anfälle und Lähmungen, und alle starben. Im auffälligen Gegensatz dazu überlebten die meisten OASL1‑defizienten Mäuse und hielten ihr Körpergewicht bei mit deutlich milderen Symptomen. Bei Messungen der Viruslast in Milz, Lunge und Gehirn zeigte sich, dass Mäuse ohne OASL1 deutlich geringere Virustiter hatten. Bluttests ergaben, dass diese Mäuse früh in der Infektion höhere Mengen an Typ‑I‑Interferonen produzieren, was darauf hindeutet, dass eine stärkere, schnellere Alarmreaktion das Virus eindämmte, bevor es sich weit ausbreiten konnte.
Weniger entgleiste Entzündung, weniger Organschaden
Schwere Virusinfektionen können einen „Zytokinsturm“ auslösen, eine überwältigende Entzündungsreaktion, die Organe schädigt. Die Wissenschaftler maßen mehrere wichtige Entzündungsmoleküle in Geweben und Blut. Normale Mäuse, die mit Pseudowutvirus infiziert waren, zeigten hohe Spiegel dieser Faktoren in Milz, Lunge und Gehirn sowie starke Infiltration entzündlicher Zellen. Dagegen wiesen OASL1‑defiziente Mäuse deutlich niedrigere Entzündungssignale auf. Mikroskopisch blieben in ihren Milzen Immunzellen erhalten, statt durch Zelltod verloren zu gehen, ihre Lungen zeigten mildere entzündliche Veränderungen, und ihre Gehirne wiesen deutlich weniger Nervenzelldegeneration im Hippocampus auf — einem für Gedächtnis wichtigen Bereich. Somit half das Entfernen von OASL1 nicht nur bei der Viruselimination, sondern verhinderte auch überschießende Entzündung und Gewebeschäden.
Fokus auf den wichtigen Schaltregler
Um zu verstehen, wie OASL1 diese Reaktion formt, untersuchten die Forschenden IRF7, den Schalter, der die Interferonproduktion antreibt. Bei Mäusen ohne OASL1 waren die IRF7‑Spiegel konsequent höher in Milz, Lunge, Gehirn und in kultivierten Immunzellen wie Makrophagen und Mikroglia nach der Infektion, während ein verwandter Faktor, IRF3, sich kaum veränderte. Diese Zellen sezernierten mehr Typ‑I‑Interferone und unterstützten weniger virale Replikation. Als die Forschenden mittels kleiner interferierender RNA IRF7 spezifisch in OASL1‑defizienten Makrophagen herunterregulierten, verschwand die verstärkte Interferonantwort und die Viruslast stieg wieder an. Dieses Experiment zeigte, dass der schützende Effekt des Verlusts von OASL1 hauptsächlich davon abhängt, IRF7 zu befreien, damit es das antivirale Programm voll aktivieren kann.
Was das für die Zukunft bedeutet
Alltagssprachlich wirkt OASL1 wie eine interne Sicherheitsbremse, die verhindert, dass der antivirale Alarm zu lange heult. Bei Pseudowutvirus‑Infektion greift diese Bremse zu früh und zu stark, wodurch dem Virus Raum zur Vermehrung gegeben und schwere Erkrankungen gefördert werden. Mäuse ohne OASL1, oder bei denen OASL1 vorübergehend in wichtigen Immunzellen stummgeschaltet wurde, zeigen eine zügige, IRF7‑getriebene Interferonantwort, die das Virus effektiver beseitigt und gleichzeitig einen schädlichen Zytokinsturm vermeidet. Diese Ergebnisse legen nahe, dass sorgfältig getimte Wirkstoffe, die diese Bremse lockern — nur im kritischen frühen Infektionsfenster — Schweine und möglicherweise Menschen vor Pseudowutvirus und verwandten Herpesviren schützen könnten. Eine solche Therapie müsste jedoch sehr fein abgestimmt sein, um zu verhindern, dass das Immunsystem von zu schwach zu überschießend wechselt.
Zitation: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Schlüsselwörter: Pseudowutvirus, angeborene Immunität, Typ‑I‑Interferon, OASL1, IRF7