Clear Sky Science · nl
2’-5’ Oligoadenylaat Synthetase-Like 1- (OASL1-) deficiënte muizen bevorderen antivirale bescherming tegen pseudorabiesvirusinfectie geassocieerd met verhoogde productie van type I interferon
Waarom dit belangrijk is voor mensen en dieren
Pseudorabiesvirus klinkt misschien als een curiositeit uit het boerenleven, maar het is een belangrijke doodsoorzaak van biggen, een bedreiging voor de wereldwijde varkensindustrie en af en toe de oorzaak van ernstige herseninfecties bij mensen. Deze studie onthult hoe een van de eigen "rem"-eiwitten van het lichaam, OASL1 genoemd, het virus juist gevaarlijker kan maken door vroege antivirale afweer te onderdrukken. Door deze rem in muizen te verwijderen, laten de auteurs zien dat het mogelijk is de overlevingskansen aanzienlijk te verbeteren, hersenschade te verminderen en de virusniveaus te verlagen, wat aanwijzingen geeft voor betere behandelingen en vaccins tegen pseudorabiesvirus en verwante herpesvirussen.
Een hardnekkig virus met een brede reikwijdte
Pseudorabiesvirus is een herpesvirus waarvan varkens de natuurlijke gastheer zijn; daar kan het ademhalingsproblemen, voortplantingsfalen en vrijwel zeker de dood van pasgeboren biggen veroorzaken. Het virus kan ook veel andere zoogdieren infecteren, waaronder boerderijdieren, huisdieren en laboratoriummuizen, en bijna al deze toevallige gastheren sterven. Recente meldingen van menselijke herseninfecties gekoppeld aan varianten van pseudorabiesvirus hebben de bezorgdheid gewekt dat deze dierlijke ziekteverwekker af en toe op mensen kan overspringen. Vanwege dit brede gastbereik en de ernstige ziekte willen onderzoekers begrijpen hoe de eerstelijnsafweer van het lichaam, het aangeboren immuunsysteem, dit virus bestrijdt — en hoe het virus zich verzet.
Het alarmsysteem van het lichaam en een ingebouwde rem
Wanneer een DNA-virus zoals pseudorabies een cel binnendringt, detecteren gespecialiseerde sensoren viraal genetisch materiaal en zetten ze de productie van type I interferonen in gang, een familie van krachtige antivirale alarmmoleculen. Deze interferonen schakelen honderden verdedigingsgenen aan. Tot die groep behoort OASL1, een eiwit dat virussen niet rechtstreeks vernietigt maar de respons verfijnt. Eerder werk toonde dat OASL1 de productie van IRF7, een sleutelregelaar van interferonproductie, kan remmen en zo een negatieve terugkoppelingslus vormt die voorkomt dat het alarmsignaal te lang blijft aanstaan. De centrale vraag van deze studie was wat er gebeurt tijdens een pseudorabiesinfectie als deze rem, OASL1, wordt verwijderd.
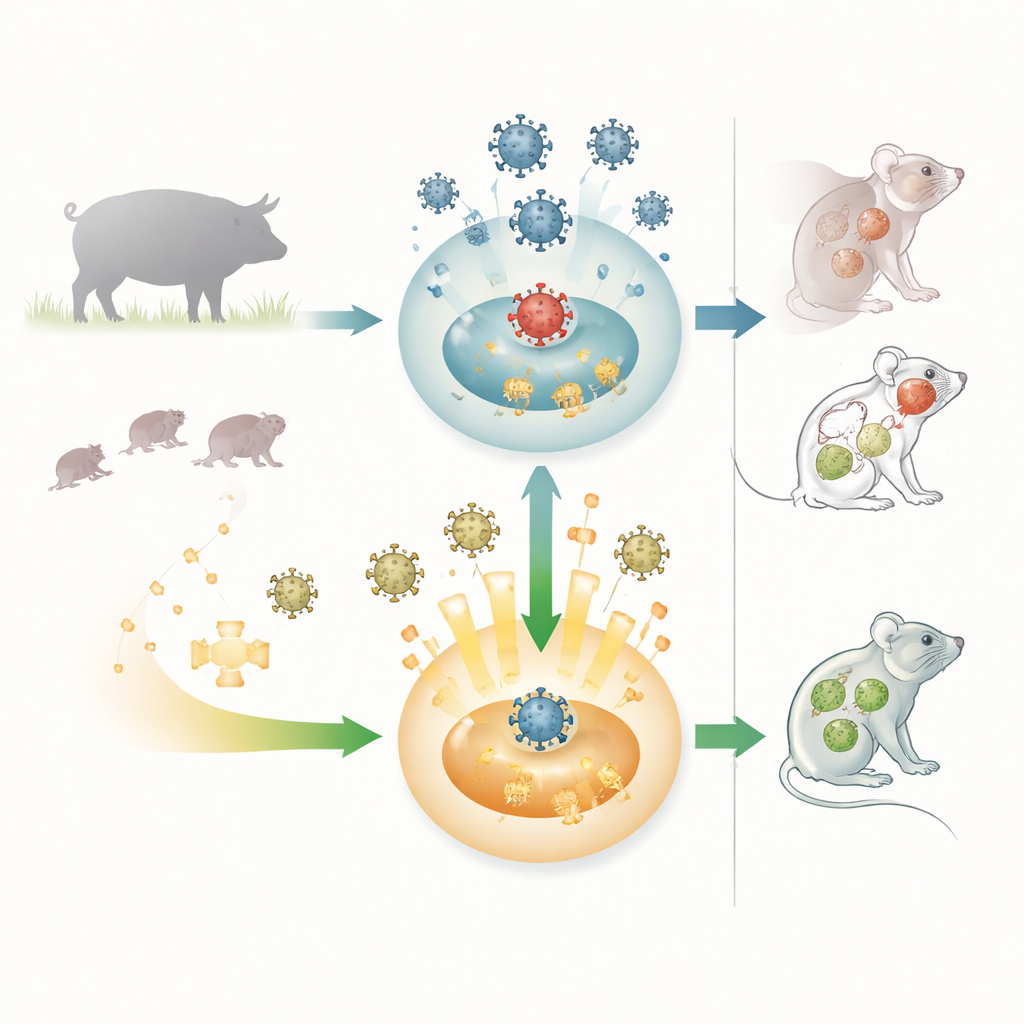
Het verwijderen van de rem beschermt muizen
De onderzoekers vergeleken normale muizen met muizen die genetisch zo gemodificeerd waren dat ze OASL1 misten. Beide groepen kregen een dosis pseudorabiesvirus die gewoonlijk dodelijk is. Alle normale muizen ontwikkelden hevige jeuk, huidwonden, aanvallen en verlamming, en geen van hen overleefde. In opvallend contrast overleefden de meeste OASL1-deficiënte muizen en behielden ze hun lichaamsgewicht met veel mildere symptomen. Toen het team de virusniveaus in de milt, longen en hersenen mat, vonden ze dat muizen zonder OASL1 veel lagere virusbelastingen hadden. Bloedtests toonden aan dat deze muizen vroeg in de infectie hogere hoeveelheden type I interferonen produceerden, wat erop wijst dat een sterkere, snellere alarmreactie hielp het virus onder controle te houden voordat het zich wijd kon verspreiden.
Minder ontspoorde ontsteking, minder orgaanschade
Ernstige virusinfecties kunnen een "cytokinestorm" veroorzaken, een overweldigende ontstekingsreactie die organen beschadigt. De wetenschappers maten verschillende belangrijke ontstekingsmoleculen in weefsels en bloed. Normale muizen geïnfecteerd met pseudorabiesvirus vertoonden hoge niveaus van deze factoren in milt, longen en hersenen, samen met sterke infiltratie van ontstekingscellen. Ter vergelijking hadden OASL1-deficiënte muizen veel lagere niveaus van deze ontstekingssignalen. Onder de microscoop behielden hun milten immuuncellen in plaats van deze te verliezen door celdood, hadden hun longen mildere ontstekingsveranderingen en lieten hun hersenen veel minder degeneratie van zenuwcellen in de hippocampus zien, een regio die cruciaal is voor geheugen. Het weghalen van OASL1 hielp dus niet alleen het virus te verwijderen, maar voorkwam ook overmatige ontsteking en weefselschade.
Inzoomen op de sleutelregelaar
Om te begrijpen hoe OASL1 deze respons vormgeeft, onderzocht het team IRF7, de schakelaar die interferonproductie aandrijft. Bij muizen zonder OASL1 waren IRF7-niveaus consequent hoger in milt, longen, hersenen en in gekweekte immuuncellen zoals macrofagen en microglia na infectie, terwijl een verwant factor, IRF3, weinig veranderde. Deze cellen secreteerden meer type I interferonen en ondersteunden minder virusreplicatie. Toen de onderzoekers kleine interfererende RNA’s gebruikten om IRF7 specifiek neer te halen in OASL1-deficiënte macrofagen, verdween de versterkte interferonrespons en stegen de virusniveaus weer. Dit experiment toonde aan dat het beschermende effect van het ontbreken van OASL1 hoofdzakelijk afhangt van het vrijmaken van IRF7 zodat deze het antivirale programma volledig kan activeren.
Wat dit betekent voor de toekomst
In gewone taal functioneert OASL1 als een interne veiligheidsrem die voorkomt dat het antivirale alarm te lang blijft loeien. Tijdens een pseudorabiesinfectie treedt die rem te vroeg en te sterk in werking, waardoor het virus de kans krijgt zich te vermenigvuldigen en bijdraagt aan ernstige ziekte. Muizen die OASL1 missen, of bij wie OASL1 tijdelijk in belangrijke immuuncellen is uitgeschakeld, geven een snelle, door IRF7 gedreven interferonreactie die het virus effectiever opruimt terwijl een schadelijke cytokinestorm wordt vermeden. Deze bevindingen suggereren dat zorgvuldig getimede geneesmiddelen die deze rem tijdelijk versoepelen — alleen in het cruciale vroege venster van de infectie — varkens en mogelijk ook mensen zouden kunnen helpen beschermen tegen pseudorabies en verwante herpesvirussen. Zo’n therapie zou echter scherp afgesteld moeten zijn om te voorkomen dat de balans doorslaat van te weinig naar te veel immuunreactie.
Bronvermelding: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Trefwoorden: pseudorabiesvirus, aangeboren immuniteit, type I interferon, OASL1, IRF7