Clear Sky Science · pt
Modelo híbrido de seleção de características e classificação usando dados de alta dimensão baseado em um algoritmo metaheurístico para diagnóstico de câncer cerebral
Por que testes mais inteligentes para tumores cerebrais são importantes
Os tumores cerebrais estão entre os cânceres mais letais, e ainda assim os médicos enfrentam dificuldades para distinguir rapidamente e com precisão os diferentes tipos de tumor. Testes laboratoriais tradicionais podem ser lentos, e exames modernos baseados em genes geram um fluxo avassalador de dados: dezenas de milhares de medidas gênicas por paciente. Este estudo apresenta um método computacional que peneira esse ruído genético para encontrar um pequeno conjunto de genes-chave que ajudam a separar tumores perigosos de casos menos agressivos, com o objetivo de apoiar diagnósticos mais precisos e, em última instância, decisões de tratamento melhores.
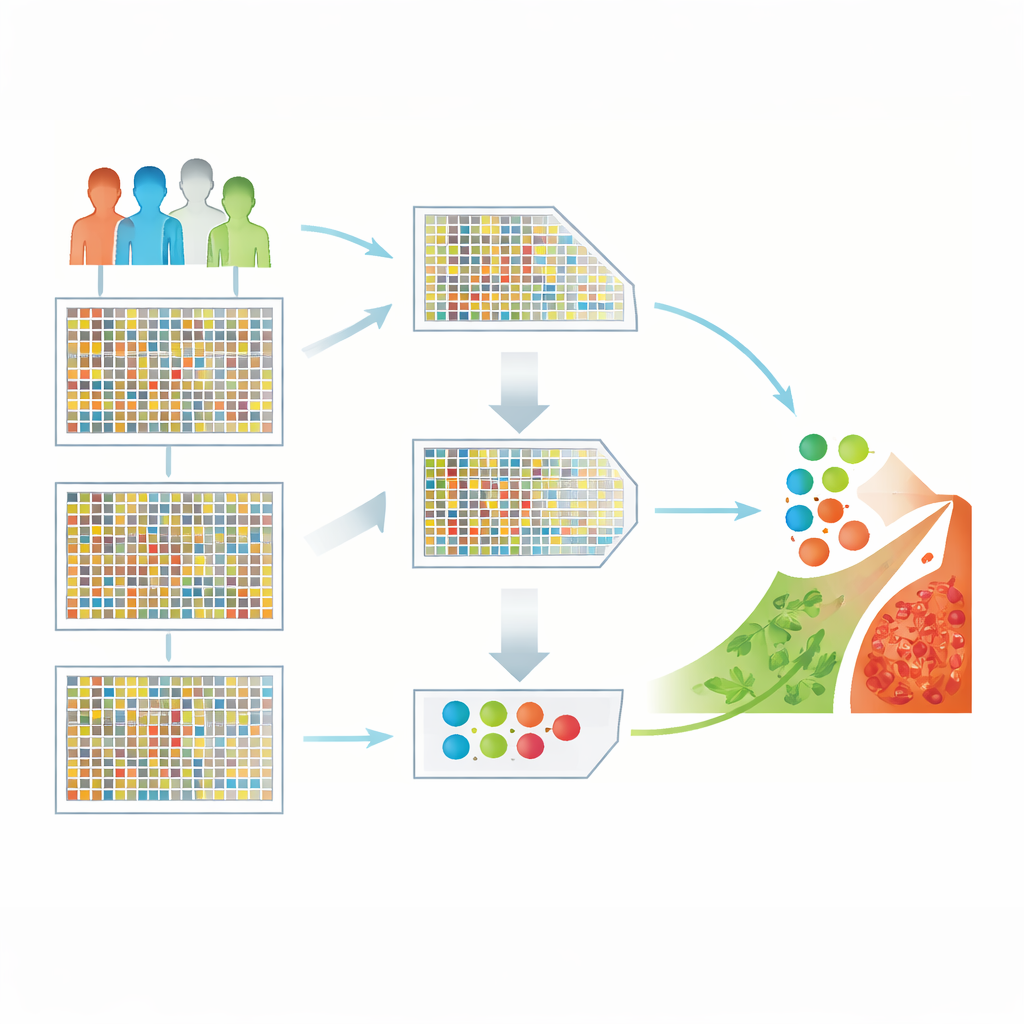
Transformando um mar de genes em pistas úteis
Os pesquisadores trabalharam com um conjunto de dados público de câncer cerebral contendo 130 amostras de pacientes, cada uma medida em mais de 54.000 genes. Esses dados de alta dimensão são poderosos, mas delicados: há muito mais medidas gênicas do que pacientes, e muitos genes são irrelevantes ou redundantes. Se alimentados diretamente a um algoritmo de aprendizagem, esse desequilíbrio pode levar a padrões enganosos e baixo desempenho em novos pacientes. O desafio central é manter apenas os genes mais informativos enquanto se descarta o resto, sem perder sinais biológicos importantes.
Uma abordagem em duas etapas para encontrar os genes mais reveladores
Para enfrentar isso, a equipe projetou um pipeline híbrido de seleção de características. Na primeira etapa, um filtro estatístico rápido chamado “mínima redundância, máxima relevância” (mRMR) examina todos os genes e preserva aqueles fortemente relacionados ao câncer cerebral e que sejam o mais diferentes possível entre si. Isso reduz rapidamente a lista de genes de dezenas de milhares para um conjunto mais manejável. Na segunda etapa, um método de busca inspirado no comportamento de caça das aves de rapina—Harris Hawks Optimization—trata cada subconjunto possível de genes como uma solução candidata e “caça” iterativamente combinações que produzem os melhores resultados de classificação. Juntas, essas etapas reduzem os 54.676 genes originais para apenas 50 que ainda capturam a essência da doença.
Treinando máquinas para traçar uma linha diagnóstica mais nítida
Uma vez identificado um conjunto compacto de genes, os autores treinaram vários modelos de aprendizado de máquina para distinguir entre cinco categorias de câncer cerebral e, mais amplamente, entre tecido maligno e menos perigoso. Um modelo-chave, a máquina de vetores de suporte, requer alguns ajustes de sensibilidade que afetam fortemente seu comportamento. Em vez de ajustar esses parâmetros por tentativa e erro, a equipe usou três estratégias de otimização—Particle Swarm Optimization, Differential Evolution e Harris Hawks Optimization—para buscar sistematicamente as melhores configurações. Avaliaram o desempenho usando validação cruzada rigorosa e repetida e verificações adicionais, como reamostragem bootstrap e análise de curva de aprendizado, para garantir que os modelos não estivessem apenas memorizando o conjunto de dados pequeno.
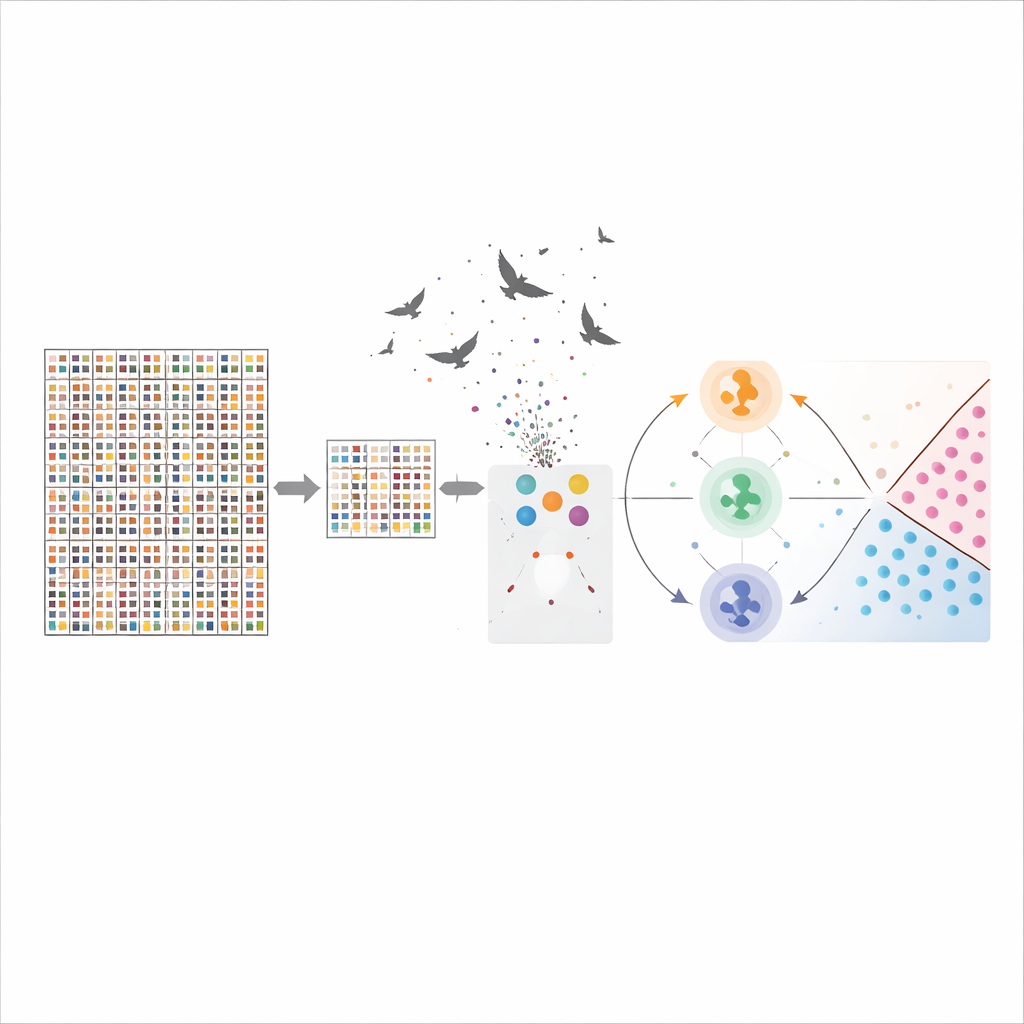
Quão bem o sistema funciona e o que os genes significam
Com a seleção híbrida de genes e a otimização em funcionamento, a máquina de vetores de suporte alcançou uma precisão de cerca de 96% nos dados de câncer cerebral, superando claramente métodos mais convencionais, como árvores de decisão. O método também reduziu o número de genes de mais de 54.000 para 50, preservando e até melhorando o poder preditivo. Muitos dos genes selecionados já são conhecidos por estarem envolvidos no crescimento celular, reparo de DNA, formação de vasos sanguíneos ou resposta imune em tumores cerebrais, conferindo credibilidade biológica às escolhas da máquina. Isso significa que o modelo não é apenas bom em classificar, mas também aponta aos pesquisadores potenciais biomarcadores que valem a pena ser estudados em laboratório.
O que isso pode significar para os pacientes
Em termos claros, o estudo mostra que é possível condensar um volume enorme de dados genéticos em uma pequena “assinatura” gênica significativa que ajuda a separar com alta confiabilidade os diferentes tipos de tumor cerebral. Embora o trabalho ainda seja baseado em um grupo relativamente pequeno de pacientes e precise ser testado em populações maiores e mais diversas, ele sugere um caminho para ferramentas de diagnóstico baseadas em genes que sejam rápidas, precisas e interpretáveis. Se validadas e integradas aos fluxos de trabalho clínicos, tais ferramentas poderiam dar aos médicos evidências mais sólidas ao escolher tratamentos e ajudar cientistas a se concentrarem em uma lista curta de genes mais prováveis de influenciar como os cânceres cerebrais se iniciam, crescem e respondem à terapia.
Citação: Manhrawy, I.I.M., Fathi, H., Alsekait, D.M. et al. Hybrid feature selection and classification model using high-dimensional data based on a metaheuristic algorithm for brain cancer diagnosis. Sci Rep 16, 11909 (2026). https://doi.org/10.1038/s41598-026-41573-5
Palavras-chave: diagnóstico de câncer cerebral, expressão gênica, seleção de características, aprendizado de máquina, biomarcadores