Clear Sky Science · pl
Hybrydowy model selekcji cech i klasyfikacji dla danych wysokiej wymiarowości oparty na algorytmie metaheurystycznym do diagnostyki raka mózgu
Dlaczego inteligentniejsze testy w kierunku guzów mózgu mają znaczenie
Guzy mózgu należą do najbardziej śmiertelnych nowotworów, a lekarze wciąż mają trudności z szybkim i precyzyjnym rozróżnieniem różnych typów guzów. Tradycyjne testy laboratoryjne mogą być powolne, a nowoczesne testy oparte na genach generują przytłaczającą ilość danych: dziesiątki tysięcy pomiarów genów dla każdego pacjenta. W tym badaniu przedstawiono metodę komputerową, która przesia ten genetyczny szum, aby znaleźć niewielki zestaw kluczowych genów pomagających oddzielić agresywne guzy od mniej złośliwych przypadków, z zamiarem wspierania bardziej precyzyjnej diagnozy i w efekcie lepszych decyzji terapeutycznych.
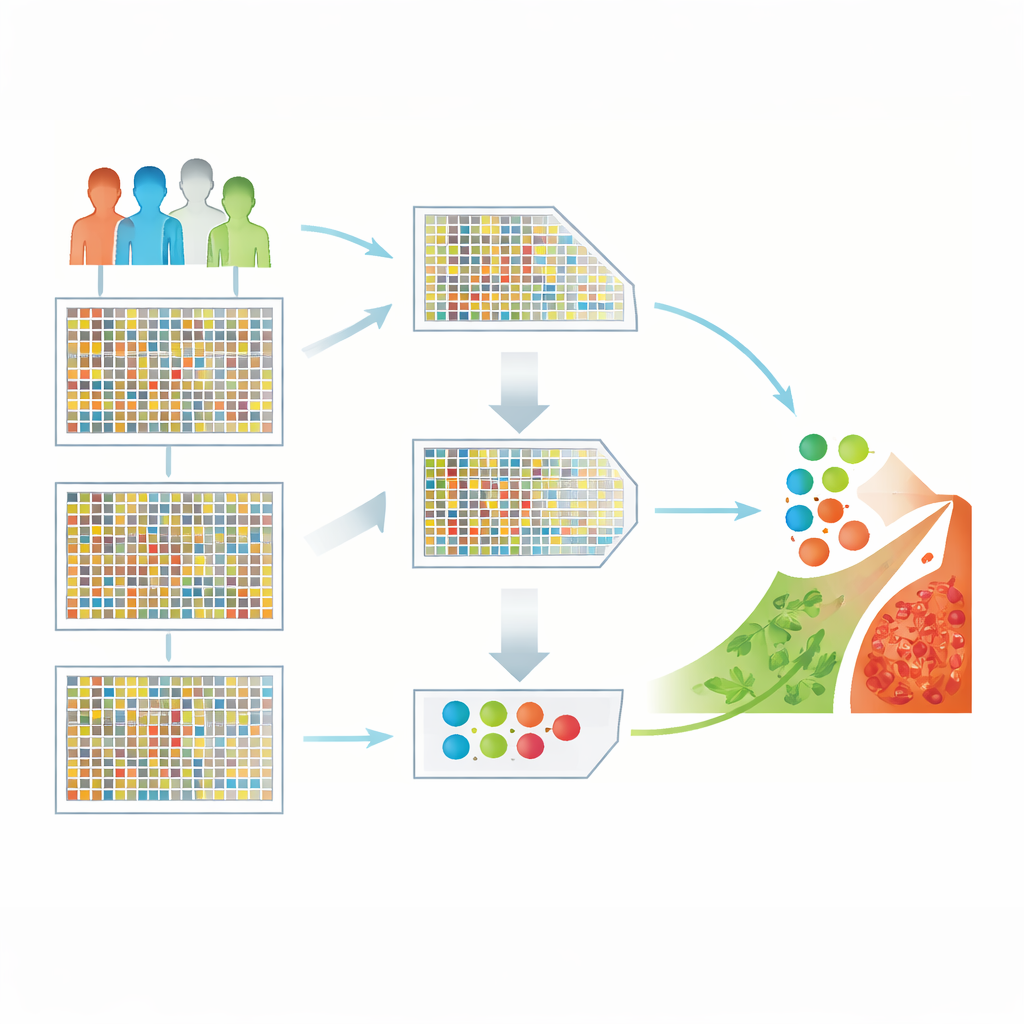
Zmiana morza genów w użyteczne wskazówki
Naukowcy pracowali na publicznym zbiorze danych dotyczących raka mózgu zawierającym 130 próbek pacjentów, z których każda obejmowała pomiary dla ponad 54 000 genów. Takie dane wysokiej wymiarowości są potężne, ale trudne w analizie: liczba pomiarów genów znacznie przewyższa liczbę pacjentów, a wiele genów jest nieistotnych lub redundantnych. Jeśli bezpośrednio podać je do algorytmu uczącego się, ta nierównowaga może prowadzić do mylących wzorców i słabej wydajności na nowych pacjentach. Głównym wyzwaniem jest pozostawienie tylko najbardziej informatywnych genów przy jednoczesnym odrzuceniu pozostałych, bez utraty ważnych sygnałów biologicznych.
Dwustopniowy sposób znalezienia najbardziej wymownych genów
Aby to rozwiązać, zespół zaprojektował hybrydowy proces selekcji cech. W pierwszym kroku szybki filtr statystyczny zwany „minimalna redundancja, maksymalna relewantność” (mRMR) skanuje wszystkie geny i zachowuje te, które są silnie powiązane z rakiem mózgu, jednocześnie będąc jak najbardziej od siebie różne. To szybko zmniejsza listę genów z dziesiątek tysięcy do bardziej zarządzalnego zbioru. W drugim kroku metoda poszukiwania inspirowana zachowaniami drapieżnych ptaków — Harris Hawks Optimization — traktuje każde możliwe podzbiory genów jako kandydatów rozwiązań i iteracyjnie „poluje” na kombinacje dające najlepsze wyniki klasyfikacji. Razem te etapy redukują początkowe 54 676 genów do zaledwie 50, które nadal oddają istotę choroby.
Nauczanie maszyn tworzenia ostrzejszej linii diagnostycznej
Gdy zidentyfikowano zwarty zestaw genów, autorzy wytrenowali kilka modeli uczenia maszynowego do rozróżniania pięciu kategorii raka mózgu, a także szerzej — między tkanką złośliwą a mniej niebezpieczną. Kluczowy model, maszyna wektorów nośnych (support vector machine), wymaga kilku parametrów wpływających na jego zachowanie. Zamiast stroić je metodą prób i błędów, zespół zastosował trzy strategie optymalizacyjne — Particle Swarm Optimization, Differential Evolution oraz Harris Hawks Optimization — aby systematycznie wyszukać najlepsze ustawienia. Wyniki oceniano za pomocą rygorystycznej, powtarzanej walidacji krzyżowej oraz dodatkowych kontroli, takich jak bootstrap i analiza krzywej uczenia, by upewnić się, że modele nie zapamiętują po prostu małego zbioru danych.
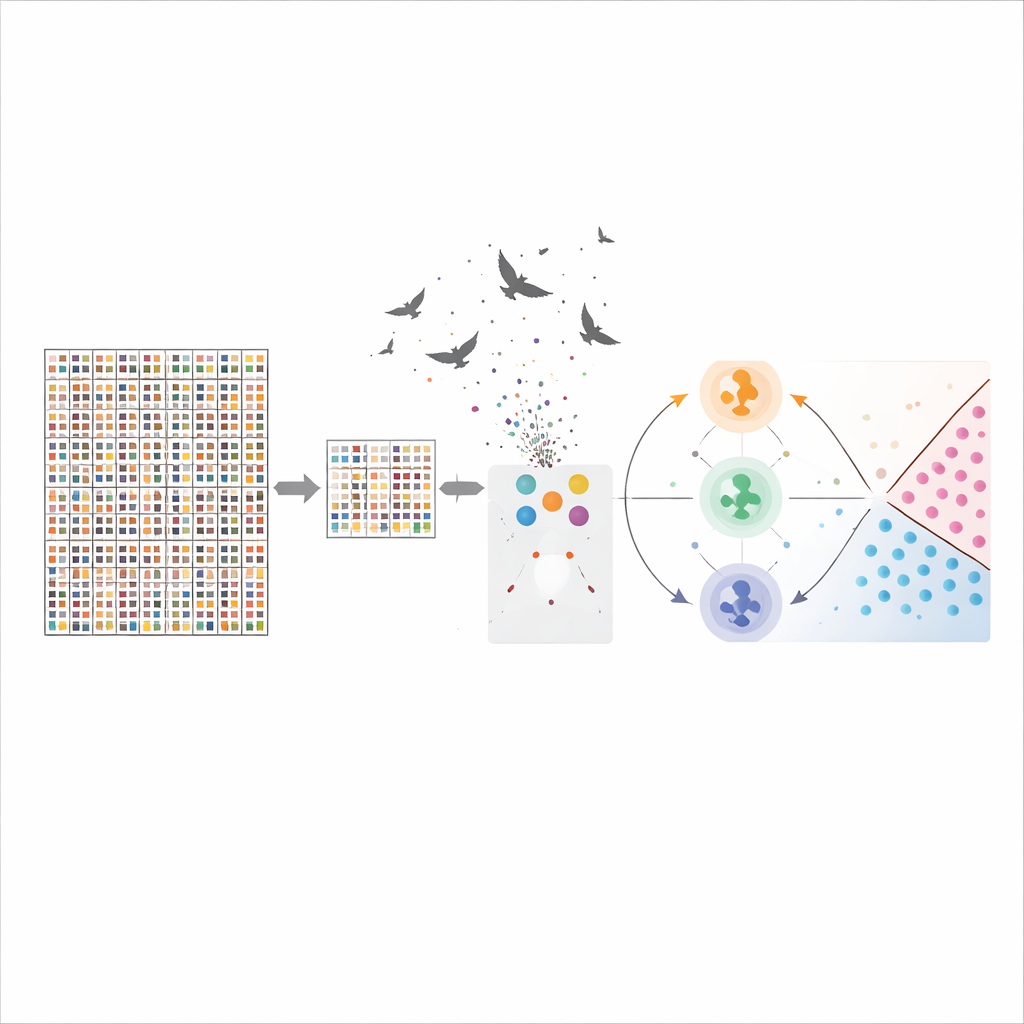
Jak system działa i co oznaczają wybrane geny
Dzięki hybrydowej selekcji genów i optymalizacji, maszyna wektorów nośnych osiągnęła dokładność około 96% na danych dotyczących raka mózgu, wyraźnie przewyższając bardziej konwencjonalne metody, takie jak drzewa decyzyjne. Metoda zmniejszyła też liczbę genów z ponad 54 000 do 50 przy jednoczesnym zachowaniu, a nawet poprawie, mocy predykcyjnej. Wiele z wybranych genów jest już znanych jako zaangażowane w wzrost komórek, naprawę DNA, tworzenie naczyń krwionośnych czy odpowiedź immunologiczną w guzach mózgu, co nadaje biologiczną wiarygodność wyborom komputera. Oznacza to, że model nie tylko sprawdza się w klasyfikacji, lecz także wskazuje badaczom potencjalne biomarkery warte dalszych badań laboratoryjnych.
Co to może znaczyć dla pacjentów
Mówiąc prosto, badanie pokazuje, że możliwe jest skompresowanie ogromnej objętości danych genetycznych do niewielkiego, znaczącego „sygnaturowego” zestawu genów, który pomaga z dużą niezawodnością rozdzielić różne typy guzów mózgu. Choć praca opiera się nadal na stosunkowo niewielkiej grupie pacjentów i wymaga testów na większych, bardziej zróżnicowanych populacjach, wskazuje drogę do szybszych, opartych na genach narzędzi diagnostycznych, które są jednocześnie dokładne i możliwe do interpretacji. Jeśli zostaną zwalidowane i zintegrowane z praktyką kliniczną, takie narzędzia mogłyby dostarczyć lekarzom mocniejszych dowodów przy wyborze terapii i pomóc naukowcom skupić się na krótkiej liście genów, które najprawdopodobniej wpływają na powstawanie, wzrost i odpowiedź nowotworów mózgu na leczenie.
Cytowanie: Manhrawy, I.I.M., Fathi, H., Alsekait, D.M. et al. Hybrid feature selection and classification model using high-dimensional data based on a metaheuristic algorithm for brain cancer diagnosis. Sci Rep 16, 11909 (2026). https://doi.org/10.1038/s41598-026-41573-5
Słowa kluczowe: diagnostyka raka mózgu, ekspresja genów, selekcja cech, uczenie maszynowe, biomarkery