Clear Sky Science · de
Hybrides Merkmal-Auswahl- und Klassifikationsmodell für hochdimensionale Daten basierend auf einem metaheuristischen Algorithmus zur Diagnose von Gehirntumoren
Warum klügere Tests bei Gehirntumoren wichtig sind
Gehirntumoren gehören zu den tödlichsten Krebsarten, dennoch fällt es Ärzten oft schwer, verschiedene Tumortypen schnell und zuverlässig zu unterscheiden. Traditionelle Labortests können langsam sein, und moderne genbasierte Tests erzeugen eine überwältigende Datenmenge: Zehntausende Genmessungen pro Patient. Diese Studie stellt eine computerbasierte Methode vor, die dieses genetische Rauschen durchforstet, um eine kleine Gruppe von Schlüsselgenen zu finden, die helfen, gefährliche Tumoren von weniger aggressiven Fällen zu trennen. Ziel ist es, präzisere Diagnosen und langfristig bessere Therapieentscheidungen zu unterstützen.
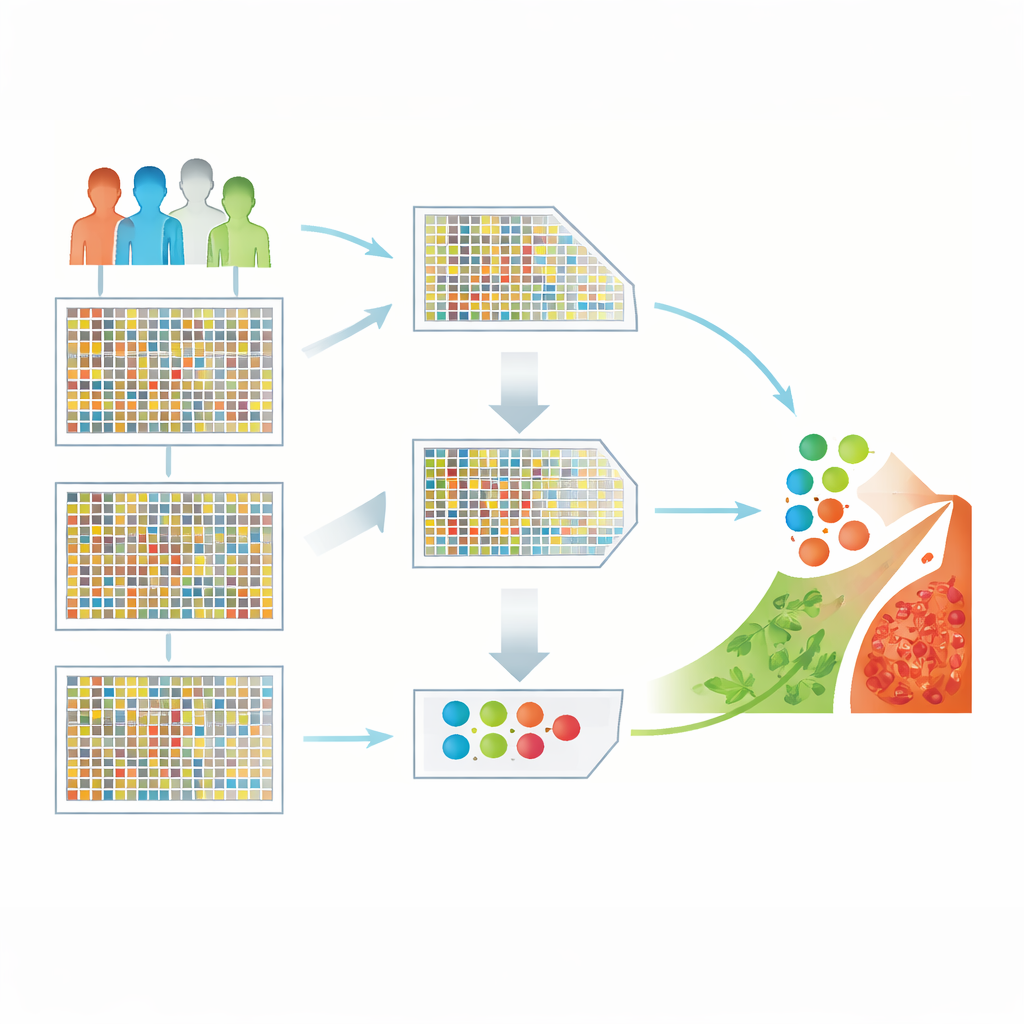
Aus einem Meer von Genen verwertbare Hinweise machen
Die Forschenden arbeiteten mit einem öffentlichen Gehirntumor-Datensatz mit 130 Patientenproben, für die jeweils mehr als 54.000 Gene gemessen wurden. Solche hochdimensionalen Daten sind mächtig, aber schwierig: Es gibt viel mehr Genmessungen als Patienten, und viele Gene sind irrelevant oder redundant. Würde man die Rohdaten direkt in einen Lernalgorithmus füttern, könnte dieses Ungleichgewicht zu irreführenden Mustern und schlechter Leistung bei neuen Patienten führen. Die zentrale Herausforderung besteht darin, nur die informativsten Gene zu behalten und den Rest wegzufiltern, ohne wichtige biologische Signale zu verlieren.
Ein zweistufiger Weg, die aussagekräftigsten Gene zu finden
Um das Problem anzugehen, entwickelte das Team eine hybride Pipeline zur Merkmalsauswahl. Im ersten Schritt durchläuft ein schneller statistischer Filter namens „Minimum Redundancy, Maximum Relevance“ (mRMR) alle Gene und behält diejenigen, die stark mit Gehirntumoren verbunden sind und gleichzeitig möglichst unterschiedlich zueinander sind. Das reduziert die Genliste rasch von Zehntausenden auf eine handlichere Menge. Im zweiten Schritt nutzt eine Suchmethode, inspiriert vom Jagdverhalten greifvogelartiger Vögel — die Harris Hawks Optimization — jede mögliche Genuntermenge als Kandidatlösung und „jagt“ iterativ nach Kombinationen, die die besten Klassifikationsergebnisse liefern. Zusammen reduzieren diese Stufen die ursprünglichen 54.676 Gene auf nur 50, die dennoch das Wesen der Erkrankung einfangen.
Maschinen beibringen, eine schärfere diagnostische Trennlinie zu ziehen
Sobald ein kompaktes Genset identifiziert war, trainierten die Autorinnen und Autoren mehrere Modelle des maschinellen Lernens, um zwischen fünf Kategorien von Gehirntumoren sowie allgemein zwischen malignem und weniger gefährlichem Gewebe zu unterscheiden. Ein zentrales Modell, die Support-Vektor-Maschine, benötigt einige Sensitivitätsregler, die ihr Verhalten stark beeinflussen. Statt diese per Trial-and-Error einzustellen, nutzte das Team drei Optimierungsstrategien — Particle Swarm Optimization, Differential Evolution und Harris Hawks Optimization — um systematisch nach den besten Parametereinstellungen zu suchen. Die Leistung bewerteten sie mit rigoroser, wiederholter Kreuzvalidierung und zusätzlichen Prüfungen wie Bootstrap-Resampling und Analyse von Lernkurven, um sicherzustellen, dass die Modelle nicht einfach das kleine Datenset auswendig lernen.
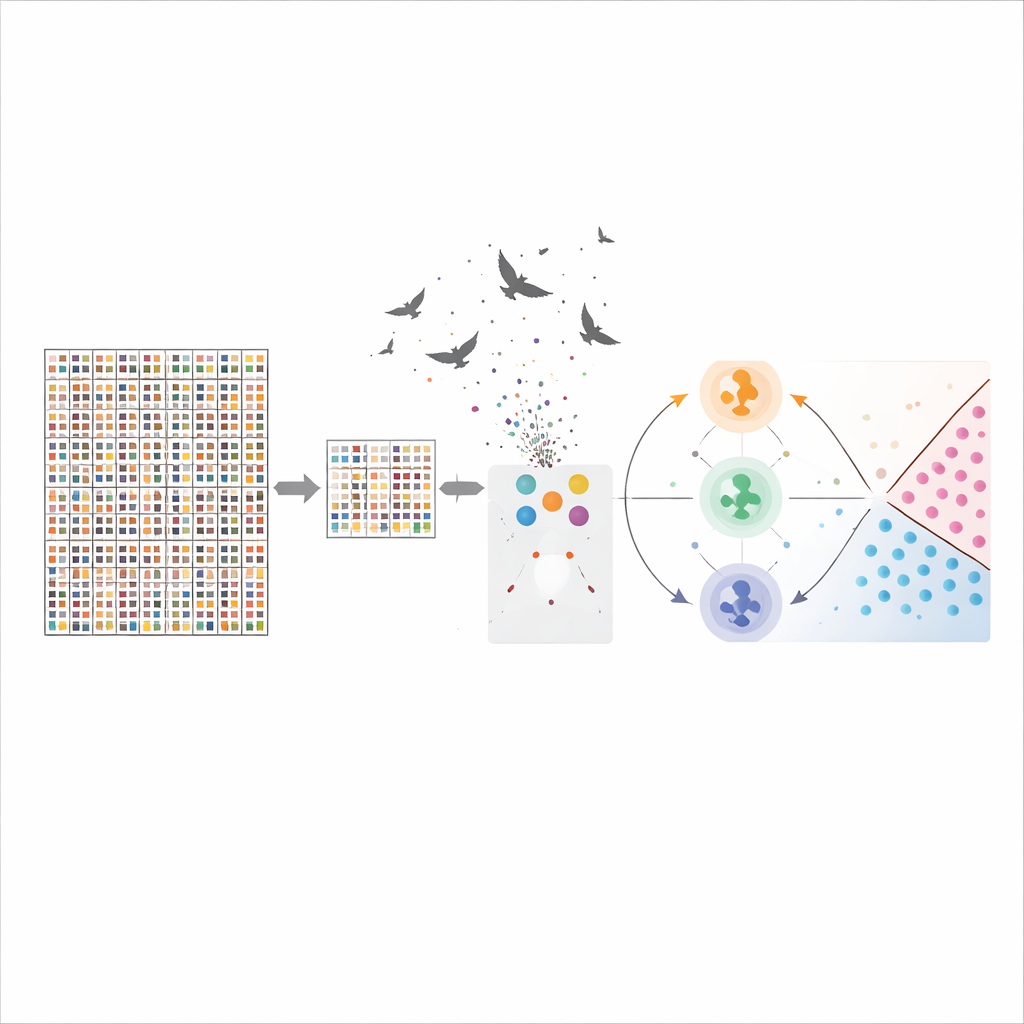
Wie gut das System funktioniert und was die Gene bedeuten
Mit der hybriden Merkmalsauswahl und Optimierung erreichte die Support-Vektor-Maschine eine Genauigkeit von etwa 96 % auf den Gehirntumordaten und übertraf damit deutlich konventionellere Methoden wie Entscheidungsbäume. Die Methode reduzierte außerdem die Anzahl der Gene von über 54.000 auf 50, während die Vorhersagekraft erhalten blieb oder sich sogar verbesserte. Viele der ausgewählten Gene sind bereits dafür bekannt, an Zellwachstum, DNA-Reparatur, Blutgefäßbildung oder Immunantwort bei Gehirntumoren beteiligt zu sein, was den computerbasierten Auswahlentscheidungen biologische Glaubwürdigkeit verleiht. Das bedeutet, dass das Modell nicht nur gut klassifiziert, sondern Forschende auch auf potenzielle Biomarker hinweist, die im Labor weiter untersucht werden sollten.
Was das für Patientinnen und Patienten bedeuten könnte
Einfach ausgedrückt zeigt die Studie, dass es möglich ist, ein enormes Volumen genetischer Daten auf eine kleine, aussagekräftige Gen-„Signatur“ zu komprimieren, die verschiedene Gehirntumortypen mit hoher Zuverlässigkeit trennt. Die Arbeit basiert zwar noch auf einer relativ kleinen Patientengruppe und muss an größeren, diverseren Populationen getestet werden, deutet aber auf einen Weg zu schnelleren, genbasierten Diagnosetools hin, die sowohl genau als auch interpretierbar sind. Wenn solche Werkzeuge validiert und in klinische Abläufe integriert werden, könnten sie Ärztinnen und Ärzten stärkere Entscheidungsgrundlagen für die Therapieauswahl liefern und Forschenden helfen, sich auf eine kurze Liste von Genen zu konzentrieren, die wahrscheinlich Einfluss darauf haben, wie Gehirntumoren entstehen, wachsen und auf Therapien reagieren.
Zitation: Manhrawy, I.I.M., Fathi, H., Alsekait, D.M. et al. Hybrid feature selection and classification model using high-dimensional data based on a metaheuristic algorithm for brain cancer diagnosis. Sci Rep 16, 11909 (2026). https://doi.org/10.1038/s41598-026-41573-5
Schlüsselwörter: Diagnose von Gehirntumoren, Genexpressionsdaten, Merkmalsauswahl, maschinelles Lernen, Biomarker