Clear Sky Science · pt
Análise matemática de um modelo estocástico com atraso para a dinâmica do vírus sincicial respiratório
Por que este estudo importa para a saúde do dia a dia
O vírus sincicial respiratório (VSR) é mais conhecido por lotar enfermarias pediátricas todo inverno, mas o mesmo vírus também ameaça idosos e pessoas com sistema imunológico debilitado. As agências de saúde precisam de previsões confiáveis sobre como o VSR se espalha em uma comunidade e como medidas de controle podem alterar seu curso. Este artigo aborda um problema sutil por trás dessas previsões: a maioria dos modelos matemáticos ignora a aleatoriedade e os atrasos no desenrolar da infecção, o que pode tornar as previsões de computador enganosas justamente quando mais são necessárias. Os autores constroem um modelo mais realista de propagação do VSR e, crucialmente, uma forma mais segura de simulá‑lo em computador para que as previsões permaneçam confiáveis mesmo em condições incertas.

Dividindo o surto em grupos simples
O estudo começa dividindo a população em cinco grupos: pessoas suscetíveis ao VSR, aquelas expostas mas ainda não contagiosas, as com infecções comuns, as que espalham o vírus muito mais do que a média (super‑propagadores) e as que se recuperaram. O modelo também incorpora um período de espera entre o momento em que alguém é infectado e o instante em que começa a transmitir o vírus. Durante esse atraso, as pessoas ainda podem morrer por outras causas, então os autores consideram a probabilidade de que um infectado simplesmente não viva tempo suficiente para se tornar contagioso. Com esses elementos, eles escrevem um conjunto de equações que descrevem como as pessoas se movem entre os grupos ao longo do tempo e mostram que a população total permanece dentro de limites realistas e nunca se torna negativa — uma verificação básica, porém essencial, para qualquer modelo de doença.
Identificando o ponto de inflexão de uma epidemia
Usando sua estrutura com atraso, os pesquisadores calculam o “número básico de reprodução”, um limiar que indica se o VSR desaparecerá ou continuará circulando. Esse número combina quão rapidamente as pessoas se misturam, quanto tempo permanecem contagiosas, a probabilidade de se tornarem super‑propagadores e a expectativa de vida. Se o número de reprodução for inferior a um, as infecções acabam por desaparecer; se for superior a um, o vírus se estabelece em uma presença estável. A equipe demonstra matematicamente que seu modelo se comporta exatamente dessa maneira: um equilíbrio corresponde a uma comunidade livre de VSR, o outro a um nível contínuo, porém estável, de infecção. Eles também mostram que esses resultados permanecem estáveis mesmo quando o atraso e outros parâmetros variam dentro de intervalos razoáveis.
Encontrando o que mais importa para o controle
Como muitas entradas do modelo são incertas, os autores testam quão sensível é o número de reprodução a cada uma delas. Eles descobrem que fatores que aumentam a taxa de novas infecções — como a frequência de contatos entre pessoas ou a rapidez com que expostos se tornam infecciosos — empurram o sistema para surtos maiores. Em contraste, fatores que reduzem o período infeccioso ou aumentam as taxas de mortalidade natural puxam o número de reprodução para baixo. Esse tipo de classificação de sensibilidade ajuda planejadores de saúde pública a ver quais alavancas são mais poderosas: por exemplo, estratégias que encurtem efetivamente quanto tempo as pessoas permanecem infecciosas, ou que reduzam oportunidades de super‑propagação, podem ter impacto desproporcional na transmissão do VSR.
Adicionando aleatoriedade e simulações de computador mais seguras
Epidemias reais não se desenrolam como curvas suaves. Os autores, portanto, estendem seu modelo para incluir flutuações ambientais aleatórias e incerteza em processos-chave, como transmissão e recuperação. Eles constroem duas versões estocásticas: uma baseada em uma lista detalhada de eventos possíveis (como uma infecção ou recuperação ocorrendo em uma pequena janela temporal) e outra que perturba cada grupo com ruído aleatório. Esses modelos mais ricos refletem melhor surtos irregulares e picos inesperados. No entanto, métodos computacionais padrão usados para resolver tais modelos podem se comportar mal: para passos de tempo grandes, podem gerar números negativos de pacientes ou oscilações explosivas sem significado biológico.
Uma nova ferramenta numérica robusta
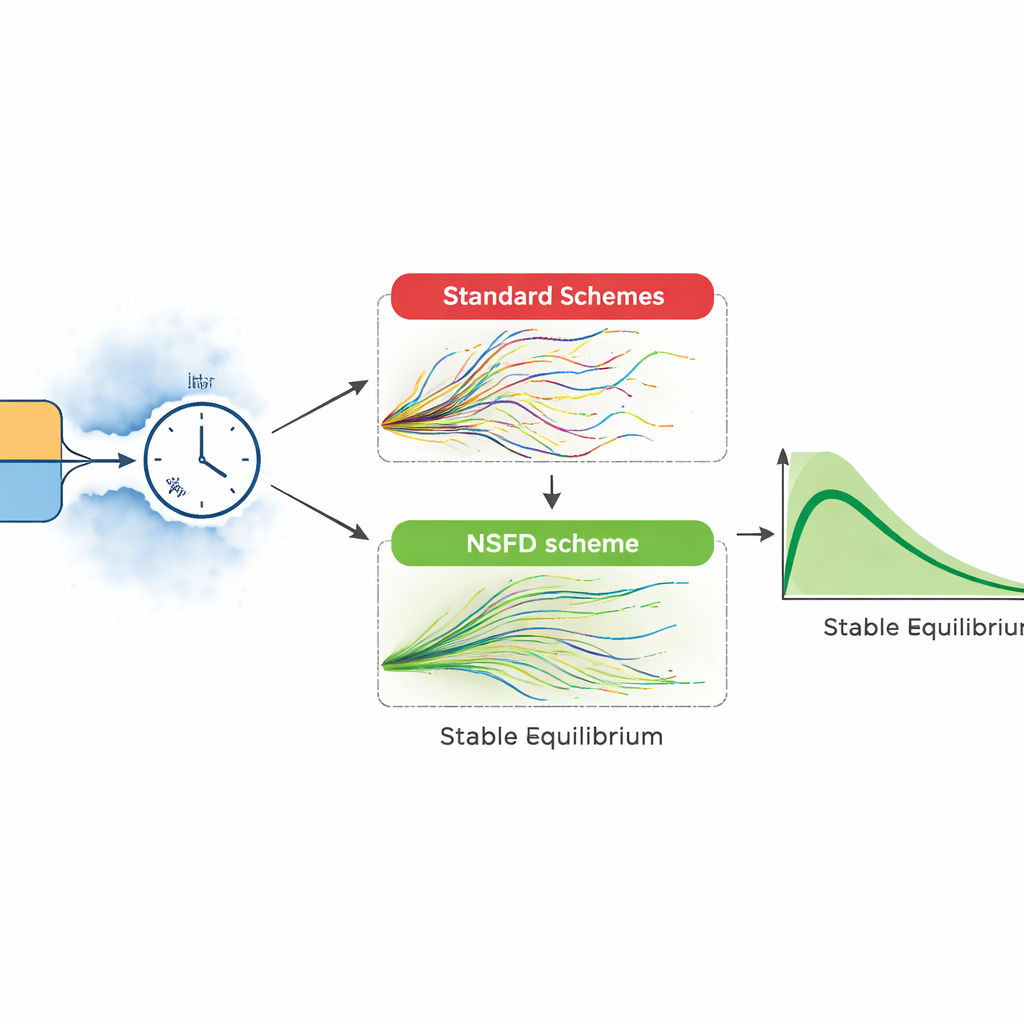
Para superar esses problemas, o artigo introduz um esquema estocástico de “diferenças finitas não padronizadas” projetado para respeitar a biologia do problema. Nessa abordagem, a deriva, ou movimento médio do sistema, é tratada com cuidado para que os números simulados de suscetíveis, infectados e recuperados permaneçam sempre não negativos e dentro de limites sensatos, mesmo quando a aleatoriedade é intensa. Os autores provam que esse esquema permanece estável para qualquer tamanho de passo temporal e, em seguida, testam‑no contra métodos amplamente usados, como Euler–Maruyama e Runge–Kutta estocástico. Em experimentos numéricos comparativos, os métodos convencionais funcionam apenas para passos muito pequenos; quando o tamanho do passo aumenta, eles geram oscilações irreais e até populações negativas. O novo esquema continua a acompanhar suavemente o curso esperado da infecção, correspondendo aos equilíbrios teóricos do modelo.
O que isso significa para a compreensão do VSR
Para não especialistas, a mensagem principal é que a forma como simulamos uma epidemia pode ser tão importante quanto as próprias equações. Este trabalho entrega um modelo detalhado de VSR que captura ao mesmo tempo atrasos e aleatoriedade, e um método computacional acompanhante que mantém as previsões com significado físico em uma ampla gama de condições. Uma ferramenta assim pode ajudar pesquisadores e formuladores de políticas a explorar cenários “e se” — como mudanças nos padrões de contato ou estratégias voltadas a super‑propagadores — sem se preocupar de que falhas numéricas estejam conduzindo os resultados. A longo prazo, abordagens como esta podem apoiar um planejamento mais confiável de campanhas de vacinação contra o VSR e outras intervenções destinadas a manter sob controle os picos sazonais.
Citação: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Palavras-chave: vírus sincicial respiratório, modelagem de epidemias, dinâmica estocástica, simulação numérica, transmissão de doenças