Clear Sky Science · de
Mathematische Analyse eines stochastischen Verzögerungsmodells für die Dynamik des respiratorischen Synzytialvirus
Warum diese Studie für die allgemeine Gesundheit wichtig ist
Das respiratorische Synzytialvirus (RSV) ist vor allem dafür bekannt, jedes Jahr die Pädiatrie-Stationen im Winter zu füllen, bedroht aber gleichermaßen ältere Erwachsene und Menschen mit geschwächtem Immunsystem. Gesundheitsbehörden benötigen verlässliche Prognosen darüber, wie sich RSV in einer Gemeinschaft ausbreitet und wie Eingriffe den Verlauf verändern könnten. Diese Arbeit geht ein subtiles Problem hinter solchen Vorhersagen an: Die meisten mathematischen Modelle lassen Zufälligkeiten und Verzögerungen im Infektionsverlauf außer Acht, wodurch Computervorhersagen gerade dann irreführend werden können, wenn sie am dringendsten gebraucht werden. Die Autorinnen und Autoren entwickeln ein realistisches Modell der RSV-Ausbreitung und — entscheidend — eine sicherere Art, es numerisch zu simulieren, sodass Prognosen auch unter unsicheren Bedingungen vertrauenswürdig bleiben.

Den Ausbruch in einfache Gruppen zerlegen
Die Studie beginnt damit, die Bevölkerung in fünf Gruppen zu unterteilen: empfängliche Personen, exponierte, noch nicht ansteckende Personen, gewöhnlich Infizierte, sogenannte Superverbreiter und Genesene. Das Modell berücksichtigt außerdem eine Wartezeit zwischen dem Moment der Ansteckung und dem Beginn der Ansteckungsfähigkeit. Während dieser Verzögerung können Menschen weiterhin an anderen Ursachen sterben, weshalb die Autorinnen und Autoren die Wahrscheinlichkeit einbeziehen, dass eine infizierte Person nicht lange genug lebt, um ansteckend zu werden. Mit diesen Elementen formulieren sie ein System von Gleichungen, das beschreibt, wie Menschen im Zeitverlauf zwischen den Gruppen wechseln, und zeigen, dass die Gesamtbevölkerung in realistischen Grenzen bleibt und niemals negativ wird — ein grundlegender, aber wesentlicher Check für jedes Krankheitsmodell.
Den Kipppunkt einer Epidemie bestimmen
Innerhalb ihres verzögerungsbasierten Rahmens berechnen die Forschenden die „basisreproduktionszahl“, eine Schwelle, die angibt, ob RSV ausstirbt oder weiter zirkuliert. Diese Zahl vereint, wie schnell Menschen sich mischen, wie lange sie ansteckend bleiben, wie wahrscheinlich Superverbreiter sind und wie lange Menschen leben. Liegt die Reproduktionszahl unter eins, verschwinden Infektionen mit der Zeit; liegt sie darüber, etabliert sich das Virus dauerhaft. Das Team beweist mathematisch, dass sich ihr Modell genau so verhält: Ein Gleichgewicht entspricht einer gemeinschaftsfreien Situation ohne RSV, das andere einem andauernden, aber stabilen Infektionsniveau. Sie zeigen außerdem, dass diese Ergebnisse stabil bleiben, selbst wenn Verzögerungen und andere Parameter innerhalb vernünftiger Bereiche variieren.
Herausfinden, was für die Kontrolle am wichtigsten ist
Da viele Eingangsgrößen des Modells unsicher sind, testen die Autorinnen und Autoren, wie empfindlich die Reproduktionszahl gegenüber einzelnen Parametern ist. Sie stellen fest, dass Faktoren, die die Rate neuer Infektionen erhöhen — etwa wie häufig Menschen Kontakt haben oder wie schnell exponierte Personen infektiös werden — das System in Richtung größerer Ausbrüche treiben. Demgegenüber drücken Faktoren, die die Infektiositätsdauer verkürzen oder die natürliche Sterberate erhöhen, die Reproduktionszahl nach unten. Diese Art von Sensitivitätsrangfolge hilft Planern im Gesundheitswesen zu erkennen, welche Stellschrauben am wirksamsten sind: Zum Beispiel können Maßnahmen, die die Zeitspanne verkürzen, in der Menschen ansteckend sind, oder die Möglichkeiten für Super‑Spreading reduzieren, einen überproportionalen Einfluss auf die RSV-Übertragung haben.
Zufälligkeiten hinzufügen und sicherere Computersimulationen
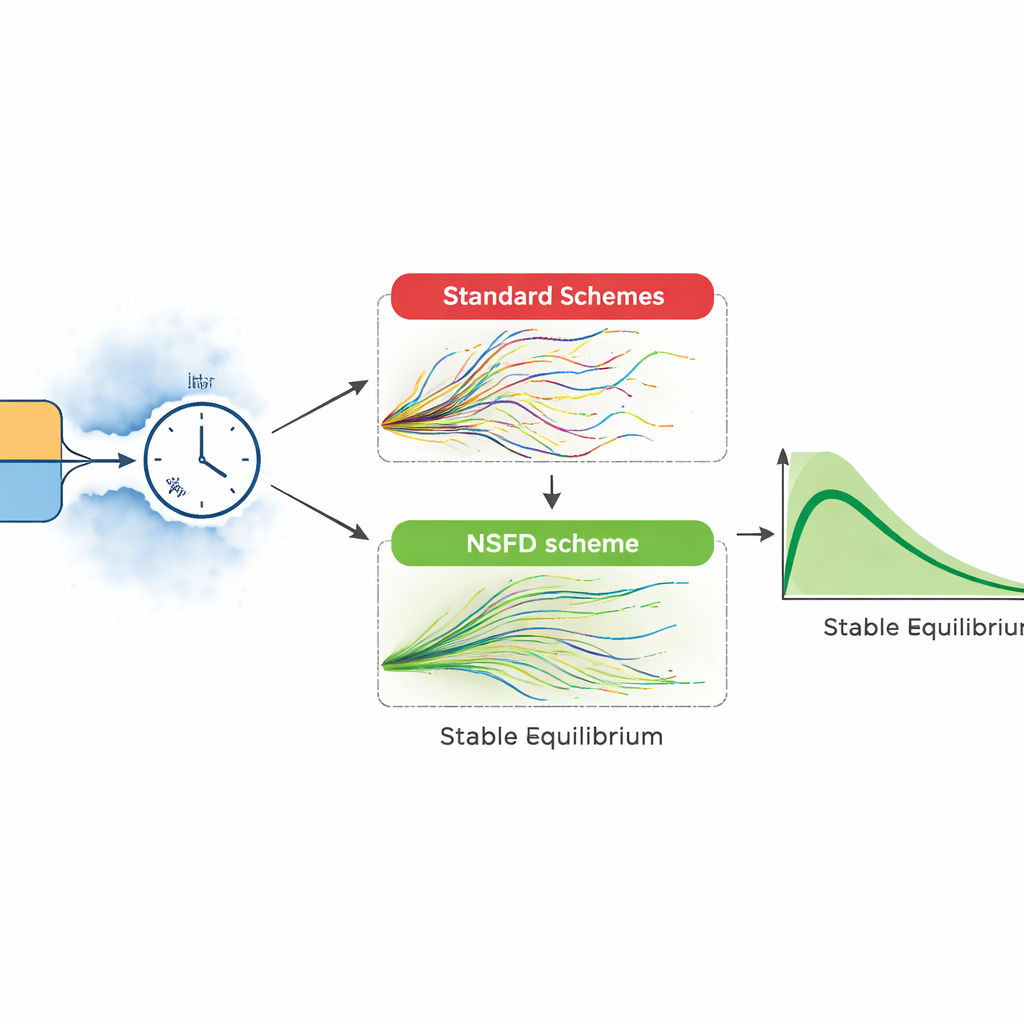
Reale Epidemien verlaufen nicht als glatte Kurven. Die Autorinnen und Autoren erweitern ihr Modell daher um zufällige Umweltfluktuationen und Unsicherheit in wichtigen Prozessen wie Übertragung und Genesung. Sie konstruieren zwei stochastische Versionen: eine, die aus einer detaillierten Liste möglicher Ereignisse (etwa eine Infektion oder Genesung in einem kurzen Zeitfenster) aufgebaut ist, und eine andere, die jede Gruppe mit zufälligem Rauschen stört. Diese reicheren Modelle spiegeln unregelmäßige Ausbrüche und unerwartete Schübe besser wider. Allerdings können Standard‑Numerikverfahren zur Lösung solcher Modelle problematisch sein: Bei großen Zeitschritten können sie negative Patientenzahlen oder explosive Schwankungen erzeugen, die biologisch keinen Sinn ergeben.
Ein robustes neues numerisches Werkzeug
Um diese Fallstricke zu umgehen, stellt die Arbeit ein stochastisches „nichtstandardmäßiges Differenzenverfahren“ vor, das darauf ausgelegt ist, die Biologie des Problems zu respektieren. Dabei wird die Drift, also die durchschnittliche Bewegung des Systems, so behandelt, dass die simulierten Zahlen von Suszeptiblen, Infizierten und Genesenen stets nichtnegativ und in sinnvollen Grenzen bleiben, selbst wenn die Zufälligkeit stark ist. Die Autorinnen und Autoren beweisen, dass dieses Schema für beliebige Zeitschrittgrößen stabil bleibt, und vergleichen es mit weit verbreiteten Methoden wie Euler–Maruyama und stochastischen Runge–Kutta‑Verfahren. In direkten numerischen Vergleichen funktionieren die konventionellen Methoden nur für sehr kleine Schritte; mit wachsender Schrittgröße erzeugen sie unrealistische Oszillationen und sogar negative Populationen. Das neue Schema folgt dagegen weiterhin dem erwarteten Infektionsverlauf glatt und stimmt mit den theoretischen Gleichgewichten des Modells überein.
Was das für das Verständnis von RSV bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die Art und Weise, wie wir eine Epidemie numerisch simulieren, genauso wichtig sein kann wie die Gleichungen selbst. Diese Arbeit liefert ein detailliertes RSV‑Modell, das sowohl Verzögerungen als auch Zufälligkeiten erfasst, sowie eine begleitende Rechenmethode, die Vorhersagen unter einer breiten Palette von Bedingungen physikalisch sinnvoll hält. Ein solches Werkzeug kann Forschenden und politischen Entscheidungsträgern helfen, „Was‑wäre‑wenn“-Szenarien zu untersuchen — etwa veränderte Kontaktmuster oder gezielte Maßnahmen gegen Superverbreiter — ohne befürchten zu müssen, dass numerische Artefakte die Ergebnisse treiben. Langfristig könnten Ansätze wie dieser eine verlässlichere Planung von RSV‑Impfkampagnen und anderen Interventionen unterstützen, die darauf abzielen, saisonale Spitzen unter Kontrolle zu halten.
Zitation: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Schlüsselwörter: respiratorisches Synzytialvirus, epidemische Modellierung, stochastische Dynamik, numerische Simulation, Erregerübertragung