Clear Sky Science · nl
Wiskundige analyse van een stochastisch vertragingmodel voor de dynamiek van respiratoir syncytieel virus
Waarom deze studie van belang is voor de dagelijkse gezondheid
Het respiratoir syncytieel virus (RSV) staat vooral bekend om volle kinderafdelingen in de winter, maar hetzelfde virus vormt ook een bedreiging voor oudere volwassenen en mensen met een verzwakt immuunsysteem. Gezondheidsinstanties hebben betrouwbare voorspellingen nodig over hoe RSV zich door een gemeenschap verspreidt en hoe beheersmaatregelen het verloop kunnen veranderen. Dit artikel pakt een subtiel probleem aan achter die voorspellingen: de meeste wiskundige modellen negeren willekeur en vertragingen in hoe een infectie zich ontwikkelt, wat computervoorspellingen misleidend kan maken juist wanneer ze het meest nodig zijn. De auteurs bouwen een realistischer model van RSV-verspreiding en, cruciaal, een veiliger manier om het op een computer te simuleren zodat voorspellingen ook onder onzekere omstandigheden betrouwbaar blijven.

De uitbraak onderverdeeld in eenvoudige groepen
De studie begint met het opdelen van de populatie in vijf groepen: mensen die vatbaar zijn voor RSV, zij die zijn blootgesteld maar nog niet besmettelijk, mensen met gewone infecties, zij die het virus veel meer verspreiden dan gemiddeld (superspreaders), en zij die hersteld zijn. Het model bouwt ook een wachttijd in tussen het moment van infectie en het moment waarop iemand het virus gaat overdragen. Tijdens deze vertraging kunnen mensen nog steeds overlijden aan andere oorzaken, dus de auteurs houden rekening met de kans dat een geïnfecteerde persoon simpelweg niet lang genoeg leeft om besmettelijk te worden. Met deze elementen schrijven ze een stel vergelijkingen die beschrijven hoe mensen in de loop van de tijd tussen groepen bewegen en tonen ze aan dat de totale populatie binnen realistische grenzen blijft en nooit negatief wordt — een eenvoudige maar essentiële controle voor elk ziektemodel.
Het kantelpunt van een epidemie vaststellen
Gebruikmakend van hun op vertragingen gebaseerde raamwerk berekenen de onderzoekers het “basisreproductiegetal”, een drempel die aangeeft of RSV zal uitsterven of blijven circuleren. Dit getal verenigt hoe snel mensen mengen, hoe lang ze besmettelijk blijven, hoe waarschijnlijk het is dat ze superspreaders worden, en hoe lang ze leven. Als het reproductiegetal onder de één ligt, verdwijnen besmettingen uiteindelijk; als het boven de één ligt, vestigt het virus zich in een blijvende aanwezigheid. Het team bewijst wiskundig dat hun model zich precies op deze manier gedraagt: het ene evenwicht correspondeert met een RSV-vrije gemeenschap, het andere met een aanhoudend, maar stabiel, infectieniveau. Ze tonen ook aan dat deze uitkomsten stabiel blijven wanneer de vertraging en andere parameters binnen redelijke grenzen variëren.
Vinden wat het meest van belang is voor beheersing
Aangezien veel modelinvoer onzeker is, testen de auteurs hoe gevoelig het reproductiegetal is voor elk van die inputs. Ze vinden dat factoren die de snelheid van nieuwe infecties verhogen — zoals hoe vaak mensen contact hebben of hoe snel blootgestelde personen besmettelijk worden — het systeem naar grotere uitbraken duwen. Daarentegen trekken factoren die de infectieuze periode verkorten of de natuurlijke sterfte verhogen het reproductiegetal omlaag. Dit soort gevoeligheidsranking helpt volksgezondheidsplanners te zien welke hefbomen het krachtigst zijn: bijvoorbeeld, strategieën die effectief verkorten hoe lang mensen besmettelijk zijn, of kansen op superverspreiding verminderen, kunnen een buitenproportioneel effect hebben op RSV-transmissie.
Willekeur toevoegen en veiligere computervarianten
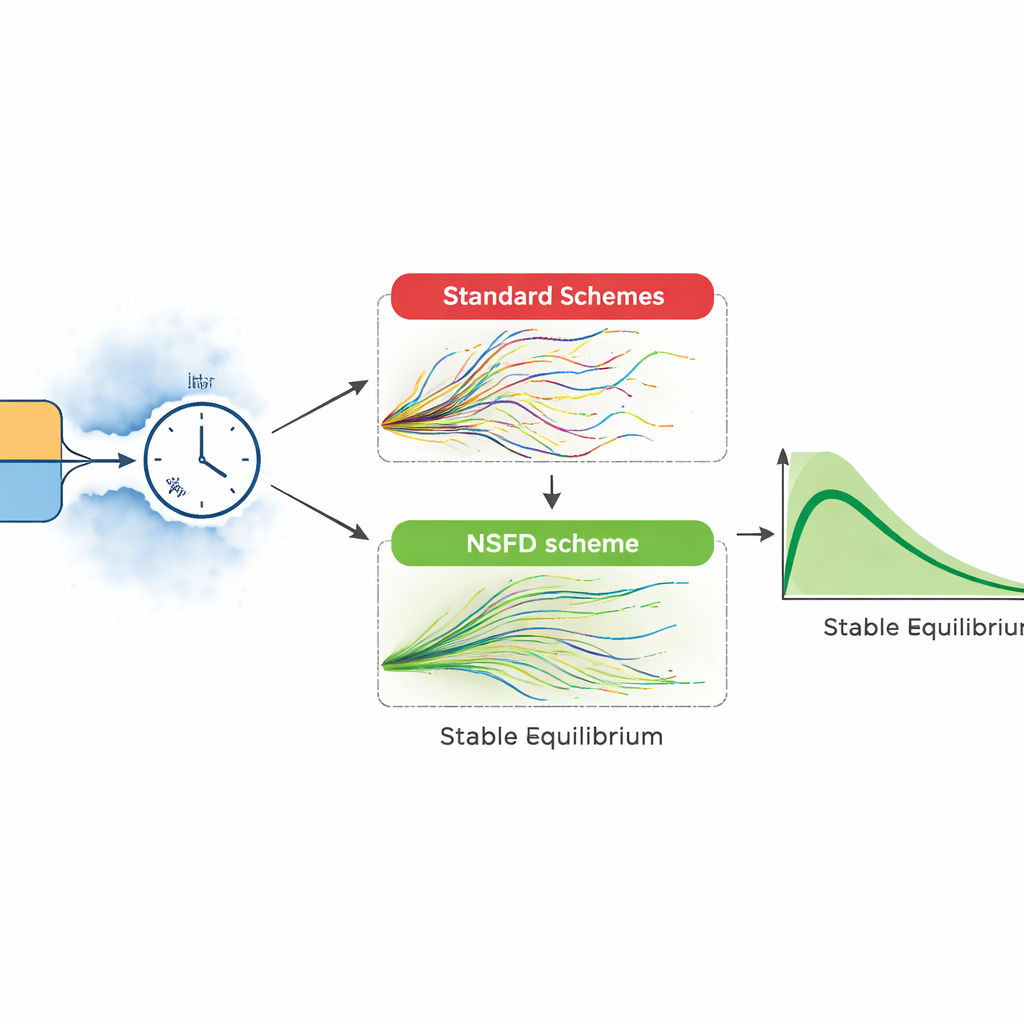
Werkelijke epidemieën ontvouwen zich niet als gladde krommen. Daarom breiden de auteurs hun model uit met willekeurige omgevingsfluctuaties en onzekerheid in belangrijke processen, zoals transmissie en herstel. Ze bouwen twee stochastische versies: één gebaseerd op een gedetailleerde lijst mogelijke gebeurtenissen (zoals een infectie of herstel dat plaatsvindt binnen een korte tijdsinterval) en een andere die elke groep verstoort met willekeurige ruis. Deze rijkere modellen weerspiegelen onregelmatige uitbraken en onverwachte pieken beter. Echter, standaard computermethoden om zulke modellen op te lossen kunnen slecht gedrag vertonen: bij grote tijdstappen kunnen ze negatieve aantallen patiënten of explosieve schommelingen genereren die geen biologische betekenis hebben.
Een robuust nieuw numeriek hulpmiddel
Om deze valkuilen te vermijden introduceert het artikel een stochastische “nonstandard finite difference”-methode die ontworpen is om de biologie van het probleem te respecteren. In deze aanpak wordt de drift, of het gemiddelde verloop van het systeem, zorgvuldig behandeld zodat de gesimuleerde aantallen vatbaren, geïnfecteerden en herstelden altijd niet-negatief en binnen redelijke grenzen blijven, zelfs wanneer de willekeur sterk is. De auteurs bewijzen dat dit schema stabiel blijft voor elke grootte van de tijdstap, en testen het vervolgens tegen veelgebruikte methoden zoals Euler–Maruyama en stochastische Runge–Kutta. In head-to-head numerieke experimenten werken de conventionele methoden alleen voor zeer kleine stappen; wanneer de stapgrootte toeneemt, produceren ze onrealistische oscillaties en zelfs negatieve populaties. Het nieuwe schema blijft het verwachte verloop van de infectie vloeiend volgen en komt overeen met de theoretische evenwichten van het model.
Wat dit betekent voor het begrip van RSV
Voor niet-specialisten is de kernboodschap dat de manier waarop we een epidemie simuleren net zo belangrijk kan zijn als de vergelijkingen zelf. Dit werk levert een gedetailleerd RSV-model dat zowel vertragingen als willekeur vastlegt, en een begeleidende computationele methode die voorspellingen fysiek zinvol houdt onder een breed scala aan omstandigheden. Zo’n hulpmiddel kan onderzoekers en beleidsmakers helpen bij het verkennen van “wat‑als”-scenario’s — zoals wijzigingen in contactpatronen of het richten op superspreaders — zonder zich zorgen te maken dat numerieke fouten de resultaten sturen. Op de lange termijn kunnen benaderingen als deze betrouwbaardere planning ondersteunen voor RSV-vaccinatiecampagnes en andere interventies gericht op het beheersen van seizoenspieken.
Bronvermelding: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Trefwoorden: respiratoir syncytieel virus, epidemiemodellering, stochastische dynamica, numerische simulatie, ziektetransmissie