Clear Sky Science · fr
Analyse mathématique d’un modèle stochastique à retard pour la dynamique du virus respiratoire syncytial
Pourquoi cette étude compte pour la santé quotidienne
Le virus respiratoire syncytial (VRS) est surtout connu pour remplir les services pédiatriques chaque hiver, mais ce même virus menace aussi les personnes âgées et les personnes immunodéprimées. Les agences de santé ont besoin de prévisions fiables sur la façon dont le VRS circule dans une communauté et sur l’effet des mesures de contrôle. Cet article s’attaque à un problème subtil sous-jacent à ces prévisions : la plupart des modèles mathématiques négligent l’aléa et les délais dans le déroulement de l’infection, ce qui peut rendre les prédictions informatiques trompeuses précisément quand elles sont les plus utiles. Les auteurs construisent un modèle de propagation du VRS plus réaliste et, surtout, une méthode de simulation informatique plus sûre afin que les prévisions restent dignes de confiance même en présence d’incertitudes.

Décomposer l’épidémie en groupes simples
L’étude commence par diviser la population en cinq groupes : les personnes susceptibles d’être infectées, celles qui ont été exposées mais ne sont pas encore contagieuses, les personnes infectées ordinaires, les personnes qui diffusent le virus beaucoup plus que la moyenne, et celles qui sont rétablies. Le modèle intègre aussi une période d’attente entre le moment de l’infection et le moment où la personne commence à transmettre le virus. Pendant ce délai, des individus peuvent mourir d’autres causes, donc les auteurs prennent en compte la probabilité qu’une personne infectée ne vive tout simplement pas assez longtemps pour devenir contagieuse. Avec ces éléments, ils écrivent un système d’équations décrivant les mouvements de population entre ces groupes au cours du temps et montrent que la population totale reste dans des limites réalistes et ne devient jamais négative — une vérification basique mais essentielle pour tout modèle de maladie.
Identifier le point de basculement d’une épidémie
En s’appuyant sur leur cadre à retard, les chercheurs calculent le « nombre de reproduction de base », un seuil indiquant si le VRS s’éteindra ou continuera de circuler. Ce nombre combine la fréquence des contacts entre personnes, la durée de la période de contagiosité, la probabilité de devenir un super‑propagateur et l’espérance de vie. Si le nombre de reproduction est inférieur à un, les infections finissent par disparaître ; s’il est supérieur à un, le virus s’établit à un niveau stable. L’équipe démontre mathématiquement que leur modèle obéit exactement à ce comportement : un équilibre correspond à une communauté exempte de VRS, l’autre à un niveau d’infection persistant mais stable. Ils montrent aussi que ces issues restent stables même lorsque le délai et d’autres paramètres varient dans des plages raisonnables.
Déterminer ce qui compte le plus pour le contrôle
Parce que de nombreuses entrées du modèle sont incertaines, les auteurs testent la sensibilité du nombre de reproduction à chacune d’elles. Ils constatent que les facteurs qui augmentent le taux de nouvelles infections — comme la fréquence des contacts ou la rapidité avec laquelle les exposés deviennent infectieux — poussent le système vers de plus grandes épidémies. En revanche, les facteurs qui réduisent la période d’infectiosité ou augmentent la mortalité naturelle font baisser le nombre de reproduction. Ce type de classement de sensibilité aide les planificateurs de santé publique à voir quels leviers sont les plus puissants : par exemple, des stratégies qui raccourcissent efficacement la durée d’infectiosité, ou réduisent les occasions de super‑propagation, peuvent avoir un impact disproportionné sur la transmission du VRS.
Ajouter de l’aléa et des simulations informatiques plus sûres
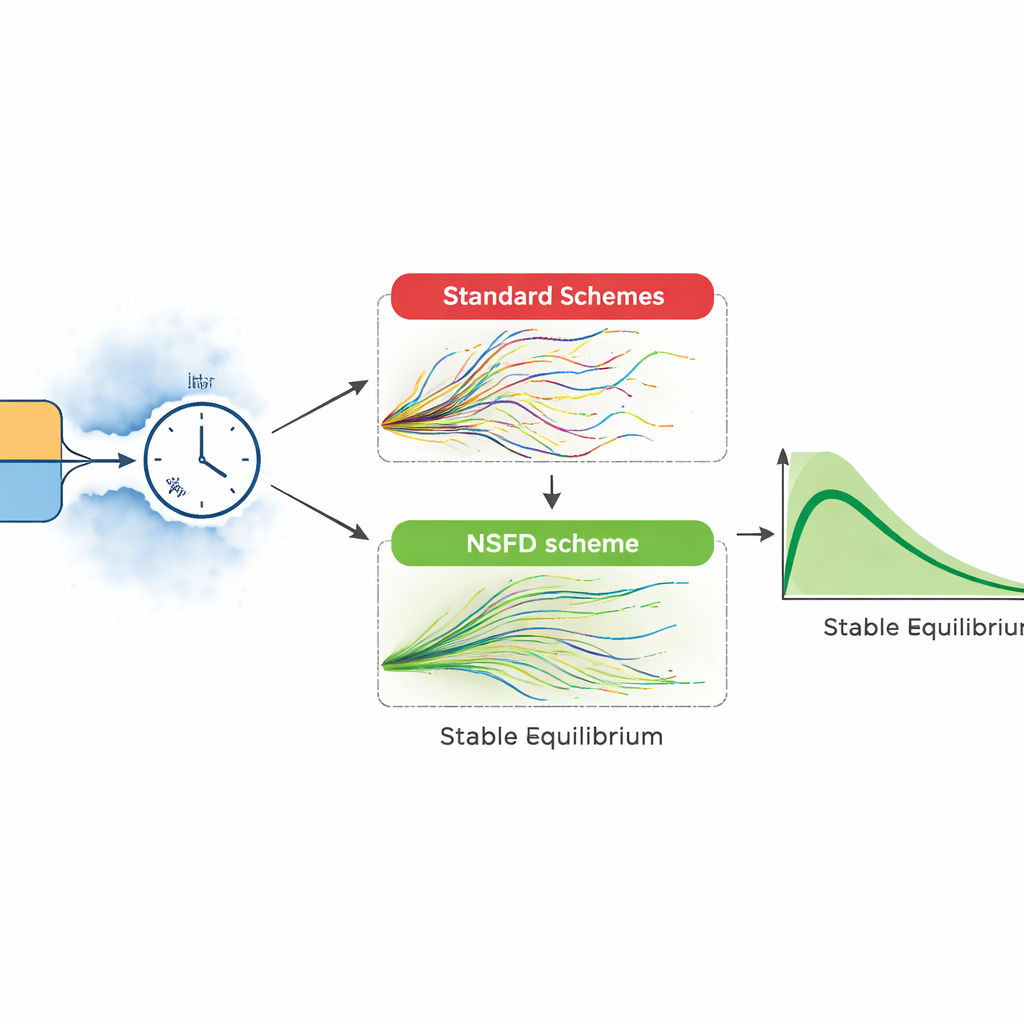
Les épidémies réelles ne suivent pas des courbes lisses. Les auteurs étendent donc leur modèle pour inclure des fluctuations environnementales aléatoires et l’incertitude dans des processus clés, comme la transmission et la guérison. Ils construisent deux versions stochastiques : l’une issue d’un inventaire détaillé d’événements possibles (par exemple une infection ou une guérison sur une courte fenêtre temporelle) et une autre qui perturbe chaque groupe par un bruit aléatoire. Ces modèles plus riches reflètent mieux les poussées irrégulières et les flambées inattendues. Toutefois, les méthodes informatiques classiques pour résoudre de tels modèles peuvent mal se comporter : pour des pas de temps importants, elles peuvent produire des nombres négatifs de malades ou des oscillations explosives sans sens biologique.
Un nouvel outil numérique robuste
Pour surmonter ces écueils, l’article présente un schéma stochastique « aux différences finies non standard » conçu pour respecter la biologie du problème. Dans cette approche, la dérive, c’est‑à‑dire le mouvement moyen du système, est traitée avec soin de sorte que les nombres simulés de susceptibles, d’infectés et de rétablis restent toujours non négatifs et dans des limites sensées, même lorsque l’aléa est fort. Les auteurs prouvent que ce schéma demeure stable pour n’importe quelle taille de pas de temps, puis le testent face à des méthodes couramment utilisées comme Euler–Maruyama et Runge–Kutta stochastique. Dans des expériences numériques comparatives, les méthodes classiques ne fonctionnent que pour des pas très petits ; lorsque le pas augmente, elles génèrent des oscillations irréalistes et même des populations négatives. Le nouveau schéma continue à suivre en douceur l’évolution attendue de l’infection, en accord avec les équilibres théoriques du modèle.
Ce que cela signifie pour la compréhension du VRS
Pour un public non spécialiste, le message clé est que la manière dont on simule une épidémie peut être aussi importante que les équations elles‑mêmes. Ce travail fournit un modèle détaillé du VRS qui capture à la fois les délais et l’aléa, ainsi qu’une méthode de calcul compagnon qui maintient les prédictions physiquement cohérentes dans un large éventail de conditions. Un tel outil peut aider les chercheurs et les décideurs à explorer des scénarios « et si » — comme modifier les patterns de contact ou cibler les super‑propagateurs — sans craindre que des artefacts numériques biaisent les résultats. À long terme, des approches de ce type pourraient soutenir une planification plus fiable des campagnes de vaccination contre le VRS et d’autres interventions visant à contenir les pics saisonniers.
Citation: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Mots-clés: virus respiratoire syncytial, modélisation épidémique, dynamique stochastique, simulation numérique, transmission des maladies