Clear Sky Science · es
Análisis matemático de un modelo estocástico con retardos para la dinámica del virus respiratorio sincitial
Por qué este estudio importa para la salud cotidiana
El virus respiratorio sincitial (VRS) es conocido sobre todo por llenar las salas pediátricas cada invierno, pero el mismo virus también amenaza a las personas mayores y a quienes tienen sistemas inmunitarios debilitados. Las agencias sanitarias necesitan pronósticos fiables sobre cómo se propaga el VRS en una comunidad y cómo las medidas de control pueden alterar su curso. Este artículo aborda un problema sutil detrás de esos pronósticos: la mayoría de los modelos matemáticos ignoran la aleatoriedad y los retardos en el desarrollo de la infección, lo que puede convertir las predicciones por ordenador en engañosas precisamente cuando más se necesitan. Los autores construyen un modelo más realista de la propagación del VRS y, crucialmente, una forma más segura de simularlo por ordenador para que las predicciones sigan siendo fiables incluso en condiciones de incertidumbre.

Descomponer el brote en grupos simples
El estudio comienza dividiendo la población en cinco grupos: personas susceptibles de contraer VRS, aquellas expuestas pero aún no contagiosas, las con infecciones ordinarias, quienes contagian mucho más de lo habitual (supercontagiadores) y las que se han recuperado. El modelo también incorpora un período de espera entre el momento en que alguien se infecta y el instante en que comienza a transmitir el virus. Durante este retardo, las personas pueden morir por otras causas, por lo que los autores tienen en cuenta la posibilidad de que una persona infectada no viva lo suficiente como para volverse contagiosa. Con estos elementos, escriben un conjunto de ecuaciones que describen cómo las personas se mueven entre los grupos a lo largo del tiempo y muestran que la población total se mantiene dentro de límites realistas y nunca se vuelve negativa —una comprobación básica pero esencial para cualquier modelo de enfermedad.
Localizar el punto crítico de una epidemia
Usando su marco con retardos, los investigadores calculan el «número básico de reproducción», un umbral que indica si el VRS desaparecerá o seguirá circulando. Este número combina cómo de rápido se mezclan las personas, cuánto tiempo permanecen contagiosas, la probabilidad de convertirse en supercontagiadores y la esperanza de vida. Si el número de reproducción está por debajo de uno, las infecciones desaparecen con el tiempo; si está por encima de uno, el virus se asienta en una presencia continua. El equipo demuestra matemáticamente que su modelo se comporta exactamente de esta manera: un equilibrio corresponde a una comunidad libre de VRS y el otro a un nivel estable de infección en curso. También muestran que estos resultados permanecen estables aun cuando el retardo y otros parámetros varían dentro de rangos razonables.
Encontrar lo que más importa para el control
Dado que muchas entradas del modelo son inciertas, los autores prueban cómo de sensible es el número de reproducción a cada una de ellas. Encuentran que los factores que aumentan la tasa de nuevas infecciones —como la frecuencia de los contactos o la rapidez con que las personas expuestas se vuelven infecciosas— empujan el sistema hacia brotes mayores. En contraste, los factores que reducen el periodo infeccioso o aumentan las tasas de mortalidad natural tiran el número de reproducción hacia abajo. Este tipo de clasificación de sensibilidad ayuda a los planificadores de salud pública a ver qué palancas son más poderosas: por ejemplo, las estrategias que acortan eficazmente el tiempo en que las personas son infecciosas, o que reducen las oportunidades de supercontagio, pueden tener un impacto desproporcionado en la transmisión del VRS.
Añadir aleatoriedad y simulaciones por ordenador más seguras
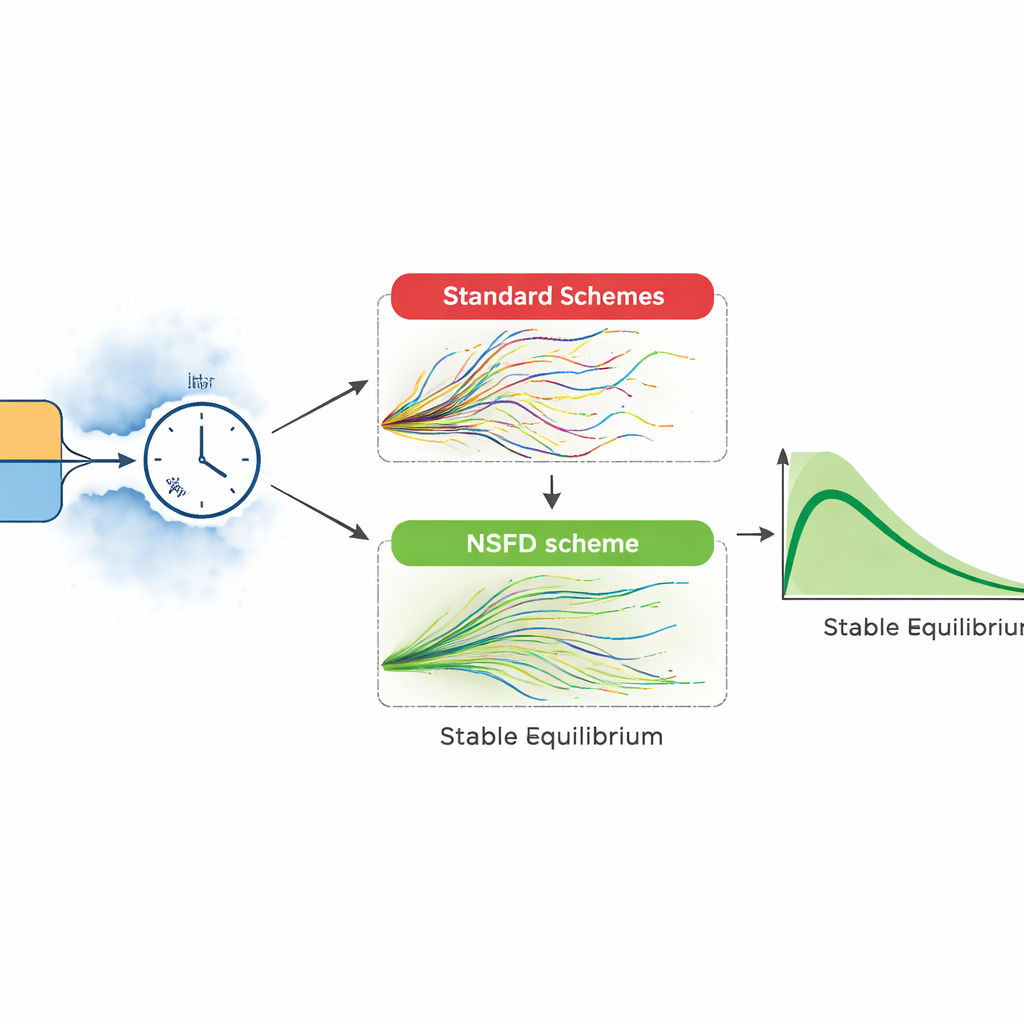
Las epidemias reales no se despliegan como curvas suaves. Por ello, los autores amplían su modelo para incluir fluctuaciones ambientales aleatorias e incertidumbre en procesos clave, como la transmisión y la recuperación. Construyen dos versiones estocásticas: una basada en una lista detallada de eventos posibles (como que ocurra una infección o una recuperación en una breve ventana temporal) y otra que perturba cada grupo con ruido aleatorio. Estos modelos más ricos reflejan mejor los brotes irregulares y los aumentos inesperados. Sin embargo, los métodos informáticos estándar usados para resolver tales modelos pueden comportarse mal: para pasos de tiempo grandes, pueden producir números negativos de pacientes o oscilaciones explosivas sin sentido biológico.
Una nueva herramienta numérica robusta
Para superar estos escollos, el artículo introduce un esquema estocástico de «diferencias finitas no estándar» diseñado para respetar la biología del problema. En este enfoque, la deriva, o movimiento medio del sistema, se maneja con cuidado para que los números simulados de susceptibles, infectados y recuperados se mantengan siempre no negativos y dentro de límites sensatos, incluso cuando la aleatoriedad es intensa. Los autores prueban que este esquema permanece estable para cualquier tamaño de paso temporal y luego lo comparan con métodos ampliamente usados como Euler–Maruyama y Runge–Kutta estocástico. En experimentos numéricos cara a cara, los métodos convencionales funcionan solo con pasos muy pequeños; cuando el tamaño del paso crece, generan oscilaciones irreales e incluso poblaciones negativas. El nuevo esquema continúa siguiendo suavemente el curso esperado de la infección, coincidiendo con los equilibrios teóricos del modelo.
Qué significa esto para entender el VRS
Para los no especialistas, el mensaje clave es que la forma en que simulamos una epidemia puede ser tan importante como las propias ecuaciones. Este trabajo ofrece un modelo detallado de VRS que captura tanto los retardos como la aleatoriedad, y un método computacional asociado que mantiene las predicciones con sentido físico bajo una amplia gama de condiciones. Tal herramienta puede ayudar a investigadores y responsables de políticas a explorar escenarios «qué pasaría si» —como cambiar los patrones de contacto o dirigir intervenciones a los supercontagiadores— sin preocuparse de que fallos numéricos estén impulsando los resultados. A la larga, enfoques como este podrían apoyar una planificación más fiable de campañas de vacunación contra el VRS y otras intervenciones destinadas a mantener bajo control los picos estacionales.
Cita: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Palabras clave: virus respiratorio sincitial, modelado epidémico, dinámica estocástica, simulación numérica, transmisión de enfermedades