Clear Sky Science · pl
Analiza matematyczna stochastycznego modelu z opóźnieniem dla dynamiki wirusa syncytialnego układu oddechowego
Dlaczego to badanie ma znaczenie dla codziennego zdrowia
Wirus syncytialny układu oddechowego (RSV) jest najbardziej znany z zapełniania oddziałów pediatrycznych każdej zimy, ale ten sam wirus zagraża też osobom starszym i tym z osłabionym układem odpornościowym. Służby zdrowia potrzebują wiarygodnych prognoz, jak RSV rozprzestrzenia się w społeczności i jak środki kontrolne mogą zmienić jego przebieg. Artykuł porusza subtelny problem leżący u podstaw tych prognoz: większość modeli matematycznych pomija losowość i opóźnienia w przebiegu zakażenia, co może sprawić, że przewidywania komputerowe będą mylące właśnie wtedy, gdy są najbardziej potrzebne. Autorzy budują bardziej realistyczny model rozprzestrzeniania się RSV i, co kluczowe, bezpieczniejszy sposób jego symulacji komputerowej, dzięki czemu prognozy pozostają wiarygodne nawet przy niepewnych warunkach.

Rozbicie epidemii na proste grupy
Badanie rozpoczyna się od podziału populacji na pięć grup: osoby podatne na zakażenie RSV, osoby narażone, ale jeszcze niezakaźne, osoby z typowym zakażeniem, osoby rozprzestrzeniające wirusa znacznie bardziej niż przeciętnie (super-roznosiciele) oraz osoby wyzdrowiałe. Model uwzględnia także okres oczekiwania między momentem zakażenia a chwilą, gdy dana osoba zaczyna przekazywać wirusa. W trakcie tego opóźnienia ludzie mogą nadal umrzeć z innych przyczyn, więc autorzy biorą pod uwagę prawdopodobieństwo, że osoba zakażona po prostu nie dożyje momentu stania się zakaźną. Z tymi elementami formułują zestaw równań opisujących, jak jednostki przechodzą między grupami w czasie i wykazują, że całkowita populacja pozostaje w realistycznych granicach i nigdy nie przyjmuje wartości ujemnych — podstawowa, lecz niezbędna weryfikacja każdego modelu choroby.
Wyznaczanie punktu krytycznego epidemii
Wykorzystując ramy modelu z opóźnieniem, badacze obliczają „podstawową liczbę reprodukcji”, próg mówiący, czy RSV zaniknie, czy będzie się utrzymywać. Ta liczba łączy w sobie to, jak szybko ludzie się stykają, jak długo pozostają zakaźni, jak prawdopodobne jest wystąpienie super-roznosicieli oraz jak długo żyją. Jeśli liczba reprodukcji jest mniejsza niż jeden, infekcje w końcu zanikają; jeśli jest większa niż jeden, wirus osiada na stałym poziomie. Zespół udowadnia matematycznie, że ich model zachowuje się dokładnie w ten sposób: jedno równowagi odpowiada społeczności wolnej od RSV, druga — trwałemu, ale stabilnemu poziomowi zakażeń. Pokazują też, że te wyniki pozostają stabilne nawet gdy opóźnienie i inne parametry zmieniają się w rozsądnych granicach.
Wskazywanie, co ma największe znaczenie dla kontroli
Ponieważ wiele danych wejściowych modelu jest niepewnych, autorzy sprawdzają, jak czuła jest liczba reprodukcji na każdy z nich. Stwierdzają, że czynniki zwiększające tempo nowych zakażeń — takie jak częstotliwość kontaktów międzyludzkich czy szybkość, z jaką osoby narażone stają się zakaźne — przesuwają system ku większym wybuchom epidemii. Z kolei czynniki skracające okres zakaźności lub zwiększające naturalne wskaźniki zgonów obniżają liczbę reprodukcji. Takie uporządkowanie wrażliwości pomaga planistom zdrowia publicznego zobaczyć, które dźwignie są najskuteczniejsze: na przykład strategie skutecznie skracające czas infekcyjności lub ograniczające możliwości super-roznoszenia mogą mieć nieproporcjonalnie duży wpływ na transmisję RSV.
Dodanie losowości i bezpieczniejsze symulacje komputerowe
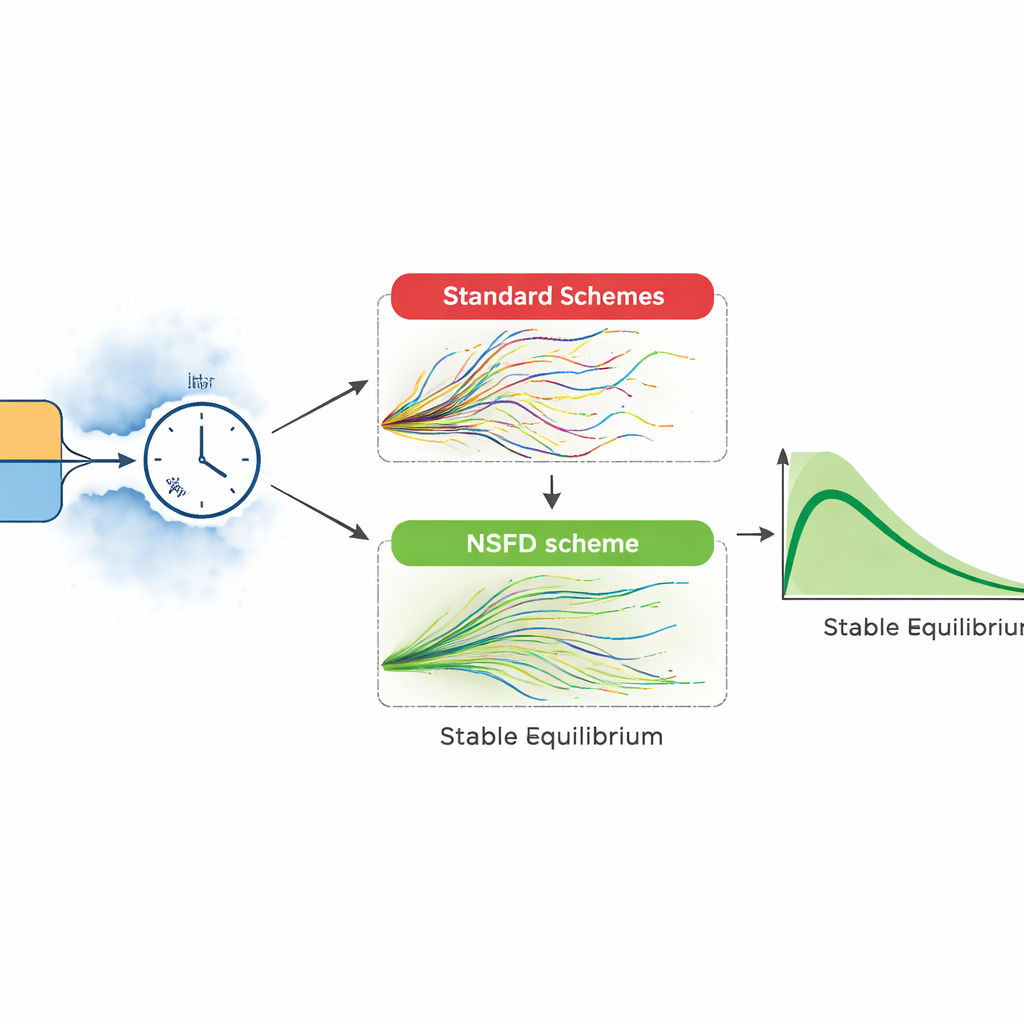
Prawdziwe epidemie nie toczą się jako gładkie krzywe. Dlatego autorzy rozszerzają swój model o losowe fluktuacje środowiskowe i niepewność w kluczowych procesach, takich jak transmisja i wyzdrowienie. Konstruują dwie wersje stochastyczne: jedną opartą na szczegółowej liście możliwych zdarzeń (jak zakażenie lub wyzdrowienie zachodzące w krótkim oknie czasowym) i drugą, która zakłóca każdą grupę przy pomocy losowego szumu. Te bogatsze modele lepiej odzwierciedlają nieregularne wybuchy i niespodziewane napływy przypadków. Jednak standardowe metody komputerowe używane do rozwiązywania takich modeli mogą zachowywać się nieprawidłowo: przy dużych krokach czasowych mogą dawać ujemne liczby pacjentów lub eksplodujące wahania bez sensu biologicznego.
Nowe, odporne narzędzie numeryczne
Aby przezwyciężyć te problemy, artykuł wprowadza stochastyczną schemat „niestandardowych różnic skończonych” zaprojektowany tak, by respektować biologię problemu. W tym podejściu dryf, czyli średni ruch systemu, jest traktowany ostrożnie, tak aby symulowane liczby osób podatnych, zakażonych i wyzdrowiałych zawsze pozostawały nieujemne i w rozsądnych granicach, nawet gdy losowość jest silna. Autorzy dowodzą, że ten schemat pozostaje stabilny dla dowolnego rozmiaru kroku czasowego, a następnie testują go przeciwko powszechnie stosowanym metodom, takim jak Euler–Maruyama i stochastyczny Runge–Kutta. W bezpośrednich eksperymentach numerycznych metody konwencjonalne działają tylko dla bardzo małych kroków; gdy krok rośnie, generują nierealistyczne oscylacje, a nawet ujemne populacje. Nowy schemat nadal gładko odwzorowuje oczekiwany przebieg zakażeń, odpowiadając teoretycznym punktom równowagi modelu.
Co to oznacza dla zrozumienia RSV
Dla osób niezwiązanych z tematem kluczowe przesłanie jest takie, że sposób, w jaki symulujemy epidemię, może być równie ważny jak same równania. Praca dostarcza szczegółowy model RSV, który uwzględnia zarówno opóźnienia, jak i losowość, oraz towarzyszącą mu metodę obliczeniową, która utrzymuje prognozy w sensownych ramach fizycznych w szerokim zakresie warunków. Takie narzędzie może pomóc badaczom i decydentom badać scenariusze „co jeśli” — jak zmiana wzorców kontaktów czy ukierunkowanie na super-roznosicieli — bez obaw, że to błędy numeryczne sterują wynikami. W długiej perspektywie podejścia tego rodzaju mogą wspierać bardziej wiarygodne planowanie kampanii szczepień przeciw RSV i innych interwencji mających na celu ograniczenie sezonowych skoków zachorowań.
Cytowanie: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Słowa kluczowe: wirus syncytialny układu oddechowego, modelowanie epidemii, dynamika stochastyczna, symulacja numeryczna, transmisja chorób