Clear Sky Science · it
Analisi matematica di un modello stocastico con ritardo per la dinamica del virus respiratorio sinciziale
Perché questo studio conta per la salute quotidiana
Il virus respiratorio sinciziale (RSV) è noto soprattutto per riempire i reparti pediatrici ogni inverno, ma lo stesso virus rappresenta una minaccia anche per gli anziani e le persone con sistemi immunitari compromessi. Le agenzie sanitarie necessitano di previsioni affidabili su come l’RSV si diffonde in una comunità e su come le misure di controllo potrebbero modificarne l’andamento. Questo articolo affronta un problema sottile alla base di quelle previsioni: la maggior parte dei modelli matematici ignora la casualità e i ritardi nel manifestarsi dell’infezione, elementi che possono rendere le previsioni al computer fuorvianti proprio quando sono più necessarie. Gli autori costruiscono un modello più realistico della diffusione dell’RSV e, cosa cruciale, un modo più sicuro di simularlo al computer affinché le previsioni rimangano attendibili anche in condizioni di incertezza.

Dividere l’epidemia in gruppi semplici
Lo studio parte suddividendo la popolazione in cinque gruppi: persone suscettibili all’RSV, persone esposte ma non ancora contagiose, persone con infezioni ordinarie, super-diffusori che trasmettono il virus molto più della media, e persone guarite. Il modello incorpora inoltre un periodo di attesa tra il momento dell’infezione e il momento in cui un individuo inizia a diffondere il virus. Durante questo ritardo, le persone possono comunque morire per altre cause, quindi gli autori tengono conto della possibilità che un infetto non viva abbastanza a lungo da diventare contagioso. Con questi elementi, formulano un sistema di equazioni che descrive come le persone si spostano fra i gruppi nel tempo e mostrano che la popolazione totale rimane entro limiti realistici e non diventa mai negativa — un controllo basilare ma essenziale per qualsiasi modello di malattia.
Individuare il punto di svolta di un’epidemia
Usando il loro quadro con ritardo, i ricercatori calcolano il “numero di riproduzione di base”, una soglia che indica se l’RSV si estinguerà o continuerà a circolare. Questo numero combina quanto velocemente le persone entrano in contatto, quanto a lungo rimangono contagiose, la probabilità di diventare super-diffusori e l’aspettativa di vita. Se il numero di riproduzione è inferiore a uno, le infezioni scompaiono nel tempo; se è superiore a uno, il virus si stabilizza in una presenza continua. Il gruppo dimostra matematicamente che il loro modello si comporta esattamente in questo modo: un equilibrio corrisponde a una comunità libera dall’RSV, l’altro a un livello di infezione persistente ma stabile. Mostrano inoltre che questi esiti rimangono stabili anche quando il ritardo e altri parametri variano entro intervalli ragionevoli.
Capire cosa conta di più per il controllo
Poiché molte variabili del modello sono incerte, gli autori verificano quanto il numero di riproduzione sia sensibile a ciascuna di esse. Risultano cruciali i fattori che aumentano il tasso di nuove infezioni — come la frequenza dei contatti o la rapidità con cui gli esposti diventano infettivi — che spingono il sistema verso focolai più ampi. Al contrario, fattori che riducono il periodo infettivo o aumentano i tassi di mortalità naturale abbassano il numero di riproduzione. Questo tipo di graduatoria di sensibilità aiuta i pianificatori della sanità pubblica a vedere quali leve sono più potenti: ad esempio, strategie che accorciano efficacemente il tempo di contagiosità o riducono le opportunità di super-diffusione possono avere un impatto sproporzionato sulla trasmissione dell’RSV.
Aggiungere casualità e simulazioni al sicuro
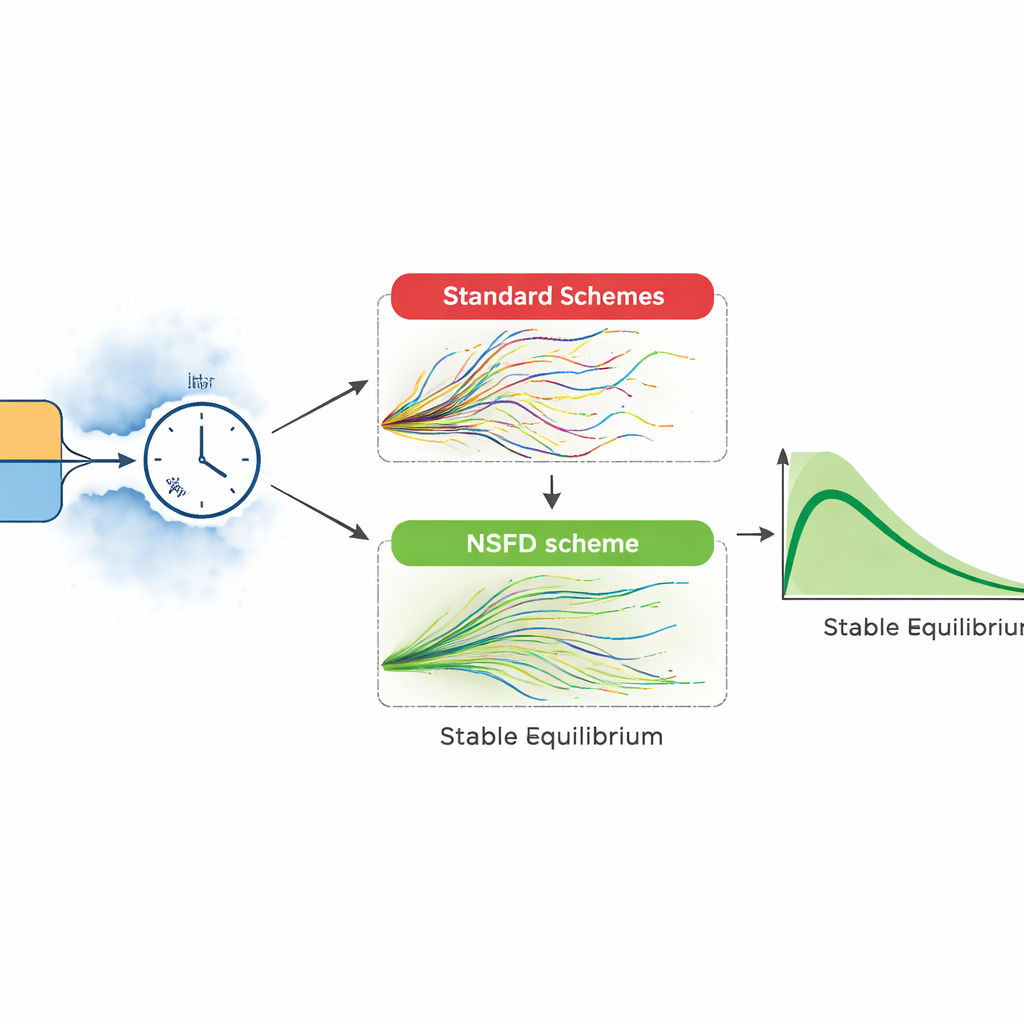
Le epidemie reali non si svolgono come curve lisce. Gli autori estendono quindi il loro modello includendo fluttuazioni ambientali casuali e incertezze nei processi chiave, come trasmissione e guarigione. Costruiscono due versioni stocastiche: una basata su un elenco dettagliato di eventi possibili (ad esempio un’infezione o una guarigione che avvengono in una breve finestra temporale) e un’altra che perturba ciascun gruppo con rumore casuale. Questi modelli più ricchi riflettono meglio focolai irregolari e picchi inattesi. Tuttavia, i metodi numerici standard usati per risolvere tali modelli possono comportarsi male: per passi temporali grandi possono produrre numeri negativi di pazienti o oscillazioni esplosive prive di significato biologico.
Un nuovo strumento numerico robusto
Per superare questi problemi, l’articolo introduce uno schema stocastico a «differenze finite non standard» progettato per rispettare la biologia del problema. In questo approccio la deriva, o il moto medio del sistema, è trattata con cura in modo che i numeri simulati di suscettibili, infetti e guariti rimangano sempre non negativi e entro limiti sensati, anche quando la casualità è intensa. Gli autori dimostrano che questo schema resta stabile per qualsiasi dimensione del passo temporale, poi lo confrontano con metodi ampiamente usati come Euler–Maruyama e Runge–Kutta stocastico. In esperimenti numerici diretti, i metodi convenzionali funzionano solo per passi molto piccoli; quando il passo cresce generano oscillazioni irrealistiche e perfino popolazioni negative. Il nuovo schema continua invece a seguire l’andamento atteso dell’infezione in modo regolare, corrispondendo agli equilibri teorici del modello.
Cosa significa per comprendere l’RSV
Per i non specialisti, il messaggio chiave è che il modo in cui simuliamo un’epidemia può essere importante quanto le equazioni stesse. Questo lavoro fornisce un modello dettagliato dell’RSV che cattura sia i ritardi sia la casualità, e un metodo computazionale che mantiene le previsioni fisicamente sensate in un ampio insieme di condizioni. Tale strumento può aiutare ricercatori e decisori a esplorare scenari «what‑if» — come modifiche nei modelli di contatto o interventi mirati ai super-diffusori — senza temere che artefatti numerici guidino i risultati. A lungo termine, approcci di questo tipo potrebbero sostenere una pianificazione più affidabile per campagne vaccinali contro l’RSV e altre misure volte a contenere i picchi stagionali.
Citazione: Raza, A., Lampart, M., Shafique, U. et al. Mathematical analysis of a stochastic delay model for respiratory syncytial virus dynamics. Sci Rep 16, 10022 (2026). https://doi.org/10.1038/s41598-026-39783-y
Parole chiave: virus respiratorio sinciziale, modellizzazione epidemica, dinamiche stocastiche, simulazione numerica, trasmissione della malattia