Clear Sky Science · pt
O metabolismo da riboflavina molda a resistência à ferroptose mediada por FSP1
Por que essa história da vitamina importa
A maioria das pessoas conhece as vitaminas como algo a ser tomado pela manhã para a saúde em geral. Este estudo mostra que uma vitamina familiar, a riboflavina (vitamina B2), pode desempenhar um papel bem mais dramático dentro de nossas células: ela ajuda a decidir se células sob estresse vivem ou morrem por meio de uma forma de dano dependente de ferro chamada ferroptose. Como a ferroptose está ligada ao câncer, à neurodegeneração e a ataques cardíacos, descobrir como um nutriente comum ajusta esse processo pode, em última instância, influenciar como projetamos dietas e medicamentos para essas doenças.
Um escudo frágil ao redor de nossas células
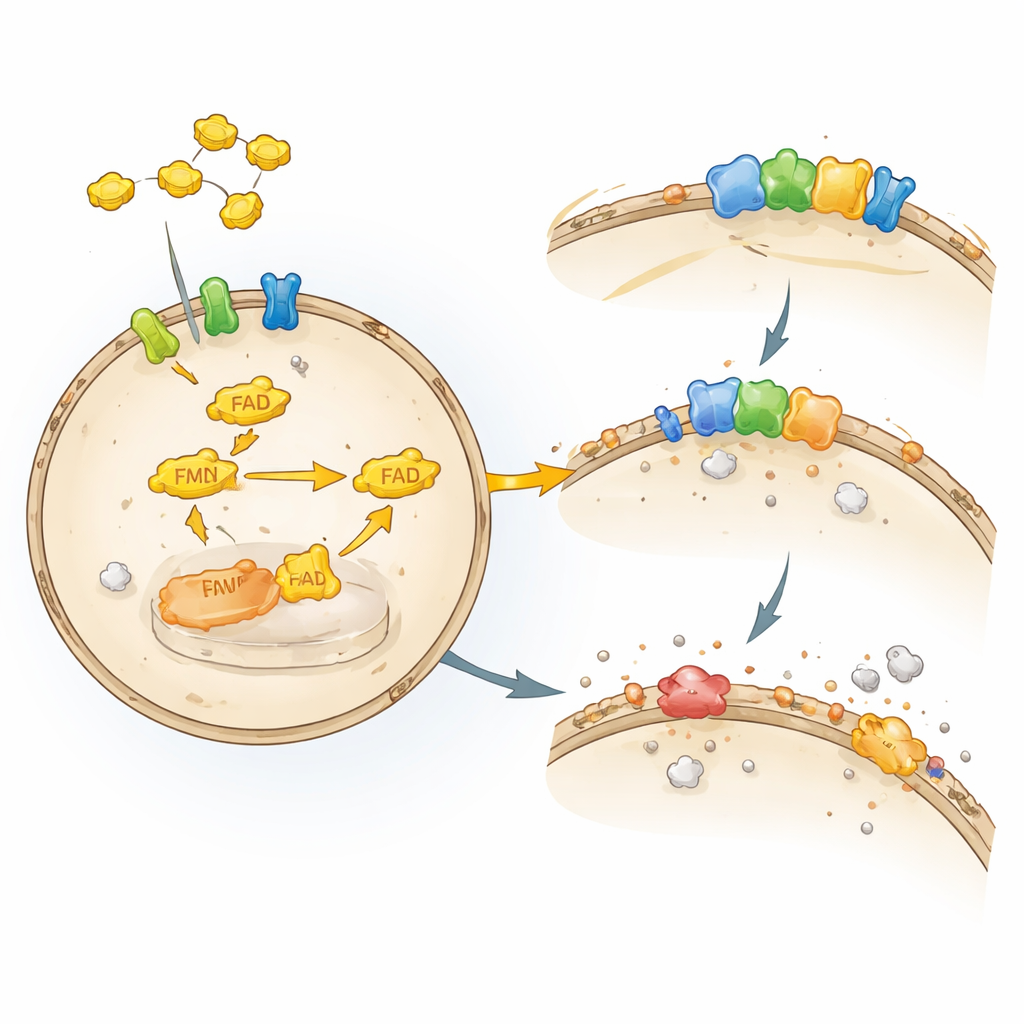
Cada célula é envolvida por uma membrana fina e gordurosa que funciona como uma combinação de muro e régua de energia. Essa camada lipídica é facilmente danificada por certas formas de oxigênio, em um processo conhecido como peroxidação lipídica. Quando esse dano sai do controle, as células passam por ferroptose, uma forma regulada de morte celular que depende de ferro e de lipídios oxidados. Nossas células empregam vários sistemas de defesa para interromper essa cascata. Um guardião-chave, a enzima GPX4, usa o antioxidante glutationa para desintoxicar peróxidos lipídicos nocivos. Outro guardião, o FSP1, fica na membrana e mantém antioxidantes solúveis em gordura, como a coenzima Q e a vitamina K, em sua forma ativa e protetora, atuando como uma estação de reciclagem para essas moléculas.
Encontrando os auxiliares ocultos de um guardião celular
Embora se soubesse que o FSP1 era um forte freio à ferroptose, os pesquisadores não sabiam quais fatores celulares o mantinham em funcionamento. Os autores engenheiraram células humanas de câncer para que dependessem inteiramente do FSP1 para sobreviver quando a GPX4 fosse desativada. Em seguida, usaram uma triagem focalizada com CRISPR–Cas9, eliminando cerca de 3.000 genes relevantes para fármacos para ver quais perdas tornavam as células subitamente vulneráveis. Entre os resultados mais contundentes estavam enzimas e transportadores envolvidos no manejo da riboflavina, especialmente a riboflavina quinase (RFK) e a flavina adenina dinucleotídeo sintase (FADS), que constroem o cofator FAD a partir da riboflavina. Quando esses genes eram perturbados, os níveis de proteína FSP1 caíam, o dano lipídico aumentava e as células morriam por ferroptose, revelando uma dependência direta e a montante do FSP1 por cofatores derivados da riboflavina.
O suprimento de vitamina como um botão de ajuste para a sobrevivência celular
Para testar se o próprio nutriente, e não apenas as enzimas, importava, a equipe cultivou células em meio sem riboflavina ou contendo quantidades mais próximas às do sangue humano, que são muito mais baixas que as soluções padrão de laboratório. Em condições pobres em riboflavina, muitas proteínas dependentes de flavina diminuíram, mas o FSP1 foi um dos mais fortemente depletados, sem uma queda semelhante em seu RNA mensageiro. As células tornaram-se muito mais sensíveis a compostos que bloqueiam a GPX4, e suas membranas acumularam fosfolipídios oxidados, uma marca registrada da ferroptose. Importante: simplesmente restaurar a riboflavina recuperou a proteína FSP1 e reduziu o dano lipídico. Mesmo mudanças modestas na riboflavina dentro de uma faixa fisiológica ajustaram quanto de proteção do FSP1 as células podiam reunir, sugerindo que variações cotidianas no estado de vitamina B2 podem influenciar silenciosamente como os tecidos lidam com o estresse oxidativo.
Virando uma vitamina útil contra o câncer
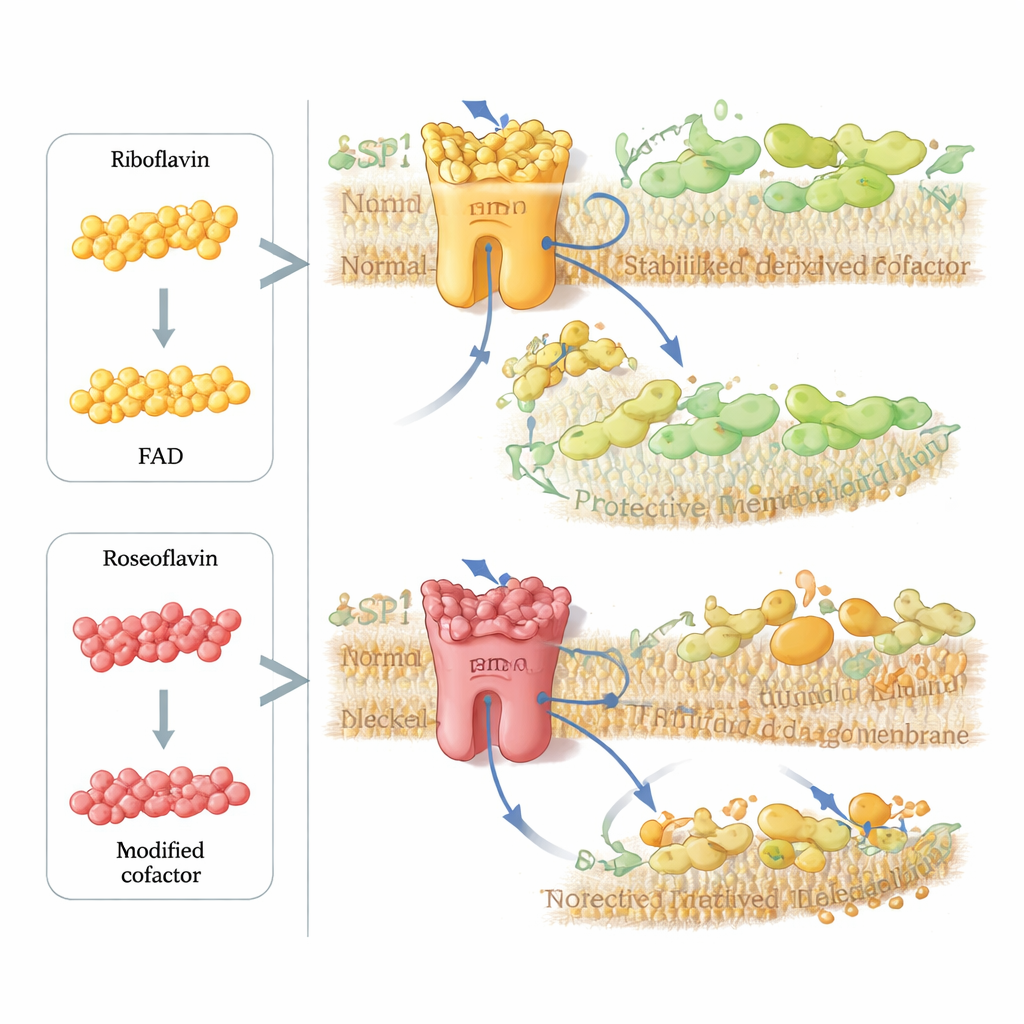
Os pesquisadores então perguntaram se poderiam deliberadamente sabotar essa via protetora em células cancerígenas. Eles recorreram à roseoflavina, um antibiótico natural produzido por certas bactérias que se assemelha muito à riboflavina, mas com uma pequena alteração química. As células absorvem a roseoflavina e a convertem em uma versão modificada do FAD que pode encaixar-se no FSP1 e estabilizar a estrutura da enzima, mas não consegue transportar elétrons adequadamente. Em testes com enzimas purificadas e simulações computacionais, o FSP1 carregado com o cofator da roseoflavina era essencialmente impotente. Em várias linhagens de células cancerígenas, doses minúsculas, na faixa de nanomolar, de roseoflavina aumentaram fortemente o poder de morte de inibidores da GPX4, mas apenas quando o FSP1 estava presente, mostrando que o composto paralisa especificamente esse circuito de reparo da membrana.
O que isso significa para saúde e terapia
Em conjunto, o trabalho redesenha a riboflavina de um nutriente simples para um regulador mestre de um interruptor crítico de morte celular. Ao alimentar o cofator FAD, a riboflavina controla a estabilidade e a atividade do FSP1, que por sua vez governa quão eficazmente as células reciclam antioxidantes solúveis em lipídios e resistem ao dano da membrana. Riboflavina insuficiente enfraquece esse escudo e promove a ferroptose; análogos inteligentemente projetados, como a roseoflavina, podem sequestrar a mesma via para desabilitar o FSP1 sob demanda. Para leigos, a conclusão é que micronutrientes fazem mais do que “apoiar o metabolismo” — eles podem determinar de forma decisiva se as células sobrevivem ao estresse oxidativo. Essa percepção abre novas vias para sensibilizar tumores à terapia, refinar estratégias antioxidantes e compreender melhor como a dieta pode influenciar doenças nas quais a ferroptose desempenha um papel central.
Citação: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Palavras-chave: ferroptose, riboflavina, FSP1, peroxidação lipídica, terapia contra o câncer