Clear Sky Science · de
Riboflavin-Stoffwechsel prägt die FSP1-vermittelte Ferroptose‑Resistenz
Warum diese Vitamin‑Geschichte wichtig ist
Viele Menschen kennen Vitamine als etwas, das man morgens für die allgemeine Gesundheit einnimmt. Diese Studie zeigt, dass ein vertrautes Vitamin, Riboflavin (Vitamin B2), innerhalb unserer Zellen etwas weit Dramatischeres bewirken kann: Es hilft mitzuentscheiden, ob belastete Zellen durch eine Form eisenabhängiger Schäden, die Ferroptose genannt wird, überleben oder sterben. Da Ferroptose mit Krebs, Neurodegeneration und Herzinfarkt verknüpft ist, könnte das Aufdecken, wie ein verbreiteter Nährstoff diesen Prozess steuert, langfristig beeinflussen, wie wir Ernährung und Medikamente für diese Erkrankungen gestalten.
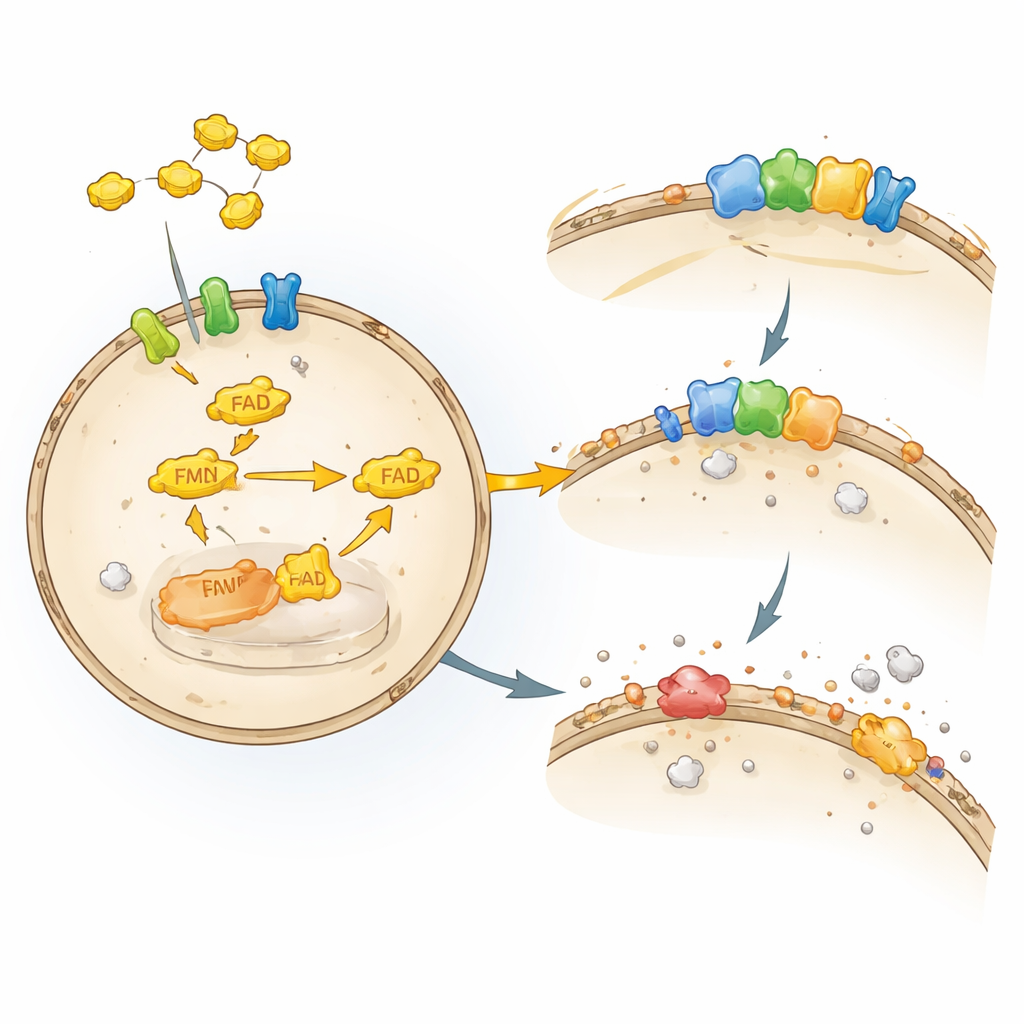
Ein fragiles Schutzschild um unsere Zellen
Jede Zelle ist von einer dünnen Fettschicht umgeben, die wie eine Kombination aus Mauer und Steckleiste funktioniert. Diese Fettschicht lässt sich leicht durch bestimmte Formen von Sauerstoff schädigen, in einem Prozess, der als Lipidperoxidation bekannt ist. Wenn diese Schäden außer Kontrolle geraten, durchlaufen Zellen Ferroptose, eine regulierte Form des Zelltods, die von Eisen und oxidierten Fetten abhängt. Unsere Zellen setzen mehrere Abwehrsysteme ein, um diese Kaskade zu stoppen. Ein wichtiger Wächter, das Enzym GPX4, nutzt das Antioxidans Glutathion, um schädliche Lipidperoxide zu entgiften. Ein anderer Wächter, FSP1, sitzt an der Membran und hält fettlösliche Antioxidantien wie Coenzym Q und Vitamin K in ihrer aktiven, schützenden Form — er fungiert wie eine Recyclingstation für diese Moleküle.
Die versteckten Helfer eines Zellwächters finden
Obwohl FSP1 als starker Bremsmechanismus gegen Ferroptose bekannt war, wussten die Forscher nicht, welche zellulären Faktoren es am Laufen hielten. Die Autoren konstruierten menschliche Krebszellen so, dass sie vollständig auf FSP1 angewiesen waren, um zu überleben, wenn GPX4 ausgeschaltet wurde. Dann nutzten sie ein fokussiertes CRISPR–Cas9‑Geneditierungs‑Screening und schalteten etwa 3.000 für Medikamente relevante Gene aus, um zu sehen, welche Verluste die Zellen plötzlich verwundbar machten. Zu den stärksten Treffern gehörten Enzyme und Transporter, die mit der Verarbeitung von Riboflavin zu tun haben, insbesondere Riboflavinkinase (RFK) und Flavin‑Adenin‑Dinukleotid‑Synthase (FADS), die das Cofaktor FAD aus Riboflavin aufbauen. Wenn diese Gene gestört waren, sanken die FSP1‑Proteinspiegel, die Lipidschäden stiegen und die Zellen starben durch Ferroptose — das zeigt eine direkte, vorgelagerte Abhängigkeit von FSP1 von Riboflavin‑abgeleiteten Cofaktoren.
Vitaminversorgung als Regler für das Zellüberleben
Um zu testen, ob der Nährstoff selbst und nicht nur die Enzyme eine Rolle spielt, kultivierte das Team Zellen in Medien ohne Riboflavin oder mit Konzentrationen, die näher am menschlichen Blut liegen, das deutlich niedrigere Werte aufweist als übliche Laborlösungen. Unter riboflavinarmer Versorgung nahmen viele flavinabhängige Proteine ab, doch FSP1 gehörte zu den am stärksten verringerten, ohne dass dessen Boten‑RNA in ähnlichem Maße zurückging. Die Zellen wurden deutlich empfindlicher gegenüber Verbindungen, die GPX4 blockieren, und ihre Membranen sammelten oxidierte Phospholipide an — ein Kennzeichen der Ferroptose. Wichtig war, dass allein die Wiederzufuhr von Riboflavin das FSP1‑Protein wiederherstellte und die Lipidschäden verringerte. Bereits moderate Schwankungen des Riboflavinspiegels im physiologischen Bereich konnten beeinflussen, wie viel Schutz FSP1 die Zellen leisten konnte, was darauf hindeutet, dass alltägliche Veränderungen im Vitamin‑B2‑Status stillschweigend beeinflussen könnten, wie Gewebe mit oxidativem Stress umgehen.
Ein hilfreiches Vitamin gegen Krebs wenden
Die Forscher fragten dann, ob sie diesen Schutzweg gezielt in Krebszellen sabotieren könnten. Sie untersuchten Roseoflavin, ein natürliches Antibiotikum bestimmter Bakterien, das Riboflavin sehr ähnlich ist, aber eine kleine chemische Veränderung trägt. Zellen nehmen Roseoflavin auf und wandeln es in eine modifizierte Form von FAD um, die in FSP1 passt und das Protein stabilisieren kann, aber Elektronen nicht richtig transportieren kann. In gereinigten Enzymtests und Computersimulationen war FSP1, das mit dem Cofaktor von Roseoflavin beladen war, faktisch kraftlos. In mehreren Krebszelllinien verstärkten winzige, nanomolare Dosen Roseoflavin die Wirkung von GPX4‑Inhibitoren deutlich — jedoch nur, wenn FSP1 vorhanden war, was zeigt, dass das Mittel gezielt diesen Membranschadens‑Reparaturkreislauf lahmlegt.
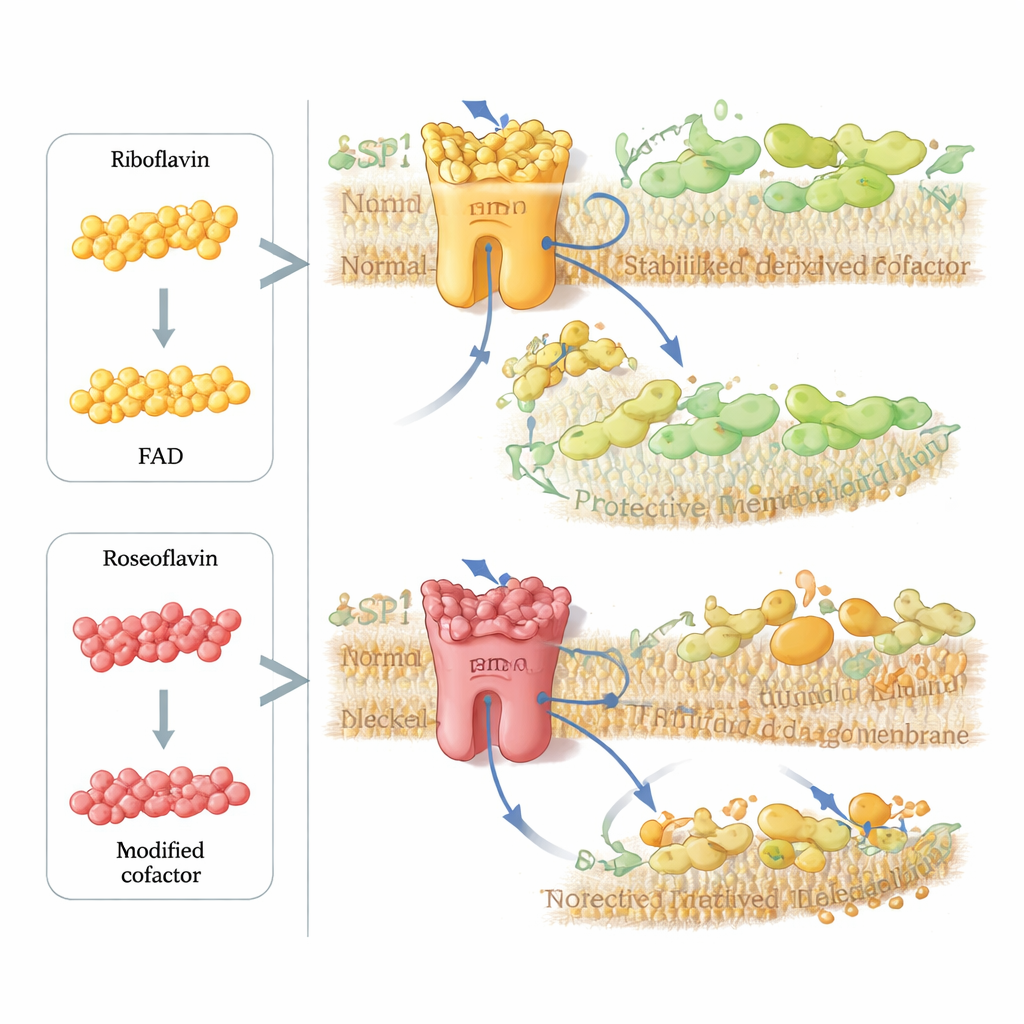
Was das für Gesundheit und Therapie bedeutet
In der Summe verwandelt die Arbeit Riboflavin von einem einfachen Nährstoff in einen zentralen Regulator eines kritischen Zell‑Tods‑Schalters. Indem es in das FAD‑Cofaktor‑System einspeist, steuert Riboflavin Stabilität und Aktivität von FSP1, das wiederum bestimmt, wie effektiv Zellen fettlösliche Antioxidantien recyclen und Membranschäden widerstehen. Zu wenig Riboflavin schwächt dieses Schutzschild und fördert Ferroptose; geschickt gestaltete Analoga wie Roseoflavin können denselben Weg kapern, um FSP1 bei Bedarf außer Gefecht zu setzen. Für Laien lautet die Schlussfolgerung, dass Mikronährstoffe mehr tun als „den Stoffwechsel unterstützen“ — sie können festlegen, ob Zellen oxidativen Stress überleben. Diese Erkenntnis eröffnet neue Wege, Tumoren für Therapien empfänglicher zu machen, Antioxidantienstrategien zu verfeinern und besser zu verstehen, wie Ernährung Krankheiten beeinflussen könnte, bei denen Ferroptose eine zentrale Rolle spielt.
Zitation: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Schlüsselwörter: Ferroptose, Riboflavin, FSP1, Lipidperoxidation, Krebstherapie