Clear Sky Science · fr
Le métabolisme de la riboflavine façonne la résistance à la ferroptose pilotée par FSP1
Pourquoi cette histoire de vitamine importe
La plupart des gens connaissent les vitamines comme quelque chose que l’on prend le matin pour la santé générale. Cette étude montre qu’une vitamine familière, la riboflavine (vitamine B2), peut jouer un rôle beaucoup plus spectaculaire à l’intérieur de nos cellules : elle aide à décider si des cellules stressées vivent ou meurent par une forme de dommage liée au fer appelée ferroptose. Comme la ferroptose est liée au cancer, aux maladies neurodégénératives et aux infarctus, comprendre comment ce nutriment courant module ce processus pourrait à terme influencer la façon dont nous concevons les régimes et les médicaments pour ces maladies.
Un bouclier fragile autour de nos cellules
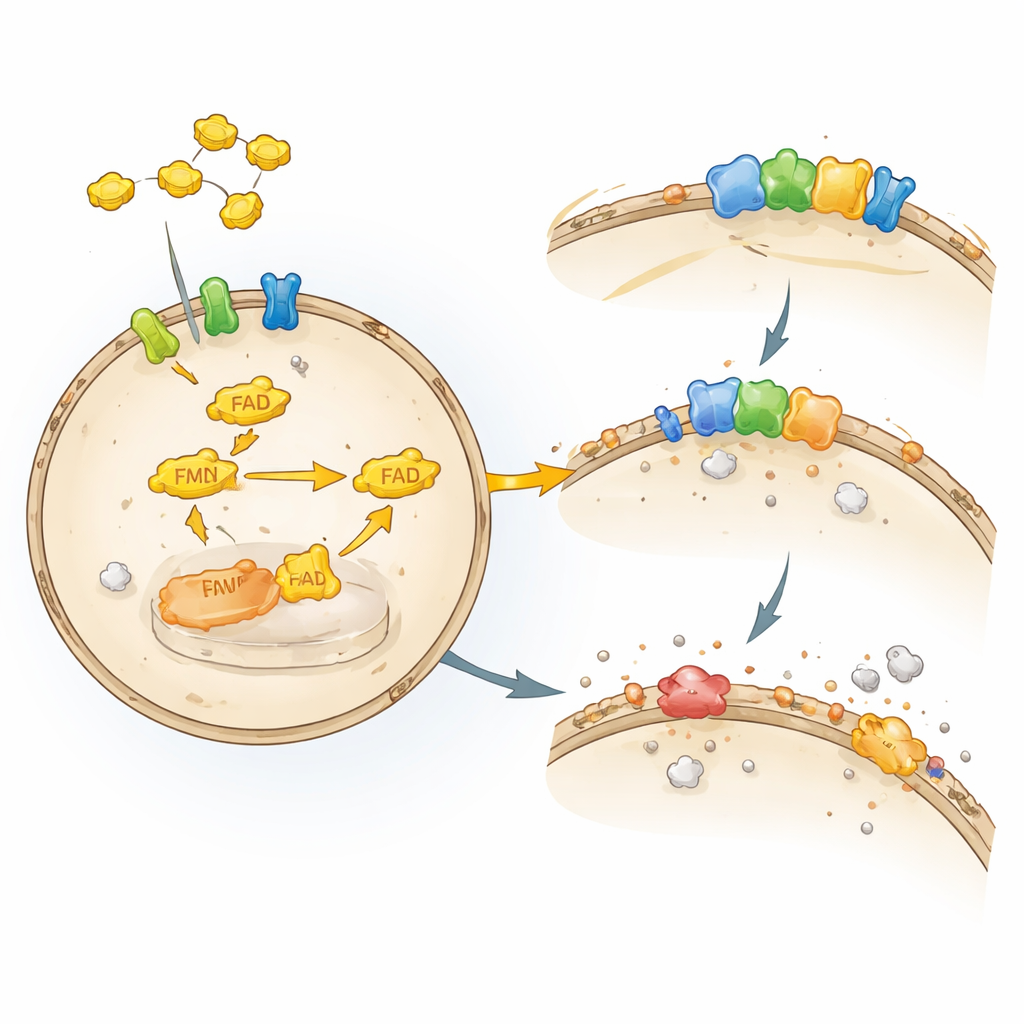
Chaque cellule est enveloppée d’une fine membrane lipidique qui fonctionne comme un mur et une multiprise à la fois. Cette couche graisseuse est facilement endommagée par certaines formes d’oxygène, dans un processus appelé peroxydation lipidique. Lorsque ces dommages deviennent incontrôlables, les cellules subissent la ferroptose, une forme régulée de mort cellulaire dépendant du fer et des lipides oxydés. Nos cellules déploient plusieurs systèmes de défense pour arrêter cette cascade. Un gardien clé, l’enzyme GPX4, utilise l’antioxydant glutathion pour détoxifier les peroxydes lipidiques nocifs. Un autre garde, FSP1, se place à la membrane et maintient les antioxydants liposolubles tels que la coenzyme Q et la vitamine K dans leur forme active et protectrice, agissant comme une station de recyclage pour ces molécules.
À la recherche des aides cachés d’un gardien cellulaire
Bien que FSP1 soit connu comme un puissant frein à la ferroptose, les chercheurs ne savaient pas quels facteurs cellulaires le maintenaient opérationnel. Les auteurs ont modifié des cellules cancéreuses humaines pour qu’elles dépendent entièrement de FSP1 pour survivre lorsque GPX4 était désactivé. Ils ont ensuite utilisé un criblage CRISPR–Cas9 ciblé, supprimant environ 3 000 gènes pertinents pour les médicaments afin de voir quelles pertes rendaient soudainement les cellules vulnérables. Parmi les résultats les plus marquants figuraient des enzymes et des transporteurs impliqués dans le traitement de la riboflavine, en particulier la riboflavine kinase (RFK) et la flavine adénine dinucléotide synthase (FADS), qui synthétisent le cofacteur FAD à partir de la riboflavine. Lorsque ces gènes étaient perturbés, les niveaux de protéine FSP1 diminuaient, les dommages lipidiques augmentaient et les cellules mouraient par ferroptose, révélant une dépendance en amont directe de FSP1 vis‑à‑vis des cofacteurs dérivés de la riboflavine.
L’apport en vitamine comme réglage du survie cellulaire
Pour tester si le nutriment lui‑même, et pas seulement les enzymes, avait de l’importance, l’équipe a cultivé des cellules dans des milieux dépourvus de riboflavine ou contenant des concentrations proches de celles du sang humain, bien plus faibles que dans les solutions de laboratoire standard. Dans des conditions pauvres en riboflavine, de nombreuses protéines dépendantes des flavines diminuaient, mais FSP1 faisait partie des plus fortement appauvries, sans baisse comparable de son ARN messager. Les cellules devenaient beaucoup plus sensibles aux composés qui bloquent GPX4, et leurs membranes accumulaient des phospholipides oxydés, une signature de la ferroptose. Fait important, la simple restauration de la riboflavine rétablissait la protéine FSP1 et réduisait les dégâts lipidiques. Même des variations modestes de riboflavine dans une plage physiologique ajustaient la protection fournie par FSP1, suggérant que des fluctuations quotidiennes du statut en vitamine B2 peuvent influencer discrètement la capacité des tissus à faire face au stress oxydatif.
Tourner une vitamine utile contre le cancer
Les chercheurs se sont ensuite demandé s’ils pouvaient délibérément saboter cette voie protectrice dans les cellules cancéreuses. Ils se sont intéressés à la roséoflavine, un antibiotique naturel produit par certaines bactéries qui ressemble beaucoup à la riboflavine mais présente une petite modification chimique. Les cellules incorporent la roséoflavine et la convertissent en une version modifiée du FAD qui peut s’insérer dans FSP1 et stabiliser la structure de l’enzyme, mais qui ne peut pas transporter correctement les électrons. Dans des essais avec l’enzyme purifiée et des simulations informatiques, FSP1 chargé du cofacteur dérivé de la roséoflavine était essentiellement impuissant. Dans plusieurs lignées cellulaires cancéreuses, des doses infimes, nanomolaires, de roséoflavine ont fortement amplifié le pouvoir létal des inhibiteurs de GPX4, mais seulement lorsque FSP1 était présent, montrant que le composé affaiblit spécifiquement ce circuit de réparation membranaire.
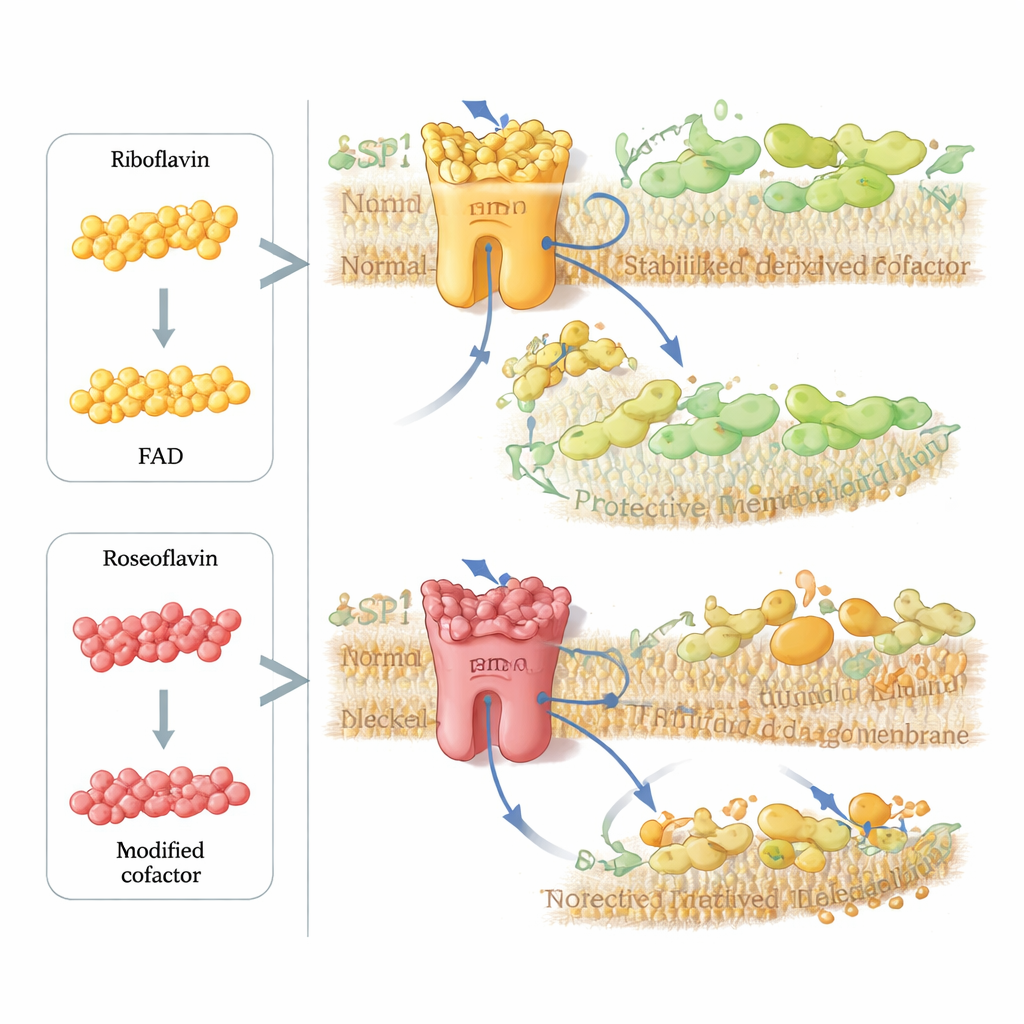
Ce que cela implique pour la santé et la thérapie
Ensemble, ces travaux requalifient la riboflavine d’un simple nutriment en régulateur maître d’un interrupteur critique de la mort cellulaire. En alimentant le cofacteur FAD, la riboflavine contrôle la stabilité et l’activité de FSP1, qui gouverne à son tour l’efficacité avec laquelle les cellules recyclent les antioxydants liposolubles et résistent aux dommages membranaires. Trop peu de riboflavine affaiblit ce bouclier et favorise la ferroptose ; des analogues astucieusement conçus comme la roséoflavine peuvent détourner la même voie pour désactiver FSP1 à la demande. Pour le grand public, la conclusion est que les micronutriments font plus que « soutenir le métabolisme » : ils peuvent déterminer de façon structurelle si les cellules survivent au stress oxydatif. Cette découverte ouvre de nouvelles voies pour sensibiliser les tumeurs aux traitements, affiner les stratégies antioxydantes et mieux comprendre comment l’alimentation peut influencer des maladies où la ferroptose joue un rôle central.
Citation: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Mots-clés: ferroptose, riboflavine, FSP1, peroxydation lipidique, thérapie contre le cancer