Clear Sky Science · pl
Metabolizm ryboflawiny kształtuje oporność na ferroptoza napędzaną przez FSP1
Dlaczego ta opowieść o witaminie ma znaczenie
Większość ludzi zna witaminy jako coś, co przyjmuje się rano dla ogólnego zdrowia. To badanie pokazuje, że jedna znana witamina, ryboflawina (witamina B2), może odgrywać znacznie bardziej dramatyczną rolę wewnątrz naszych komórek: pomaga decydować, czy komórki poddane stresowi przeżyją, czy umrą przez formę uszkodzenia zależną od żelaza zwaną ferroptozą. Ponieważ ferroptoza wiąże się z rakiem, neurodegeneracją i zawałami serca, odkrycie, jak powszechny składnik odżywczy reguluje ten proces, może w przyszłości wpływać na projektowanie diet i leków przeciw tym chorobom.
Krucha tarcza wokół naszych komórek
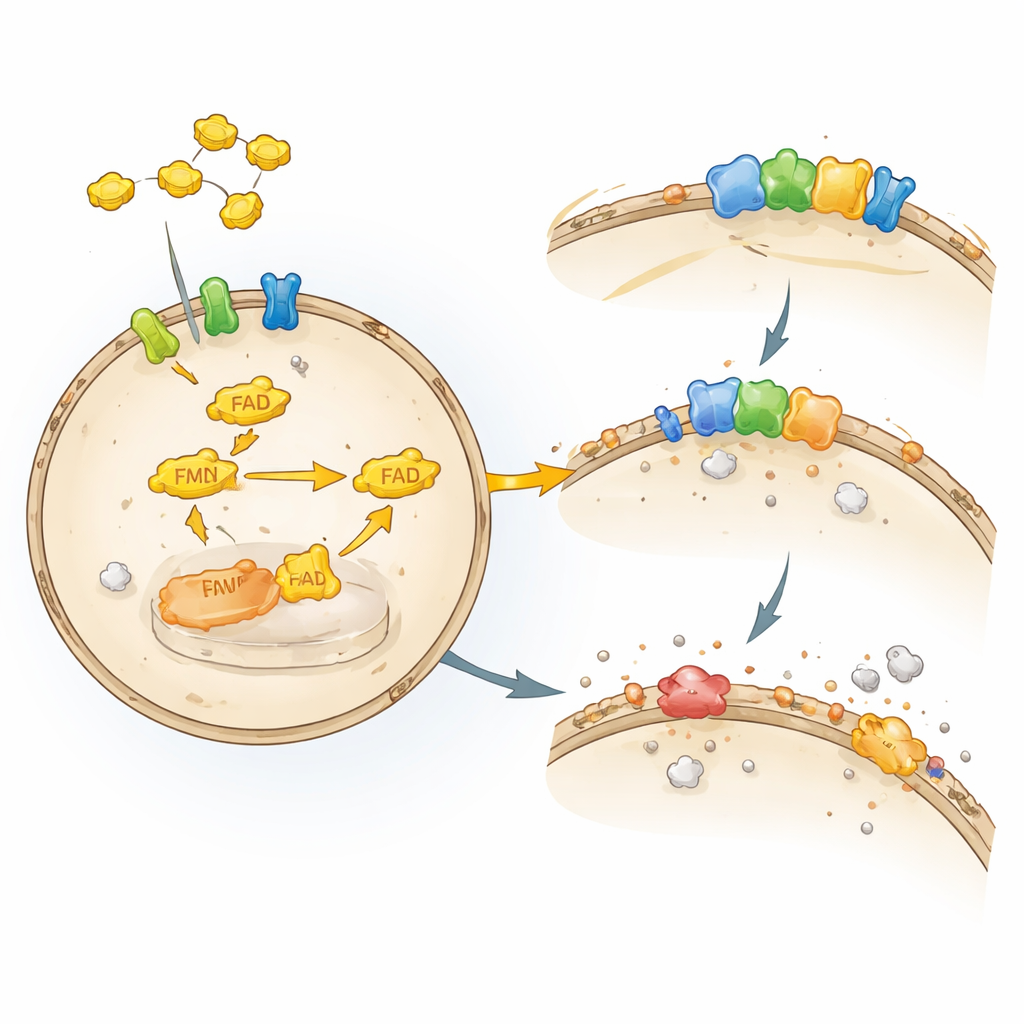
Każda komórka jest otoczona cienką lipidową błoną, która działa jak ściana i listwa zasilająca w jednym. Ta warstwa tłuszczowa jest łatwo uszkadzana przez pewne formy tlenu w procesie zwanym peroksydacją lipidów. Gdy to uszkodzenie wymyka się spod kontroli, komórki przechodzą ferroptozę — regulowaną formę śmierci komórkowej zależną od żelaza i utlenionych tłuszczów. Komórki dysponują kilkoma systemami obronnymi, aby powstrzymać tę kaskadę. Jednym z kluczowych strażników jest enzym GPX4, który wykorzystuje antyoksydant glutation do detoksykacji szkodliwych nadtlenków lipidowych. Innym opiekunem jest FSP1, umiejscowiony przy błonie, który utrzymuje rozpuszczalne w tłuszczach antyoksydanty, takie jak koenzym Q i witamina K, w ich aktywnej, ochronnej formie, działając jak stacja recyklingu dla tych cząsteczek.
Odkrywanie ukrytych pomocników strażnika komórkowego
Chociaż wiadomo było, że FSP1 stanowi silny hamulec ferroptozy, badacze nie wiedzieli, jakie czynniki komórkowe utrzymują jego działanie. Autorzy zaprojektowali ludzkie komórki nowotworowe tak, by do przeżycia przy wyłączonym GPX4 polegały całkowicie na FSP1. Następnie zastosowali ukierunkowany ekran CRISPR–Cas9, wyłączając około 3000 genów istotnych dla leków, aby zobaczyć, które straty nagle uczynią komórki wrażliwymi. Wśród najsilniejszych trafień znalazły się enzymy i transportery zaangażowane w przetwarzanie ryboflawiny, zwłaszcza kinaza ryboflawiny (RFK) i syntaza FMN/FAD (FADS), które budują kofaktor FAD z ryboflawiny. Gdy te geny zostały zaburzone, poziomy białka FSP1 spadły, uszkodzenia lipidów wzrosły, a komórki zginęły wskutek ferroptozy, ujawniając bezpośrednie zależności FSP1 od kofaktorów pochodzących z ryboflawiny.
Dostępność witaminy jako regulator przeżycia komórek
Aby sprawdzić, czy sam składnik odżywczy, a nie tylko enzymy, ma znaczenie, zespół hodował komórki w pożywce pozbawionej ryboflawiny lub zawierającej stężenia zbliżone do tych we krwi ludzkiej, które są znacznie niższe niż w standardowych roztworach laboratoryjnych. W warunkach ubogich w ryboflawinę wiele białek zależnych od flawin uległo zmniejszeniu, ale FSP1 znalazł się wśród najsilniej wyczerpanych, bez podobnego spadku jego mRNA. Komórki stały się znacznie bardziej wrażliwe na związki blokujące GPX4, a ich błony nagromadziły utlenione fosfolipidy — cechę charakterystyczną ferroptozy. Co ważne, proste przywrócenie ryboflawiny odtworzyło poziom białka FSP1 i zmniejszyło uszkodzenia lipidów. Nawet niewielkie zmiany w stężeniu ryboflawiny w zakresie fizjologicznym dostroiły, jak dużą ochronę FSP1 mogły zapewnić komórki, co sugeruje, że codzienne wahania statusu witaminy B2 mogą dyskretnie wpływać na to, jak tkanki radzą sobie ze stresem oksydacyjnym.
Wykorzystanie pomocnej witaminy przeciwko rakowi
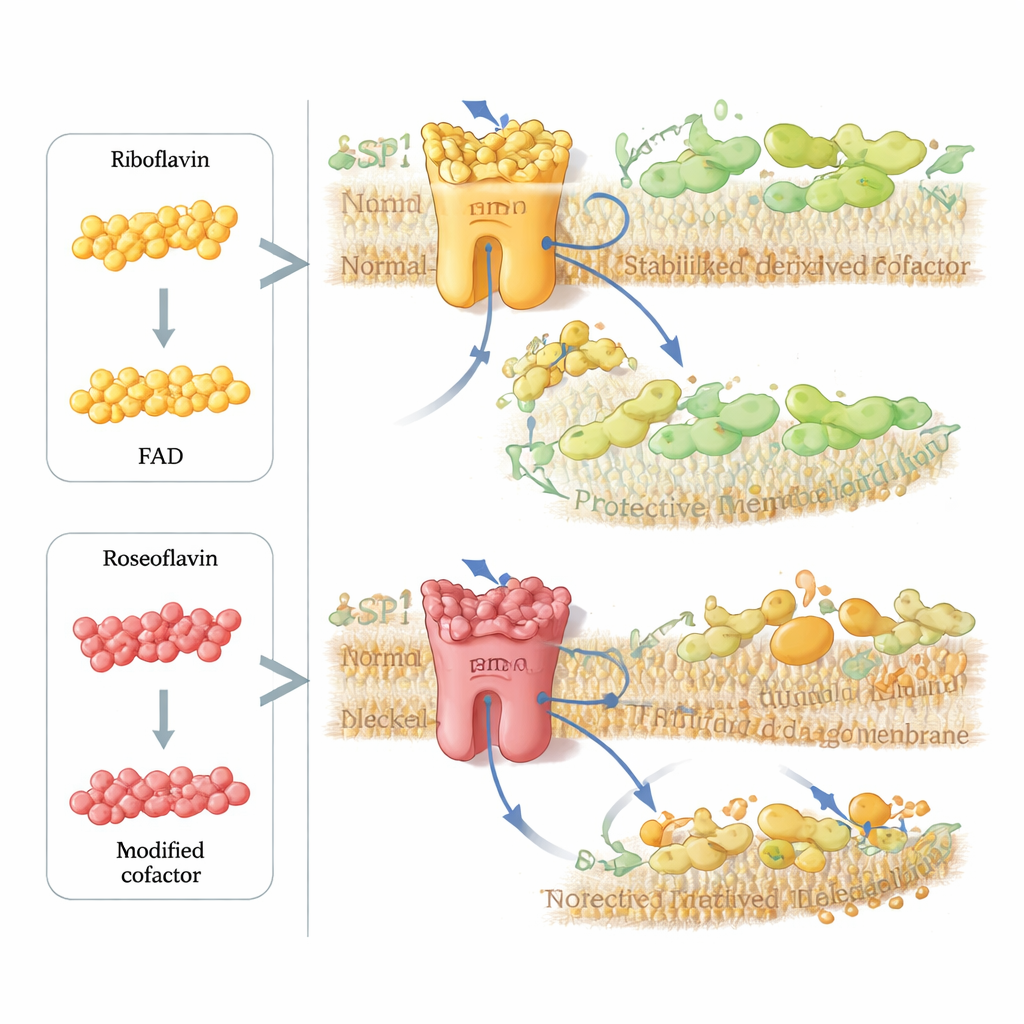
Następnie badacze zapytali, czy można celowo sabotować tę ochronną ścieżkę w komórkach nowotworowych. Sięgnęli po rozeoflawinę, naturalny antybiotyk produkowany przez niektóre bakterie, która bardzo przypomina ryboflawinę, ale zawiera niewielką zmianę chemiczną. Komórki pobierają rozeoflawinę i przekształcają ją w zmodyfikowaną wersję FAD, która może zająć miejsce w FSP1 i stabilizować strukturę enzymu, ale nie jest w stanie prawidłowo przenosić elektronów. W testach na oczyszczonym enzymie i w symulacjach komputerowych FSP1 obciążony kofaktorem pochodzącym z rozeoflawiny był praktycznie bezsilny. W wielu liniach komórek nowotworowych maleńkie, nanomolowe dawki rozeoflawiny znacznie zwiększały śmiercionośność inhibitorów GPX4, lecz tylko gdy FSP1 był obecny, pokazując, że związek celowo unieszkodliwia ten obwód naprawy błony.
Co to znaczy dla zdrowia i terapii
Podsumowując, praca przekształca ryboflawinę z prostego składnika odżywczego w głównego regulatora krytycznego przełącznika śmierci komórkowej. Poprzez włączenie się w syntezę kofaktora FAD, ryboflawina kontroluje stabilność i aktywność FSP1, który z kolei decyduje o tym, jak skutecznie komórki odzyskują rozpuszczalne w lipidach antyoksydanty i opierają się uszkodzeniom błony. Zbyt mało ryboflawiny osłabia tę tarczę i sprzyja ferroptozie; inteligentnie zaprojektowane analogi, takie jak rozeoflawina, mogą porwać tę samą ścieżkę, by na żądanie unieszkodliwić FSP1. Dla laika wniosek jest taki, że mikroelementy robią więcej niż „wspierają metabolizm” — mogą na stałe wpływać na to, czy komórki przetrwają stres oksydacyjny. To odkrycie otwiera nowe drogi do uczulania guzów na terapię, dopracowania strategii antyoksydacyjnych i lepszego zrozumienia, jak dieta może wpływać na choroby, w których ferroptoza odgrywa kluczową rolę.
Cytowanie: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Słowa kluczowe: ferroptoza, ryboflawina, FSP1, peroksydacja lipidów, terapia przeciwnowotworowa