Clear Sky Science · it
Il metabolismo della riboflavina modula la resistenza alla ferroptosi guidata da FSP1
Perché questa storia sulle vitamine conta
La maggior parte delle persone conosce le vitamine come qualcosa da assumere al mattino per la salute generale. Questo studio mostra che una vitamina familiare, la riboflavina (vitamina B2), può svolgere un ruolo molto più drammatico all’interno delle nostre cellule: aiuta a decidere se le cellule sotto stress vivono o muoiono attraverso una forma di danno guidata dal ferro chiamata ferroptosi. Poiché la ferroptosi è legata al cancro, alla neurodegenerazione e agli infarti, scoprire come un nutriente comune modula questo processo potrebbe infine influenzare il modo in cui progettiamo diete e farmaci per queste malattie.
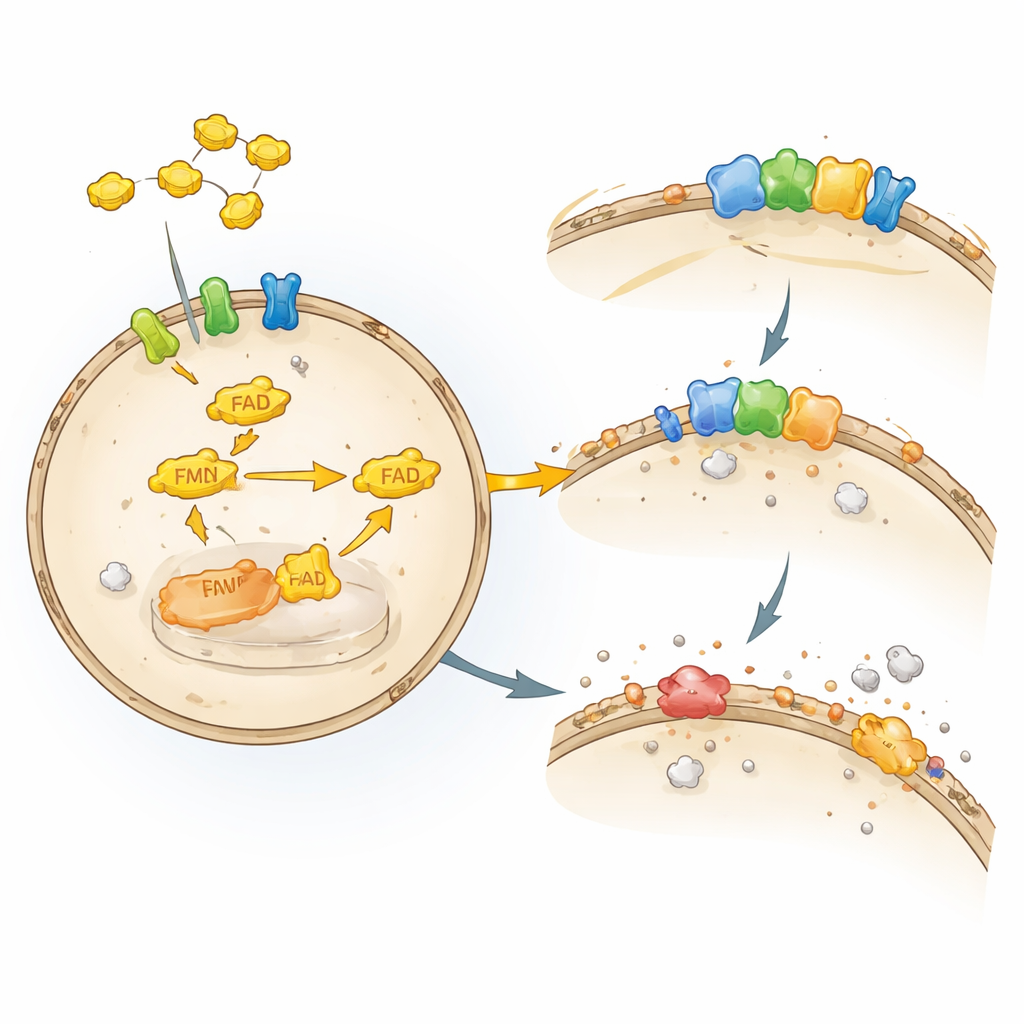
Uno scudo fragile attorno alle nostre cellule
Ogni cellula è avvolta da una sottile membrana lipidica che funziona come una parete e una multipresa insieme. Quo strato lipidico è facilmente danneggiato da certe forme di ossigeno, in un processo noto come perossidazione lipidica. Quando questo danno sfugge al controllo, le cellule subiscono ferroptosi, una forma regolata di morte cellulare che dipende dal ferro e dai lipidi ossidati. Le nostre cellule dispongono di diversi sistemi di difesa per fermare questa cascata. Un guardiano chiave, l’enzima GPX4, usa l’antiossidante glutatione per detossificare i perossidi lipidici dannosi. Un altro guardiano, FSP1, si trova alla membrana e mantiene gli antiossidanti liposolubili come il coenzima Q e la vitamina K nella loro forma attiva e protettiva, agendo come una stazione di riciclo per queste molecole.
Alla ricerca degli aiutanti nascosti di un guardiano cellulare
Sebbene FSP1 fosse noto come un potente freno alla ferroptosi, i ricercatori non sapevano quali fattori cellulari ne sostenessero il funzionamento. Gli autori hanno ingegnerizzato cellule tumorali umane in modo che dipendessero interamente da FSP1 per sopravvivere quando GPX4 era disattivato. Hanno quindi usato uno screen mirato CRISPR–Cas9, eliminando circa 3.000 geni rilevanti per i farmaci per vedere quali perdite rendevano le cellule improvvisamente vulnerabili. Tra i risultati più forti ci sono stati enzimi e trasportatori coinvolti nella gestione della riboflavina, in particolare la riboflavina chinasi (RFK) e la flavina adenina dinucleotide sintetasi (FADS), che costruiscono il cofattore FAD a partire dalla riboflavina. Quando questi geni sono stati disturbati, i livelli proteici di FSP1 sono diminuiti, il danno lipidico è aumentato e le cellule sono morte per ferroptosi, rivelando una dipendenza diretta a monte di FSP1 dai cofattori derivati dalla riboflavina.
La fornitura di vitamina come manopola per la sopravvivenza cellulare
Per verificare se fosse importante il nutriente stesso, e non solo gli enzimi, il gruppo ha coltivato le cellule in mezzo privo di riboflavina o contenente quantità più vicine a quelle presenti nel sangue umano, molto inferiori rispetto alle soluzioni standard di laboratorio. In condizioni povere di riboflavina, molte proteine dipendenti dalla flavina diminuivano, ma FSP1 è risultata tra le più fortemente deplegate, senza una caduta simile del suo RNA messaggero. Le cellule sono diventate molto più sensibili ai composti che bloccano GPX4 e le loro membrane hanno accumulato fosfolipidi ossidati, una caratteristica della ferroptosi. Importante, il semplice ripristino della riboflavina ha riportato i livelli proteici di FSP1 e ridotto il danno lipidico. Anche spostamenti modesti della riboflavina entro un intervallo fisiologico hanno modulato quanta protezione FSP1 le cellule potevano mettere in campo, suggerendo che le variazioni quotidiane nello stato di vitamina B2 possano influenzare silenziosamente come i tessuti affrontano lo stress ossidativo.
Invertire una vitamina utile contro il cancro
I ricercatori si sono poi chiesti se fosse possibile sabotare deliberatamente questa via protettiva nelle cellule tumorali. Hanno esaminato la roseoflavina, un antibiotico naturale prodotto da alcuni batteri che somiglia molto alla riboflavina ma presenta una piccola modifica chimica. Le cellule assumono la roseoflavina e la convertono in una versione modificata di FAD che può inserirsi in FSP1 e stabilizzare la struttura dell’enzima, ma non può trasferire elettroni correttamente. In test con enzimi purificati e simulazioni al computer, FSP1 caricato con il cofattore derivato dalla roseoflavina risultava sostanzialmente impotente. In molte linee cellulari tumorali, dosi minime, nell’ordine dei nanomolari, di roseoflavina hanno aumentato drasticamente il potere letale degli inibitori di GPX4, ma solo quando FSP1 era presente, dimostrando che il composto danneggia specificamente questo circuito di riparazione della membrana.
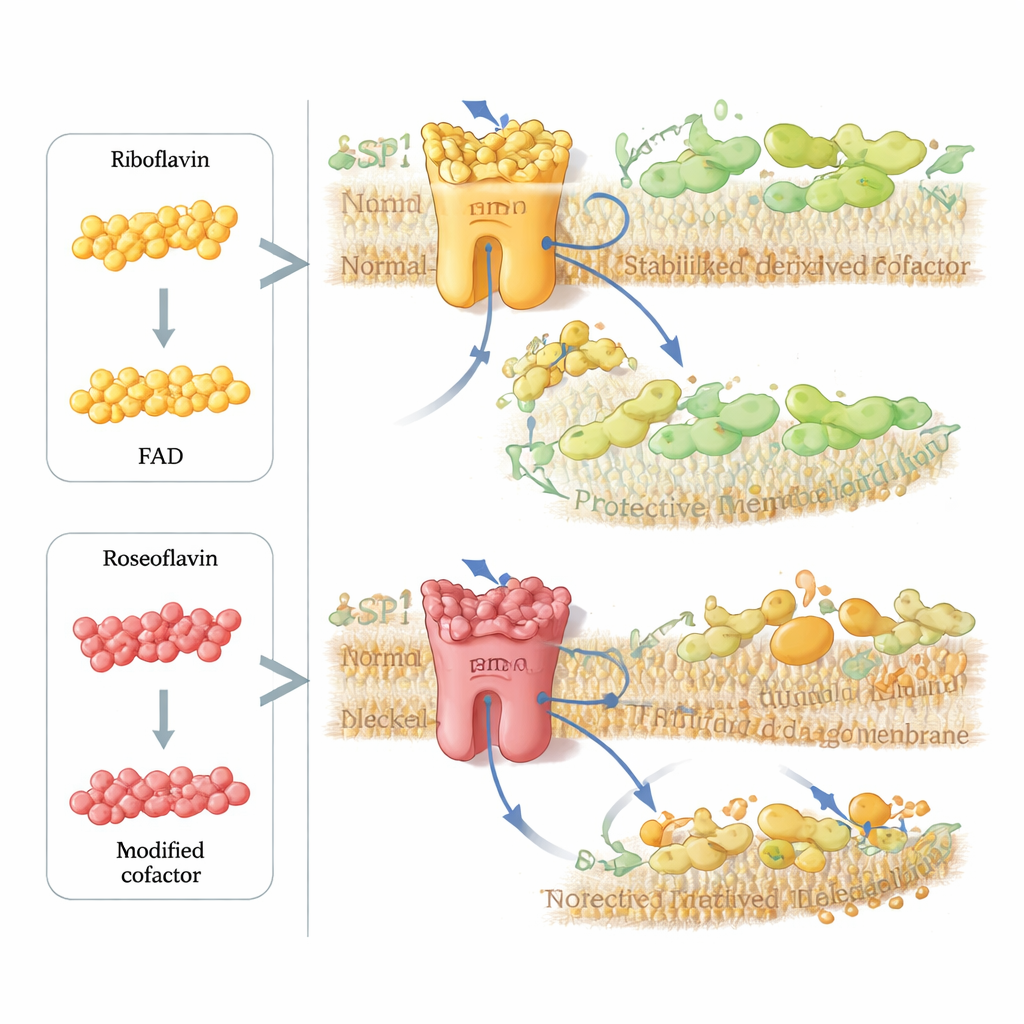
Cosa significa per la salute e la terapia
Nel loro insieme, i risultati ricollocano la riboflavina da nutriente semplice a regolatore maestro di un interruttore critico della morte cellulare. Alimentando il cofattore FAD, la riboflavina controlla la stabilità e l’attività di FSP1, che a sua volta governa quanto efficacemente le cellule riciclano gli antiossidanti liposolubili e resistono al danno della membrana. Troppa poca riboflavina indebolisce questo scudo e favorisce la ferroptosi; analoghi progettati con ingegno come la roseoflavina possono dirottare la stessa via per disabilitare FSP1 su richiesta. Per il lettore non specialistico, la conclusione è che i micronutrienti fanno più che “sostenere il metabolismo”: possono determinare se le cellule sopravvivono allo stress ossidativo. Questa intuizione apre nuove strade per sensibilizzare i tumori alle terapie, perfezionare le strategie antiossidanti e comprendere meglio come la dieta possa influenzare le malattie in cui la ferroptosi svolge un ruolo centrale.
Citazione: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Parole chiave: ferroptosi, riboflavina, FSP1, perossidazione lipidica, terapia del cancro