Clear Sky Science · ar
استقلاب الريبوفلافين يشكل مقاومة الفيروبتوسيس التي يقودها FSP1
لماذا تهمنا قصة هذا الفيتامين
يعرف معظم الناس الفيتامينات كشيء تتناوله في الصباح للصحة العامة. تُظهر هذه الدراسة أن فيتامينًا مألوفًا واحدًا، الريبوفلافين (فيتامين B2)، قد يقوم بدور أكثر دراماتيكية داخل خلايانا: فهو يساعد في تقرير ما إذا كانت الخلايا المتعرضة للإجهاد ستبقى حية أم تموت عبر شكل من الضرر المدفوع بالحديد يُسمى الفيروبتوسيس. وبما أن الفيروبتوسيس مرتبط بالسرطان والتنكس العصبي والنوبات القلبية، فقد يؤثر كشف الكيفية التي يضبط بها هذا المغذّي الشائع هذه العملية في نهاية المطاف على تصميم الحميات الدوائية والعلاجات لهذه الأمراض.
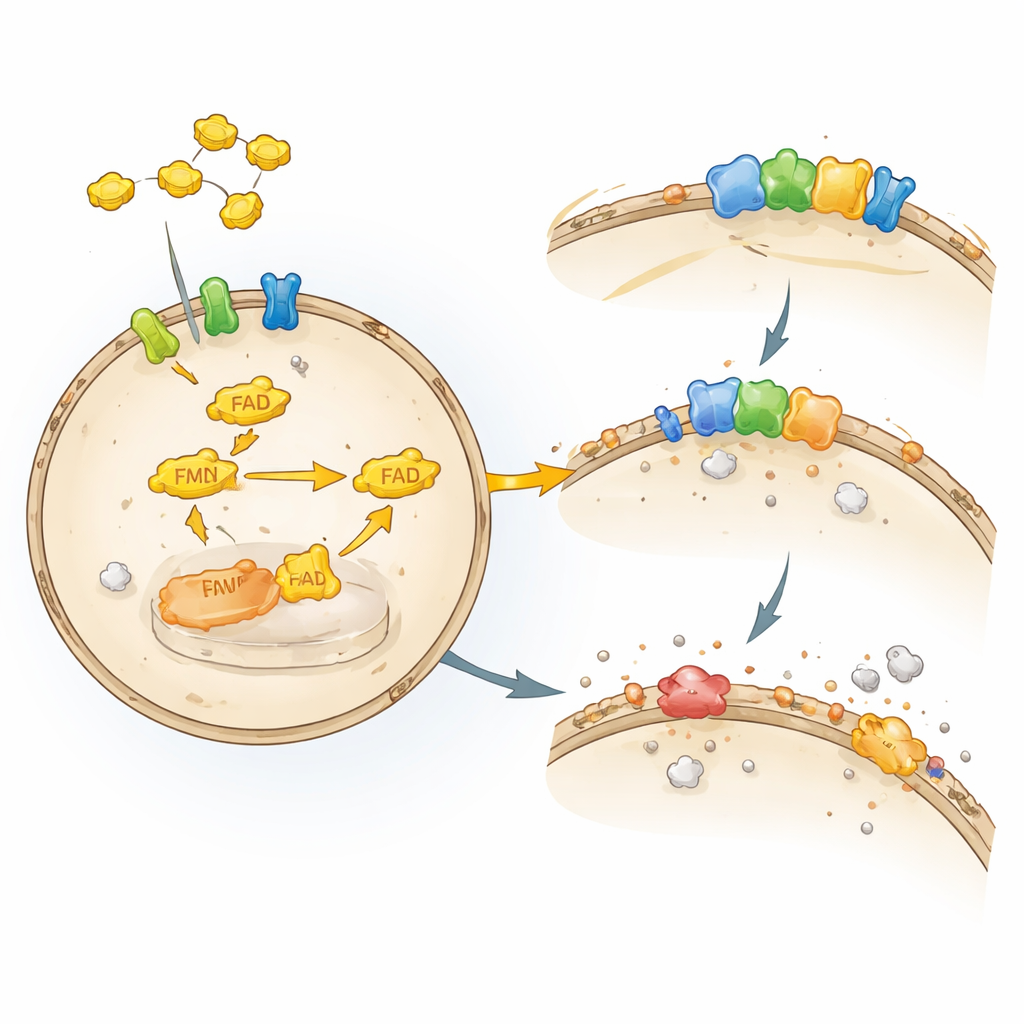
درع هش حول خلايانا
تُحاط كل خلية بغشاء دهني رقيق يعمل كمزيج من جدار ومصدر طاقة. هذا الطبق الدهني يتعرض بسهولة للتلف بواسطة أشكال معينة من الأكسجين، في عملية تُعرف بأكسدة الدهون. عندما يخرج هذا الضرر عن السيطرة، تدخل الخلايا في الفيروبتوسيس، وهو شكل منظم من موت الخلايا يعتمد على الحديد والدهون المؤكسدة. تنشر خلايانا عدة أنظمة دفاعية لوقف هذا التسلسل. أحد الحراس الرئيسيين، الإنزيم GPX4، يستخدم مضاد الأكسدة غلوتاثيون لإزالة سمية البيروكسيدات الدهنية الضارة. حارس آخر، FSP1، يقع عند الغشاء ويُبقي مضادات الأكسدة القابلة للذوبان في الدهون مثل أنزيم المساعدة Q وفيتامين K في شكلها النشط الواقي، ويعمل كمحطة إعادة تدوير لهذه الجزيئات.
اكتشاف المساعدين الخفيين لحارس الخلية
على الرغم من أن FSP1 كان معروفًا كفرملة قوية للفيروبتوسيس، لم يكن الباحثون يعرفون العوامل الخلوية التي تحافظ على عمله بسلاسة. حرر المؤلفون خلايا سرطانية بشرية بحيث تعتمد بالكامل على FSP1 للبقاء عندما يُعطل GPX4. ثم استخدموا شاشة تحرير جيني مركزة CRISPR–Cas9، حذفوا فيها حوالي 3000 جين ذي صلة بالأدوية لمعرفة أي حالات خسارة تجعل الخلايا عرضة فجأة. من بين النتائج الأقوى كانت إنزيمات وناقلات متورطة في معالجة الريبوفلافين، خاصة كيناز الريبوفلافين (RFK) وإنزيم تركيب FLAD (FADS)، اللذان يبنيان العامل المساعد FAD من الريبوفلافين. عندما تعطلت هذه الجينات، انخفضت مستويات بروتين FSP1، وتزايدت أضرار الدهون، وماتت الخلايا عبر الفيروبتوسيس، كاشفةً اعتماد FSP1 المباشر على العوامل المساعدة المشتقة من الريبوفلافين.
إمداد الفيتامين كمُنظّم لبقاء الخلية
لاختبار ما إذا كان المغذّي نفسه، وليس الإنزيمات فقط، مهمًا، زرع الفريق الخلايا في وسط خالٍ من الريبوفلافين أو يحتوي على كميات أقرب إلى تلك الموجودة في دم الإنسان، وهي أقل بكثير من المحاليل المختبرية القياسية. في ظروف فقيرة بالريبوفلافين، انخفضت العديد من البروتينات المعتمدة على الفلافين، لكن FSP1 كان من بين الأكثر انخفاضًا بشكل قوي، دون تراجع مشابه في حمضه النووي الرسول. أصبحت الخلايا أكثر حساسية بكثير للمركبات التي تحجب GPX4، وتراكمت في أغشيتها الفسفوليبيدات المؤكسدة، وهي سمة مميزة للفيروبتوسيس. ومن المهم أن استعادة الريبوفلافين ببساطة أعادت بروتين FSP1 وقللت من تلف الدهون. حتى التغيرات الطفيفة في مستوى الريبوفلافين ضمن نطاق فيسيولوجي ضبطت مقدار الحماية التي يمكن أن يوفرها FSP1 للخلايا، مما يوحي بأن التباينات اليومية في حالة فيتامين B2 قد تؤثر بهدوء على قدرة الأنسجة على مواجهة الإجهاد التأكسدي.
تحويل فيتامين مفيد ضد السرطان
سأل الباحثون بعد ذلك ما إذا كانوا يستطيعون عمدًا تعطيل هذه المسار الوقائي في الخلايا السرطانية. لجأوا إلى الروزيوفلافين، وهو مضاد حيوي طبيعي تصنعه بعض البكتيريا ويشبه الريبوفلافين بدرجة كبيرة لكنه يحمل تغييرًا كيميائيًا طفيفًا. تبتلع الخلايا الروزيوفلافين وتحوّله إلى نسخة معدلة من FAD يمكنها أن تتناسب مع FSP1 وتُستقر بنية الإنزيم، لكنها لا تستطيع حمل الإلكترونات بشكل صحيح. في اختبارات على الإنزيم المنقى ومحاكيات حاسوبية، كان FSP1 المحمّل بعامل روزيوفلافين شبه عاجز. في عدة خطوط خلايا سرطانية، عززت جرعات ضئيلة بنانومول من الروزيوفلافين بحدة قدرة مثبطات GPX4 على القتل، لكن ذلك فقط عندما كان FSP1 حاضرًا، مما يظهر أن الدواء يعيق على وجه التحديد دارة إصلاح الغشاء هذه.
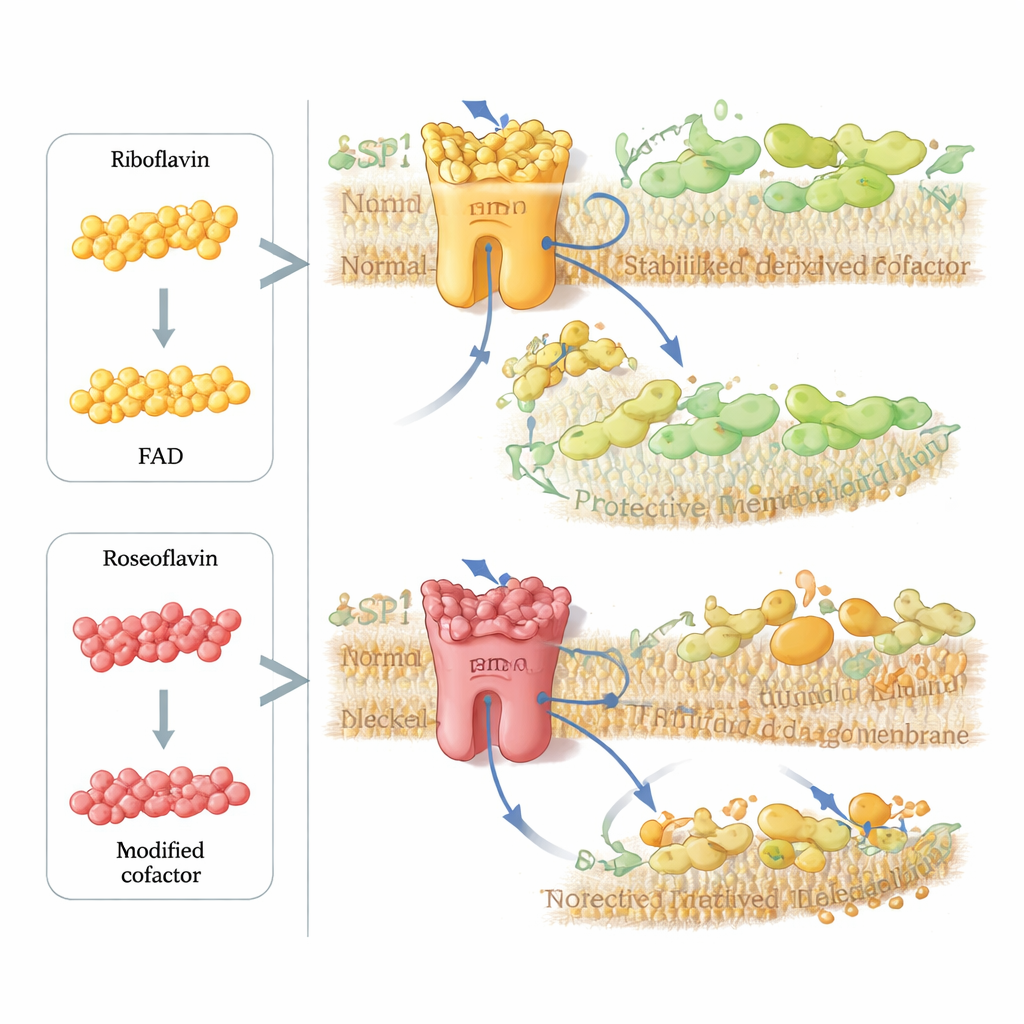
ما يعنيه هذا للصحة والعلاج
معًا، تعيد هذه الدراسة صياغة الريبوفلافين من مجرد مغذّي بسيط إلى منظم رئيسي لمفتاح حاسم لموت الخلايا. عبر تغذيته لعامل FAD، يتحكم الريبوفلافين في ثبات ونشاط FSP1، والذي بدوره يحكم مدى فعالية الخلايا في إعادة تدوير مضادات الأكسدة القابلة للذوبان في الدهون ومقاومة تلف الغشاء. نقص الريبوفلافين يضعف هذا الدرع ويعزز الفيروبتوسيس؛ وبالمقابل يمكن لمولدات تناظرية مصممة بذكاء مثل الروزيوفلافين أن تختطف نفس المسار لتعطيل FSP1 عند الطلب. للمستخدم العادي، الخلاصة هي أن المغذيات الصغرى تقوم بأكثر من "دعم الأيض"—فهي قد تحدد بشكل جوهري ما إذا كانت الخلايا ستصمد أمام الإجهاد التأكسدي. تفتح هذه الرؤية طرقًا جديدة لجعل الأورام أكثر حساسية للعلاج، وصقل استراتيجيات مضادات الأكسدة، وفهم أفضل لكيفية تأثير النظام الغذائي على الأمراض التي يلعب فيها الفيروبتوسيس دورًا مركزيًا.
الاستشهاد: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
الكلمات المفتاحية: الفيروبتوسيس, الريبوفلافين, FSP1, أكسدة الدهون, علاج السرطان