Clear Sky Science · es
El metabolismo de la riboflavina modula la resistencia a la ferroptosis dirigida por FSP1
Por qué importa esta historia sobre una vitamina
La mayoría de la gente conoce las vitaminas como algo que se toma por la mañana para la salud general. Este estudio muestra que una vitamina familiar, la riboflavina (vitamina B2), puede hacer algo mucho más dramático dentro de nuestras células: ayuda a decidir si las células estresadas viven o mueren mediante una forma de daño impulsado por hierro llamada ferroptosis. Dado que la ferroptosis está vinculada al cáncer, la neurodegeneración y los infartos, desvelar cómo un nutriente común regula este proceso podría, con el tiempo, influir en el diseño de dietas y fármacos para estas enfermedades.
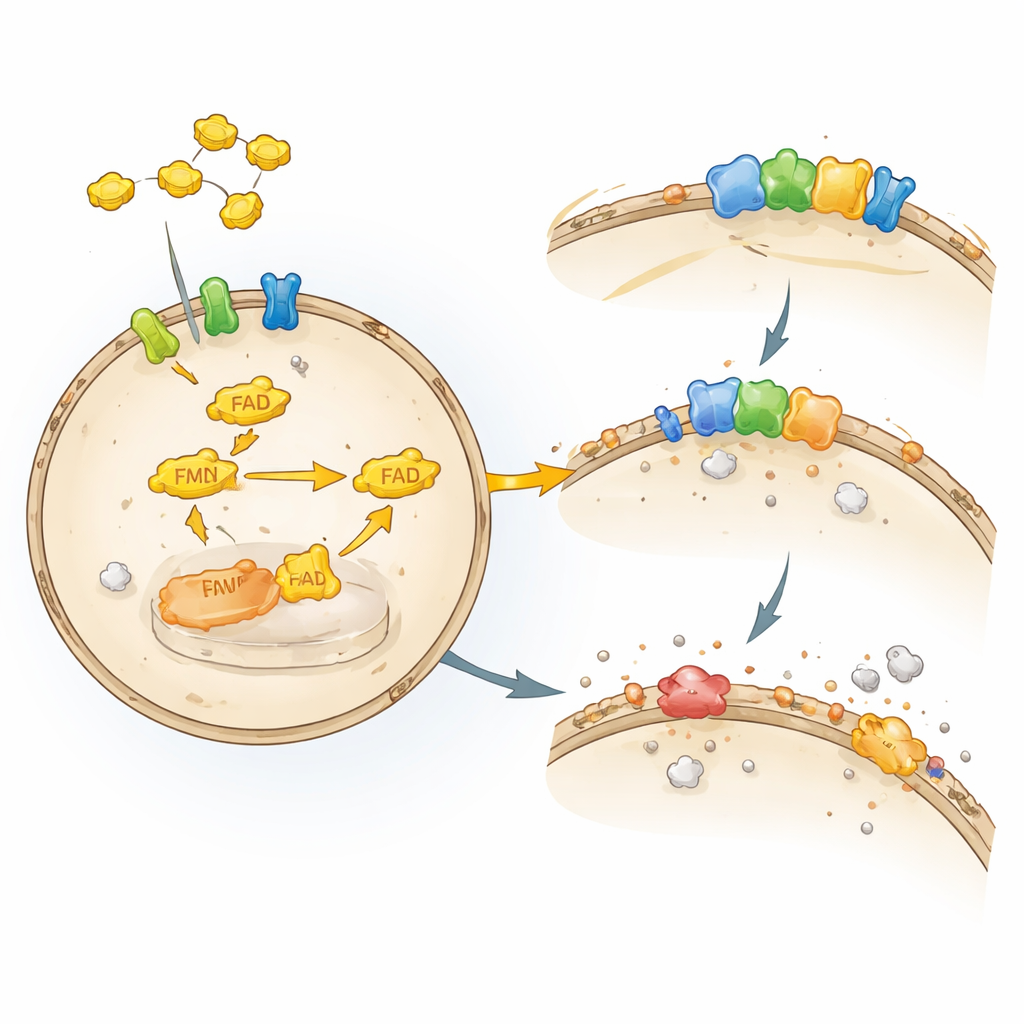
Un escudo frágil alrededor de nuestras células
Cada célula está envuelta en una fina membrana grasa que funciona como una combinación de muro y regleta eléctrica. Esa capa grasa se daña con facilidad por determinadas formas de oxígeno, en un proceso conocido como peroxidación lipídica. Cuando este daño se descontrola, las células sufren ferroptosis, una forma regulada de muerte celular que depende del hierro y de los lípidos oxidados. Nuestras células despliegan varios sistemas de defensa para detener esta cascada. Un guardián clave, la enzima GPX4, utiliza el antioxidante glutatión para desintoxicar los peróxidos lipídicos nocivos. Otro guardián, FSP1, se sitúa en la membrana y mantiene a los antioxidantes liposolubles como la coenzima Q y la vitamina K en su forma activa y protectora, funcionando como una estación de reciclaje para estas moléculas.
Encontrar los ayudantes ocultos de un guardián celular
Aunque se sabía que FSP1 era un freno poderoso de la ferroptosis, los investigadores no conocían qué factores celulares lo mantenían funcionando correctamente. Los autores modificaron células cancerosas humanas para que dependieran exclusivamente de FSP1 para sobrevivir cuando GPX4 estaba desactivada. Luego usaron una pantalla focalizada de edición genética CRISPR–Cas9, inactivando alrededor de 3.000 genes relevantes para fármacos para ver qué pérdidas volvían a las células súbitamente vulnerables. Entre los resultados más fuertes aparecieron enzimas y transportadores implicados en el manejo de la riboflavina, especialmente la riboflavina quinasa (RFK) y la sintasa de flavina adenina dinucleótido (FADS), que construyen el cofactor FAD a partir de riboflavina. Cuando estos genes se alteraron, los niveles de proteína FSP1 cayeron, aumentó el daño lipídico y las células murieron por ferroptosis, revelando una dependencia directa aguas arriba de FSP1 de los cofactores derivados de la riboflavina.
El suministro de la vitamina como regulador de la supervivencia celular
Para probar si era el nutriente en sí, y no solo las enzimas, el equipo cultivó células en medios sin riboflavina o con cantidades más cercanas a las presentes en la sangre humana, que son mucho menores que en las soluciones estándar de laboratorio. En condiciones pobres en riboflavina, muchas proteínas dependientes de flavina disminuyeron, pero FSP1 fue de las más fuertemente agotadas, sin una caída similar en su ARN mensajero. Las células se volvieron mucho más sensibles a compuestos que bloquean GPX4 y sus membranas acumularon fosfolípidos oxidados, una marca de la ferroptosis. Es importante que simplemente restaurar la riboflavina devolviera la proteína FSP1 y redujera el daño lipídico. Incluso cambios modestos en la riboflavina dentro de un rango fisiológico ajustaron cuánto protección por FSP1 podían movilizar las células, lo que sugiere que las variaciones cotidianas en el estado de la vitamina B2 pueden influir discretamente en cómo los tejidos hacen frente al estrés oxidativo.
Convertir una vitamina útil contra el cáncer
Los investigadores se preguntaron luego si podían sabotear deliberadamente esta vía protectora en células cancerosas. Recurriron a la roseoflavina, un antibiótico natural producido por ciertas bacterias que se parece mucho a la riboflavina pero presenta un pequeño cambio químico. Las células captan la roseoflavina y la convierten en una versión modificada de FAD que puede encajar en FSP1 y estabilizar la estructura de la enzima, pero no puede transportar electrones correctamente. En pruebas con enzima purificada y simulaciones informáticas, FSP1 cargada con el cofactor de la roseoflavina resultó esencialmente impotente. En múltiples líneas celulares de cáncer, dosis diminutas, nanomolares, de roseoflavina aumentaron drásticamente el poder letal de los inhibidores de GPX4, pero solo cuando FSP1 estaba presente, mostrando que el fármaco incapacita específicamente este circuito de reparación de la membrana.
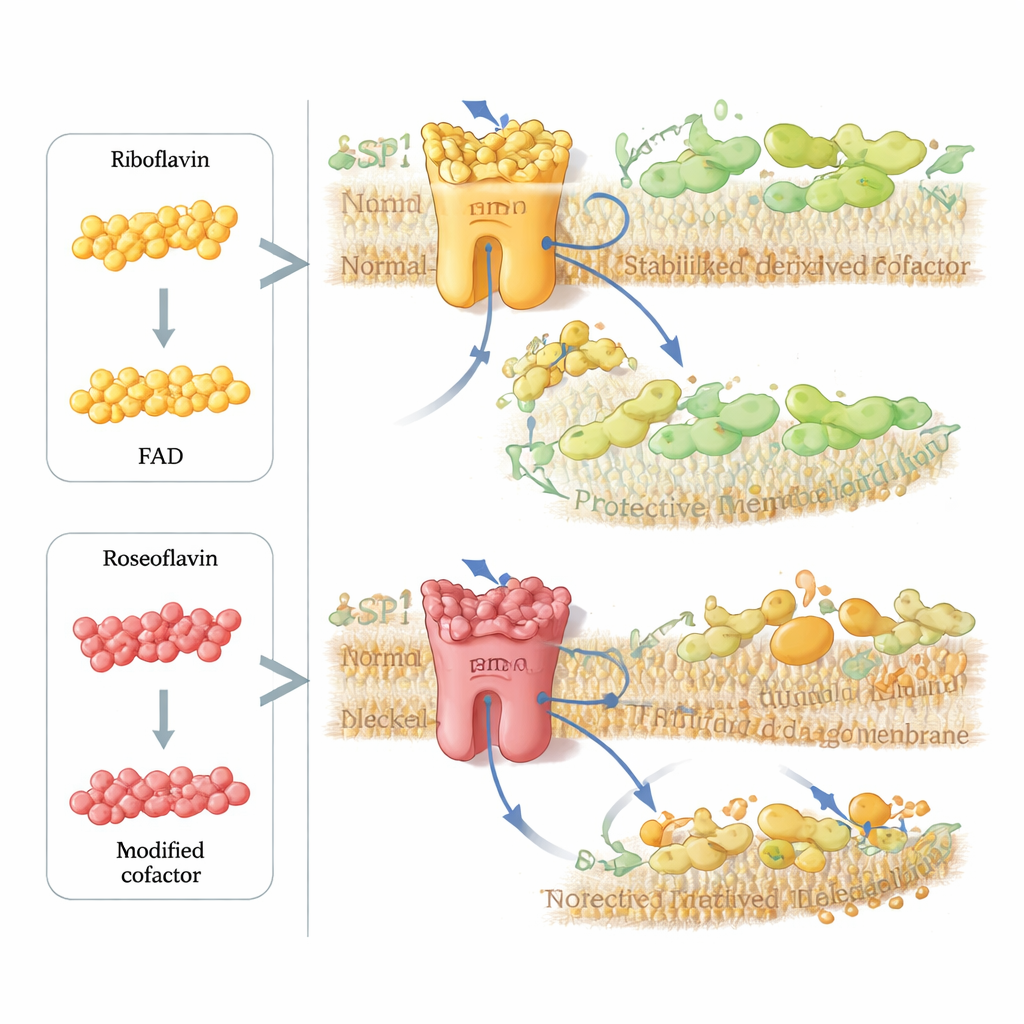
Qué significa esto para la salud y la terapia
En conjunto, el trabajo redefine la riboflavina desde un nutriente simple hacia un regulador maestro de un interruptor crítico de muerte celular. Al alimentar el cofactor FAD, la riboflavina controla la estabilidad y la actividad de FSP1, que a su vez gobierna la eficacia con la que las células reciclan antioxidantes liposolubles y resisten el daño de la membrana. Muy poca riboflavina debilita este escudo y promueve la ferroptosis; análogos diseñados con ingenio como la roseoflavina pueden secuestrar la misma vía para desactivar FSP1 a demanda. Para el público general, la conclusión es que los micronutrientes hacen más que «apoyar el metabolismo»: pueden fijar de forma determinante si las células sobreviven al estrés oxidativo. Este hallazgo abre nuevas vías para sensibilizar tumores a la terapia, refinar estrategias antioxidantes y comprender mejor cómo la dieta puede influir en enfermedades donde la ferroptosis desempeña un papel central.
Cita: Skafar, V., de Souza, I., Ghosh, B. et al. Riboflavin metabolism shapes FSP1-driven ferroptosis resistance. Nat Cell Biol 28, 696–706 (2026). https://doi.org/10.1038/s41556-025-01856-x
Palabras clave: ferroptosis, riboflavina, FSP1, peroxidación lipídica, terapia contra el cáncer