Clear Sky Science · pt
Diferenças populacionais na estrutura da duplicação do cromossomo 22q11.2 predispõem de forma distinta a microdeleções e inversões
Por que esse ponto sensível do cromossomo importa
Algumas pessoas nascem sem um pequeno trecho do cromossomo 22, uma alteração que pode causar defeitos cardíacos, dificuldades de aprendizagem, diferenças faciais e maior risco de esquizofrenia. Essa condição, chamada síndrome da deleção 22q11.2, é uma das desordens genéticas conhecidas mais comuns. Ainda assim, é curiosamente menos frequente em pessoas de ascendência africana. Este estudo investiga a estrutura detalhada do DNA nessa região cromossômica, mostrando como diferenças sutis entre populações podem alterar as chances de quebras perigosas, inversões e perdas de material genético.
Um trecho frágil de DNA repetido
Os autores se concentram em um trecho de 5 milhões de bases do DNA no cromossomo 22, chamado 22q11.2. Essa região é repleta de grandes segmentos repetidos quase idênticos, conhecidos como repetições de baixa cópia. Essas repetições funcionam como parágrafos parecidos em um livro: quando as células formam óvulos ou espermatozoides, a maquinaria de cópia pode alinhar por engano repetições erradas e trocar pedaços entre elas. Esse processo, chamado recombinação homóloga não alelica, pode deletar seções, duplicá-las ou invertê-las. A maioria dos casos da síndrome da deleção 22q11.2 surge quando dois blocos repetidos específicos, denominados A e D, emparelham de forma incorreta e removem um segmento de aproximadamente 3 milhões de bases que contém dezenas de genes importantes para o desenvolvimento e a função cerebral.
Lendo a região de ponta a ponta
Até recentemente, essa parte do cromossomo 22 era demasiado repetitiva e complexa para ser lida de forma limpa com o sequenciamento padrão. Os pesquisadores usaram novas tecnologias de leitura longa que podem seguir trechos de DNA de dezenas de milhares de bases, combinadas com softwares de montagem aprimorados, para reconstruir 135 versões completas desse segmento cromossômico a partir de pessoas de várias partes do mundo, além de várias espécies de primatas. Eles descobriram 63 “haplótipos” estruturais distintos — diferentes maneiras como os blocos repetidos na região A estão organizados e dimensionados — variando mais de onze vezes em comprimento. Grande parte dessa diversidade vem de uma unidade repetida central com cerca de 105.000 bases, emoldurada por peças repetidas mais curtas. Essa unidade central se multiplicou e embaralhou especificamente em humanos ao longo do último milhão de anos, tornando nossa versão de 22q11.2 muito mais elaborada do que a de chimpanzés, gorilas ou orangotangos.
Diferenças populacionais em um campo minado genético
Ao comparar grupos humanos, a equipe descobriu que indivíduos de ascendência africana tendem a ter versões do bloco A mais longas e ricas em repetições do que não africanos. Contraintuitivamente, essas estruturas mais longas frequentemente colocam repetições-chave em orientações opostas em relação às suas parceiras no bloco D. Nessa disposição, o emparelhamento incorreto tende a produzir inversões — giros inofensivos de segmentos de DNA — em vez de grandes deleções que removem genes. Usando comparações tanto dentro do mesmo cromossomo quanto entre cromossomos das unidades centrais de 105.000 bases, os autores construíram um ranking de haplótipos mais propensos a gerar deleções versus aqueles mais propensos a gerar inversões. Haplótipos africanos foram significativamente enriquecidos por arquiteturas previstas para proteger contra a deleção clássica, enquanto haplótipos do Leste Asiático foram enriquecidos por estruturas previstas para favorecer deleções.
Acompanhando inversões e perdas no mundo real
Para testar essas previsões, os pesquisadores buscaram grandes inversões — segmentos de vários milhões de bases invertidos de ponta a ponta — em centenas de genomas. Identificaram vários tipos distintos de inversão que abrangem a região 22q11.2. Cada uma foi rara no conjunto, mas a maioria foi encontrada em pessoas de ascendência africana ou americana admixturada, o que corrobora a ideia de que a configuração local do DNA dessas populações favorece inversões em vez de deleções. A equipe então analisou com detalhe quatro famílias nas quais uma criança apresentou uma nova deleção 22q11.2 não presente em nenhum dos pais. Ao montar completamente os segmentos do cromossomo 22 dos pais e das crianças, os pesquisadores puderam localizar onde ocorreu a quebra e o reparo defeituoso. Em todos os casos, os pontos de quebra da deleção caíram dentro da unidade repetida de 105.000 bases, mas as posições exatas variaram, situando-se em pequenos trechos de sequência quase perfeitamente pareada que são especialmente propensos a emparelhamento incorreto.
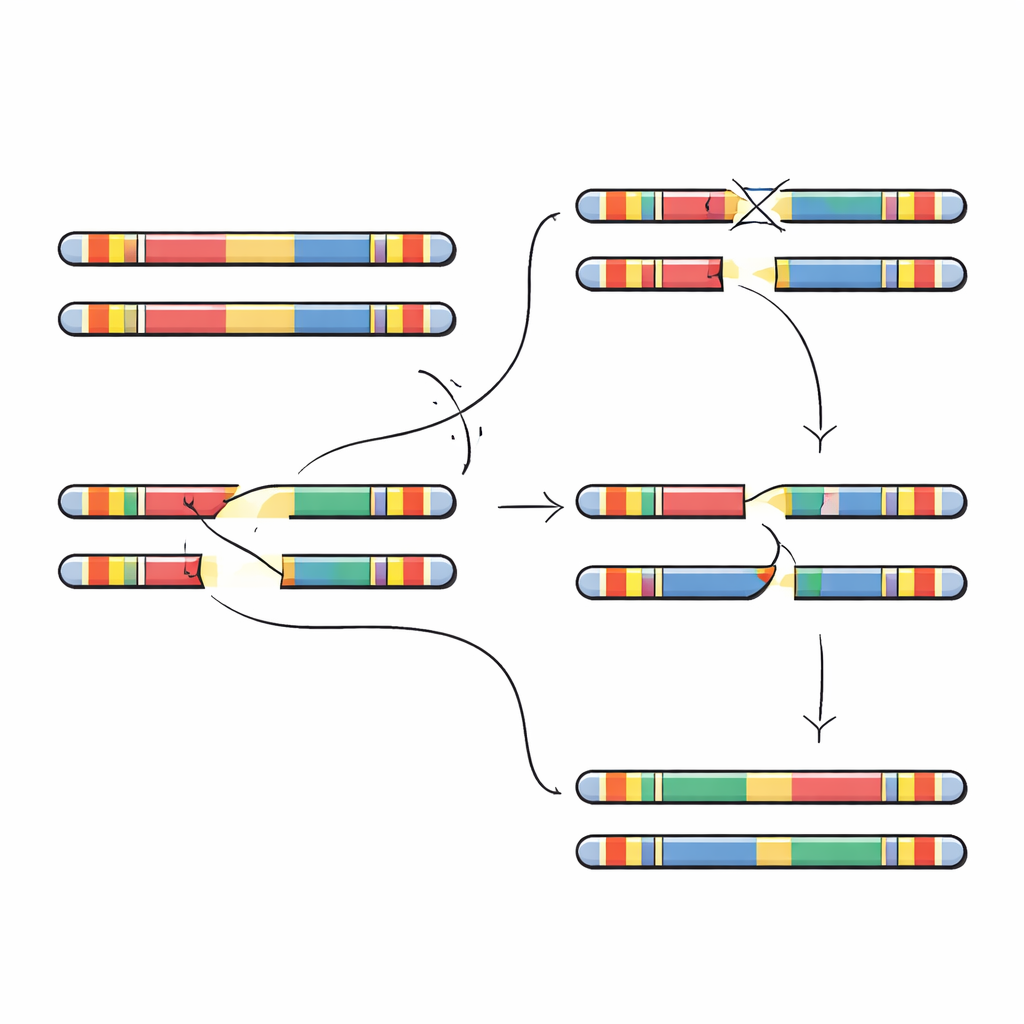
O que isso significa para risco e diagnóstico
Em conjunto, os achados mostram que nem todas as versões dessa região cromossômica são igualmente frágeis da mesma maneira. Algumas arquiteturas tendem a favorecer inversões do DNA, que frequentemente preservam o conteúdo gênico geral, enquanto outras produzem mais prontamente deleções que eliminam genes. Como as arquiteturas protetoras são mais comuns em pessoas de ascendência africana, isso ajuda a explicar por que a síndrome da deleção 22q11.2 tem sido observada com menos frequência nessas populações. Ao mesmo tempo, arquiteturas previstas como mais propensas a deleções são mais frequentes em genomas do Leste Asiático, sugerindo que triagens cuidadosas nesses grupos podem ser particularmente importantes. Mais amplamente, o trabalho demonstra como ler regiões complexas do genoma de ponta a ponta pode revelar diferenças estruturais ocultas que moldam quem é mais ou menos suscetível a padecer de graves desordens genéticas.
Citação: Porubsky, D., Yoo, D., Koundinya, N. et al. Population differences of chromosome 22q11.2 duplication structure predispose differentially to microdeletion and inversion. Nat Commun 17, 3701 (2026). https://doi.org/10.1038/s41467-026-71905-y
Palavras-chave: síndrome da deleção 22q11.2, variação estrutural cromossômica, duplicações segmentares, genômica populacional, instabilidade genômica