Clear Sky Science · nl
Populatieverschillen in de duplicatiestructuur van chromosoom 22q11.2 predisponeren differentieel voor microverwijdering en inversie
Waarom deze chromosoom-hotspot ertoe doet
Sommige mensen worden geboren zonder een klein stukje van chromosoom 22, een verandering die kan leiden tot hartafwijkingen, leerproblemen, gezichtsverschillen en een verhoogd risico op schizofrenie. Deze aandoening, 22q11.2 deletiesyndroom genoemd, is een van de meest voorkomende bekende genetische stoornissen. Toch komt ze opmerkelijk minder vaak voor bij mensen van Afrikaanse afkomst. Deze studie graaft in de fijne structuur van het DNA in dit chromosoomgebied en laat zien hoe subtiele verschillen tussen populaties de kans op schadelijke breuken, omkeringen en verlies van genetisch materiaal kunnen veranderen.
Een kwetsbare strook herhaald DNA
De auteurs richten zich op een stuk DNA van vijf miljoen letters op chromosoom 22, aangeduid als 22q11.2. Dit gebied zit vol met grote, bijna identieke herhaalde DNA-segmenten, bekend als low-copy repeats. Deze herhalingen werken als vergelijkbare alinea’s in een boek: wanneer cellen eicellen of zaadcellen vormen, kan de kopieermachine per ongeluk de verkeerde herhalingen naast elkaar leggen en stukken tussen hen uitwisselen. Dat proces, niet-allelische homologe recombinatie genoemd, kan secties verwijderen, verdubbelen of omkeren. De meeste gevallen van 22q11.2 deletiesyndroom ontstaan wanneer twee specifieke herhalingsblokken, A en D genoemd, verkeerd paren en een ongeveer 3 miljoen letters lang segment weghalen dat tientallen genen bevat die belangrijk zijn voor ontwikkeling en hersenfunctie.
Het gebied eind-tot-eind lezen
Tot voor kort was dit deel van chromosoom 22 te repetitief en complex om met standaard DNA-sequencing goed te lezen. De onderzoekers gebruikten nieuwe long-read technieken die DNA-stretches van tienduizenden letters kunnen volgen, gecombineerd met verbeterde assemblagesoftware, om 135 volledige versies van dit chromosoomsegment te reconstrueren van mensen wereldwijd, plus enkele mensapen. Ze ontdekten 63 verschillende structurele “haplotypes”—verschillende manieren waarop de herhalingsblokken in regio A zijn gerangschikt en van grootte—met een variatie in lengte van meer dan elfvoud. Veel van deze diversiteit komt van een kernherhalingseinheid van ongeveer 105.000 letters, omkaderd door kortere herhaalde stukjes. Deze kernunit is in de afgelopen miljoen jaar specifiek bij mensen vermenigvuldigd en geschud, waardoor onze versie van 22q11.2 veel complexer is geworden dan die van chimpansees, gorilla’s of orang-oetans.
Populatieverschillen in een genetisch mijnenveld
Toen het team menselijke groepen vergeleek, vonden ze dat individuen van Afrikaanse afkomst de neiging hadden om langere, meer herhalingsrijke versies van blok A te hebben dan niet-Afrikanen. Tegenintuïtief plaatsen deze langere structuren vaak sleutelherhalingen in tegengestelde oriëntaties ten opzichte van hun partners in blok D. In die configuratie leidt verkeerd paren eerder tot onschadelijke omkeringen, of inversies, van DNA-segmenten dan tot grote deleties die genen verwijderen. Met zowel binnen-chromosoom- als tussen-chromosoomvergelijkingen van de kern van 105.000-letter herhalingen bouwden de auteurs een rangorde van haplotypes die eerder tot deleties neigen versus die die eerder tot inversies neigen. Afrikaanse haplotypes waren significant verrijkt voor architecturen die naar verwachting beschermen tegen de klassieke deletie, terwijl Oost-Aziatische haplotypes verrijkt waren voor structuren die deleties zouden bevorderen.
Wereldwijde omkeringen en verlies volgen
Om deze voorspellingen te testen, zochten de onderzoekers in honderden genomen naar grote inversies—meer-Million-lettersegmenten die omgekeerd zijn—en identificeerden verschillende distincte type inversies die het 22q11.2-gebied overspannen. Elk type was in het geheel zeldzaam, maar de meeste werden gevonden bij mensen van Afrikaanse of gemengde Amerikaanse afkomst, wat overeenkomt met het idee dat hun lokale DNA-opmaak inversies boven deleties bevoordeelt. Het team zoomde vervolgens in op vier families waarbij een kind een nieuwe 22q11.2-deletie had die bij geen van beide ouders aanwezig was. Door de chromosoom 22-segmenten van ouders en kinderen volledig te assembleren, konden ze precies vaststellen waar de breuk en foutieve reparatie plaatsvonden. In elk geval vielen de deletie-breukpunten binnen de 105.000-letter herhalingseenheid, maar de exacte posities verschilden en lagen in kleine stroken bijna perfect overeenkomende sequentie die bijzonder vatbaar zijn voor verkeerd paren.
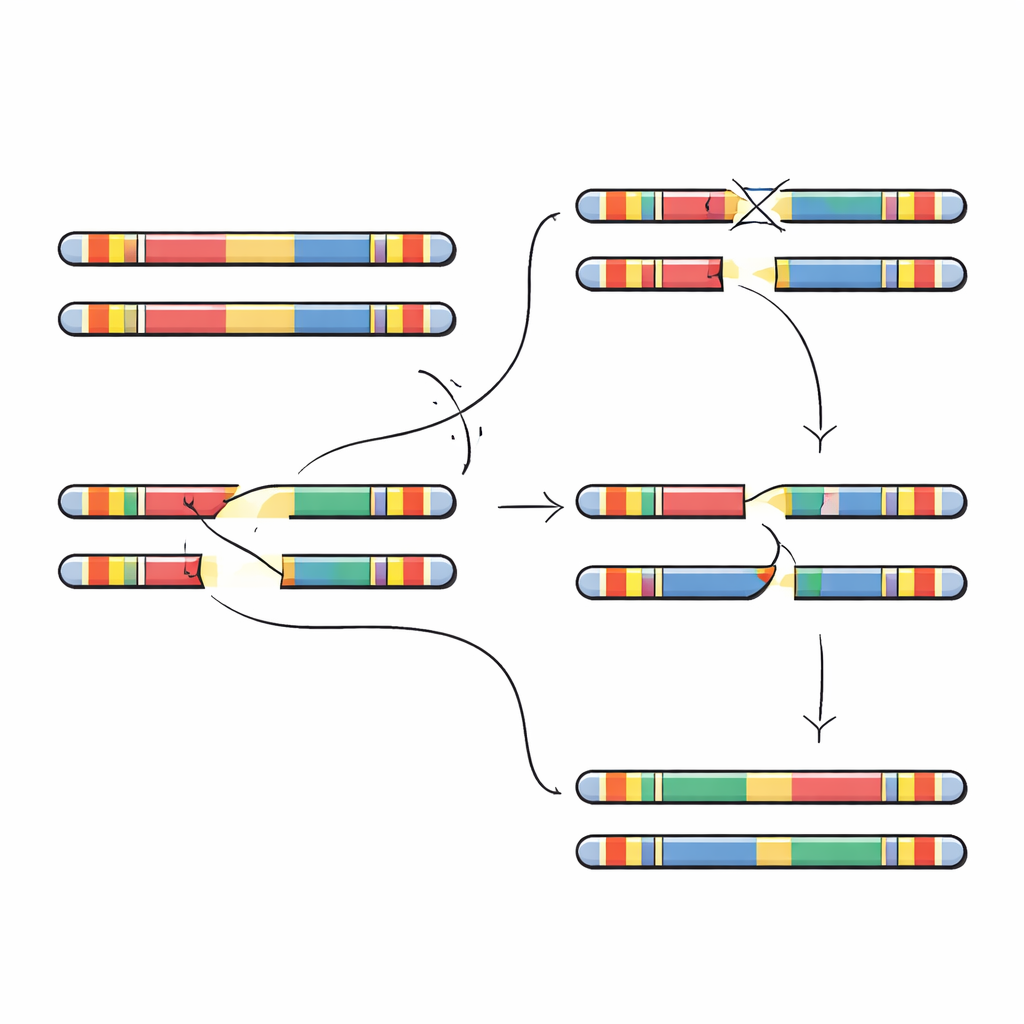
Wat dit betekent voor risico en diagnose
Gezamenlijk laten de bevindingen zien dat niet alle versies van dit chromosoomgebied even kwetsbaar zijn op dezelfde manier. Sommige architecturen neigen het systeem naar omkeringen van DNA, die vaak de totale hoeveelheid genen intact laten, terwijl andere gemakkelijker gene-verliesgevende deleties produceren. Omdat de beschermende architecturen vaker voorkomen bij mensen van Afrikaanse afkomst, helpt dit verklaren waarom 22q11.2 deletiesyndroom minder vaak is waargenomen in deze populaties. Tegelijkertijd komen architecturen die naar verwachting deleties bevorderen vaker voor in Oost-Aziatische genomen, wat suggereert dat zorgvuldige screening in deze groepen bijzonder belangrijk kan zijn. In bredere zin toont het werk aan hoe het eind-tot-eind lezen van complexe regio’s van het genoom verborgen structurele verschillen kan onthullen die bepalen wie meer of minder waarschijnlijk ernstige genetische aandoeningen ontwikkelt.
Bronvermelding: Porubsky, D., Yoo, D., Koundinya, N. et al. Population differences of chromosome 22q11.2 duplication structure predispose differentially to microdeletion and inversion. Nat Commun 17, 3701 (2026). https://doi.org/10.1038/s41467-026-71905-y
Trefwoorden: 22q11.2 deletiesyndroom, structurele variatie van chromosomen, segmentale duplicaties, populatiegenomica, genoominstabiliteit