Clear Sky Science · pt
Um pequeno descompasso entre o uso de códons de um gene e o suprimento celular de tRNA é benéfico
Quando escolhas “silenciosas” no DNA não são tão silenciosas
Nossos genes contêm muitas maneiras de escrever a mesma instrução, usando diferentes “palavras” de três letras no DNA que significam o mesmo aminoácido. Durante décadas, essas grafias alternativas — chamadas códons sinônimos — foram consideradas detalhes em grande parte triviais. Este estudo derruba essa visão. Mostra que o quão próximo o “sotaque” de códons de um gene corresponde à maquinaria de tradução da célula pode fazer a diferença entre crescimento lento e prosperidade, e que um pequeno descompasso pode, na verdade, ser o ideal.
Como as células leem as instruções genéticas
Para transformar genes em proteínas, as células usam pequenas moléculas adaptadoras chamadas tRNAs, que reconhecem códons no RNA mensageiro e entregam os aminoácidos corretos. Cada aminoácido (com duas exceções) possui vários códons possíveis, mas as células não os utilizam igualmente. Ao longo da evolução, os organismos desenvolvem um padrão característico de uso de códons e ajustam seu conjunto de tRNAs de acordo. A visão tradicional assume que a situação ideal é um casamento perfeito: os códons usados nos genes espelham os tRNAs disponíveis, proporcionando tradução rápida e precisa. Qualquer desvio desse casamento perfeito era pensado como resultado apenas da deriva genética e da mutação, não como algo vantajoso.
Um caso-teste usando resistência a antibióticos
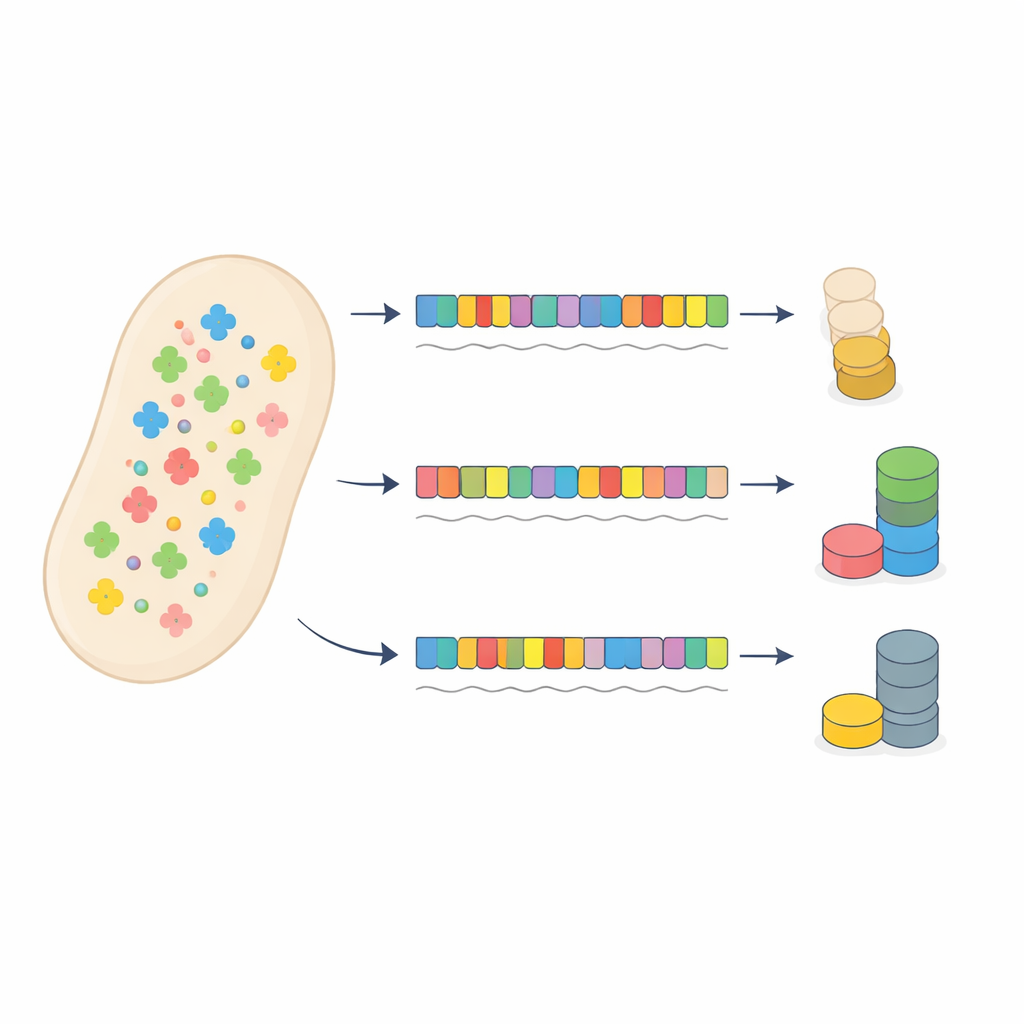
Os autores desafiaram esse quadro convencional ao redesenhar cuidadosamente um gene de resistência a antibiótico em bactérias. Eles criaram 53 versões de um gene de resistência à gentamicina que codificavam a mesma proteína, mas usavam diferentes padrões de códons sinônimos, variando de um quase casamento perfeito com o pool de tRNAs da célula até um forte descompasso. Cada versão foi colocada em um plasmídeo e fundida a um marcador fluorescente para que a produção de proteína pudesse ser medida. Uma segunda proteína fluorescente no mesmo plasmídeo atuou como sensor de quanto o sistema de tradução estava sendo exigido de modo geral, já que o uso intenso de tRNAs pelo gene de resistência retardaria a tradução de outras proteínas.
Encontrando o ponto ótimo para o crescimento
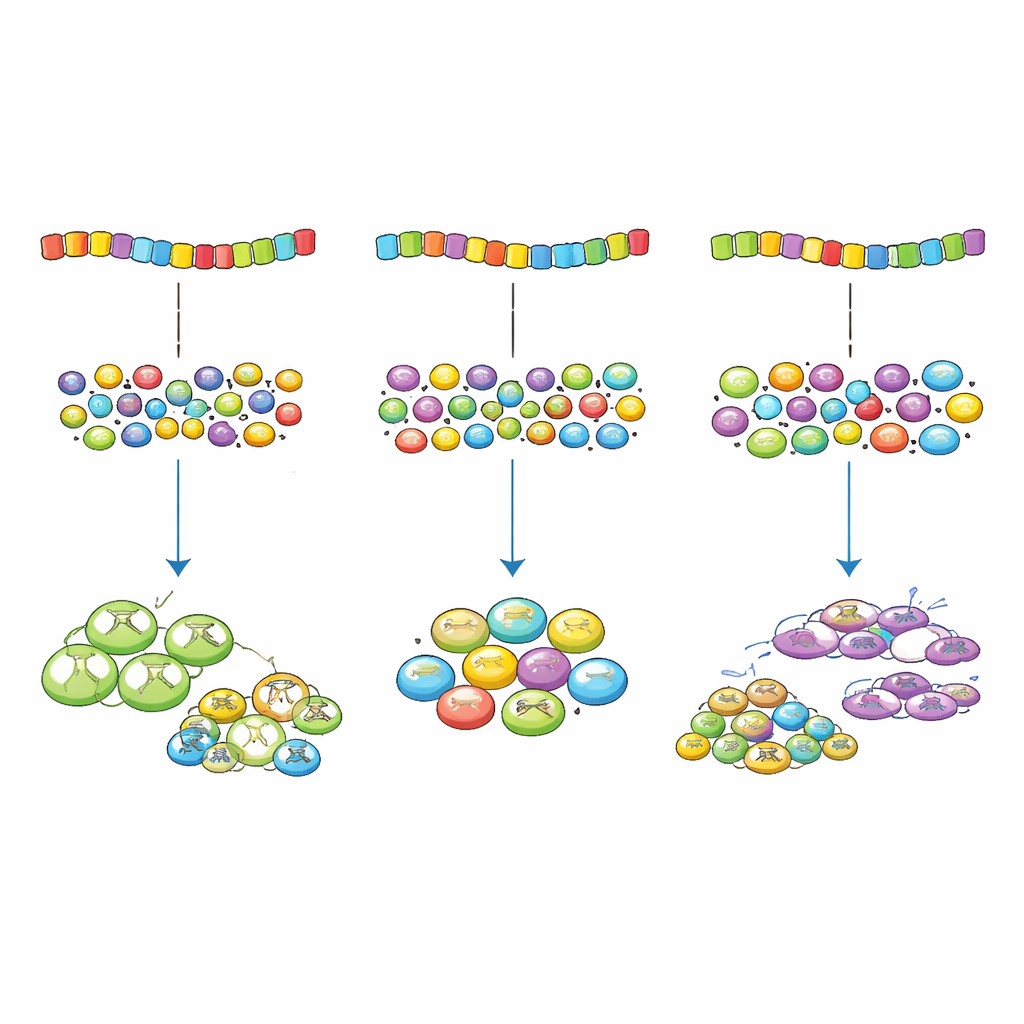
Quando essas bactérias modificadas cresceram em meio contendo gentamicina, genes cujos códons casavam extremamente bem com o pool de tRNA produziram a maior quantidade de proteína de resistência — mas também impuseram o maior ônus à maquinaria de tradução da célula. Bactérias portadoras de genes assim “super-otimizados” cresceram mais devagar do que as que carregavam um descompasso moderado. Em outras palavras, embora um melhor casamento aumentasse o benefício da proteína de resistência, ele também elevava o custo de usar recursos compartilhados de tradução, e além de certo ponto o custo prevalecia. As células de crescimento mais rápido foram aquelas cujas versões do gene apresentavam um pequeno, não mínimo, descompasso com o suprimento de tRNA, indicando que o verdadeiro ótimo equilibra benefício e custo em vez de maximizar apenas um dos lados.
Quando a importância do gene muda, o ótimo também muda
Em seguida, a equipe variou o quão crucial era o gene de resistência alterando a dose do antibiótico. Em níveis baixos de gentamicina, o benefício da proteína para a sobrevivência era modesto, e os padrões de códons com melhor desempenho apresentaram um descompasso relativamente grande, o que reduziu o desgaste desnecessário da tradução. À medida que a concentração do antibiótico aumentou e o gene se tornou mais importante, o padrão de códons ótimo deslocou-se em direção a um casamento mais próximo com o pool de tRNAs, e em doses muito altas o casamento quase perfeito foi o melhor. Experimentos semelhantes com um segundo gene de resistência e com a alteração direta do suprimento de tRNA apoiaram o mesmo princípio: o melhor uso de códons depende de quanto benefício um gene oferece e de quanto custo de tradução ele impõe.
Pistas a partir de genomas naturais
Para verificar se esse trade-off se reflete na evolução, os autores examinaram milhares de genes de bactérias, leveduras, moscas-das-frutas e humanos. Para genes mais importantes à sobrevivência — estimados a partir do quanto o crescimento sofre quando são deletados — o uso natural de códons tende a casar mais de perto com o pool de tRNA, especialmente entre genes altamente expressos. Ao mesmo tempo, entre os genes mais altamente expressos, padrões de códons com um casamento perfeitamente ajustado são, na verdade, menos comuns; em vez disso, esses genes retêm um descompasso moderado, consistente com a evitação de custo excessivo de tradução. Experimentos de acumulação de mutações e medições precisas de fitness de mutações sinônimas individuais em levedura mostraram ainda que tanto aumentar quanto diminuir o descompasso frequentemente é prejudicial, o que implica que a evolução mantém o uso de códons próximo de um ótimo intermediário em vez de empurrar indefinidamente rumo a um casamento perfeito.
Por que um pouco de imperfeição ajuda
Para um público não especialista, a mensagem principal é que existe algo como “excesso de otimização” quando se trata da ortografia dos genes. Um casamento perfeito entre códons e as ferramentas de tradução da célula pode fazer com que certos genes monopolizem a maquinaria compartilhada, deixando os outros sem recursos e retardando o crescimento global. A evolução parece, em vez disso, favorecer um descompasso controlado e leve que entrega proteína suficiente dos genes importantes sem sobrecarregar o sistema. Essa percepção não apenas muda nossa visão sobre mutações supostamente “silenciosas”, como também oferece orientação prática para projetar genes mais seguros e eficientes na biotecnologia e na medicina.
Citação: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Palavras-chave: viés de uso de códons, suprimento de tRNA, mutações sinônimas, tradução de proteínas, resistência a antibióticos