Clear Sky Science · nl
Een kleine mismatch tussen het codongebruik van een gen en de cellulaire tRNA‑voorraad is voordelig
Wanneer “stille” DNA‑keuzes niet zo stil zijn
Onze genen bevatten veel manieren om dezelfde instructie te schrijven, met verschillende drieletterige DNA‑“woorden” die allemaal hetzelfde aminozuur betekenen. Decennialang werden deze alternatieve spellen — synonieme codons genoemd — als grotendeels triviale details beschouwd. Deze studie kantelt dat beeld. Ze laat zien dat hoe nauw het “accent” van het codongebruik van een gen aansluit bij de vertaalmachinerie van de cel het verschil kan maken tussen traag groeien en goed gedijen, en dat een kleine mismatch juist voordelig kan zijn.
Hoe cellen genetische instructies lezen
Om genen om te zetten in eiwitten gebruiken cellen kleine adaptormoleculen genaamd tRNAs die codons op boodschapper‑RNA herkennen en de juiste aminozuren aanleveren. Elk aminozuur (met twee uitzonderingen) heeft meerdere mogelijke codons, maar cellen gebruiken die niet gelijkmatig. In de loop van de evolutie ontwikkelt een organisme een kenmerkend patroon van codongebruik en vult het zijn tRNA‑voorraad daarop af. De traditionele opvatting gaat uit van een ideaalplaatje: dat codons in genen de beschikbare tRNAs spiegelen, wat zorgt voor snelle, nauwkeurige translatie. Afwijkingen van die perfecte match werden gezien als het gevolg van toeval of mutatie, niet als iets nuttigs.
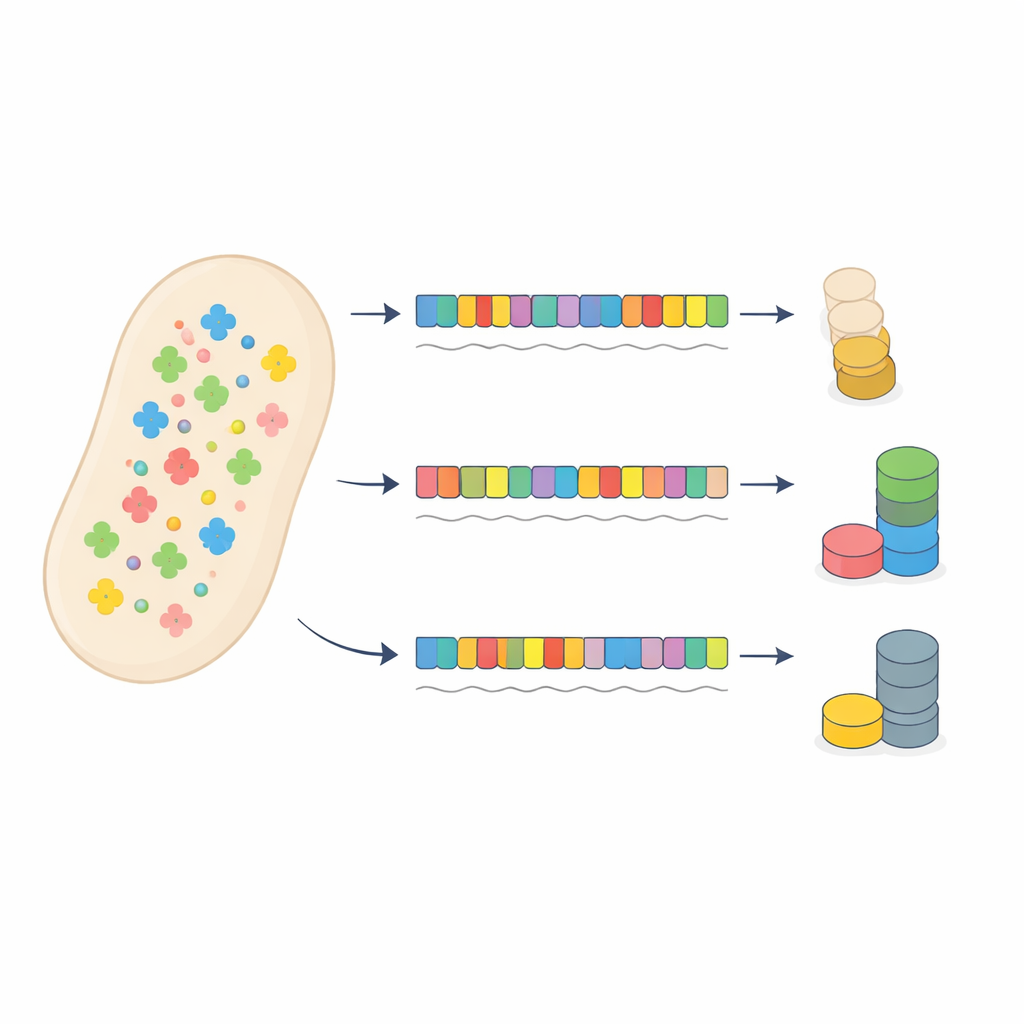
Een proef met antibioticaresistentie
De auteurs daagden dit conventionele beeld uit door een gen voor antibioticaresistentie in bacteriën nauwkeurig te herontwerpen. Ze maakten 53 versies van een gentamicine‑resistentiegen die allemaal hetzelfde eiwit codeerden maar verschillende patronen van synonieme codons gebruikten, variërend van bijna perfecte aansluiting op de tRNA‑voorraad van de cel tot een sterke mismatch. Elke versie werd op een plasmide geplaatst en gefuseerd met een fluorescent merkteken zodat eiwitproductie gemeten kon worden. Een tweede fluorescerend eiwit op hetzelfde plasmide fungeerde als sensor voor hoe zwaar het translatesysteem in zijn geheel werkte, omdat intensief tRNA‑gebruik door het resistentiegen de translatie van andere eiwitten zou vertragen.
Het vinden van het optimale punt voor groei
Wanneer deze gemodificeerde bacteriën groeiden in medium met gentamicine, produceerden genen waarvan de codons extreem goed bij de tRNA‑voorraad pasten de meeste resistentie‑eiwitten — maar ze legden ook de grootste belasting op de translatieapparatuur van de cel. Bacteriën met zulke “over‑geoptimaliseerde” genen groeiden trager dan die met een bescheiden mismatch. Met andere woorden: hoewel betere aansluiting het voordeel van het resistentieeiwit verhoogde, bracht het ook hogere kosten met zich mee door gebruik van gedeelde vertaalmiddelen, en voorbij een bepaald punt domineerde die kost. Het snelst groeiende materiaal had genversies met een kleine, niet minimale, mismatch met de tRNA‑voorraad, wat aangeeft dat het echte optimum afweging maakt tussen opbrengst en kosten in plaats van één van beide te maximaliseren.
Wanneer de belangrijkheid van een gen verandert, verandert ook het optimum
Het team varieerde daarna hoe cruciaal het resistentiegen was door de antibiotica‑dosis aan te passen. Bij lage gentamicineniveaus was het voordeel van het eiwit voor overleving beperkt, en presteerden codonpatronen met een relatief grote mismatch het best, omdat dit verspillingvolle belasting van het translatesysteem verminderde. Naarmate de antibioticaconcentratie steeg en het gen belangrijker werd, verschoof het optimale codonpatroon naar een nauwere aansluiting op de tRNA‑voorraad, en bij zeer hoge doses was de bijna perfecte match het beste. Vergelijkbare experimenten met een tweede resistentiegen en met directe aanpassing van de tRNA‑voorraad ondersteunden hetzelfde principe: het beste codongebruik hangt af van hoeveel voordeel een gen levert en hoeveel vertaal‑kost het oplegt.
Sporen in natuurlijke genomen
Om te onderzoeken of deze afweging in de evolutie terug te zien is, bekeken de auteurs duizenden genen van bacteriën, gist, fruitvlieg en mensen. Voor genen die belangrijker zijn voor overleving — geschat uit hoeveel groei afneemt wanneer ze worden verwijderd — neigt het natuurlijke codongebruik ernaar de tRNA‑voorraad nauwer te benaderen, vooral bij sterk geëxprimeerde genen. Tegelijkertijd zijn onder de hoogst geëxprimeerde genen patronen met een volledig perfecte match juist minder gebruikelijk; in plaats daarvan behouden deze genen een bescheiden mismatch, wat overeenkomt met het vermijden van overmatige vertaalkosten. Mutatie‑accumulatieexperimenten en precieze fitheidsmetingen van individuele synonieme mutaties in gist toonden verder aan dat zowel het vergroten als het verkleinen van de mismatch vaak schadelijk is, wat impliceert dat evolutie codongebruik bij een tussenliggend optimum houdt in plaats van eindeloos naar een perfecte match te duwen.
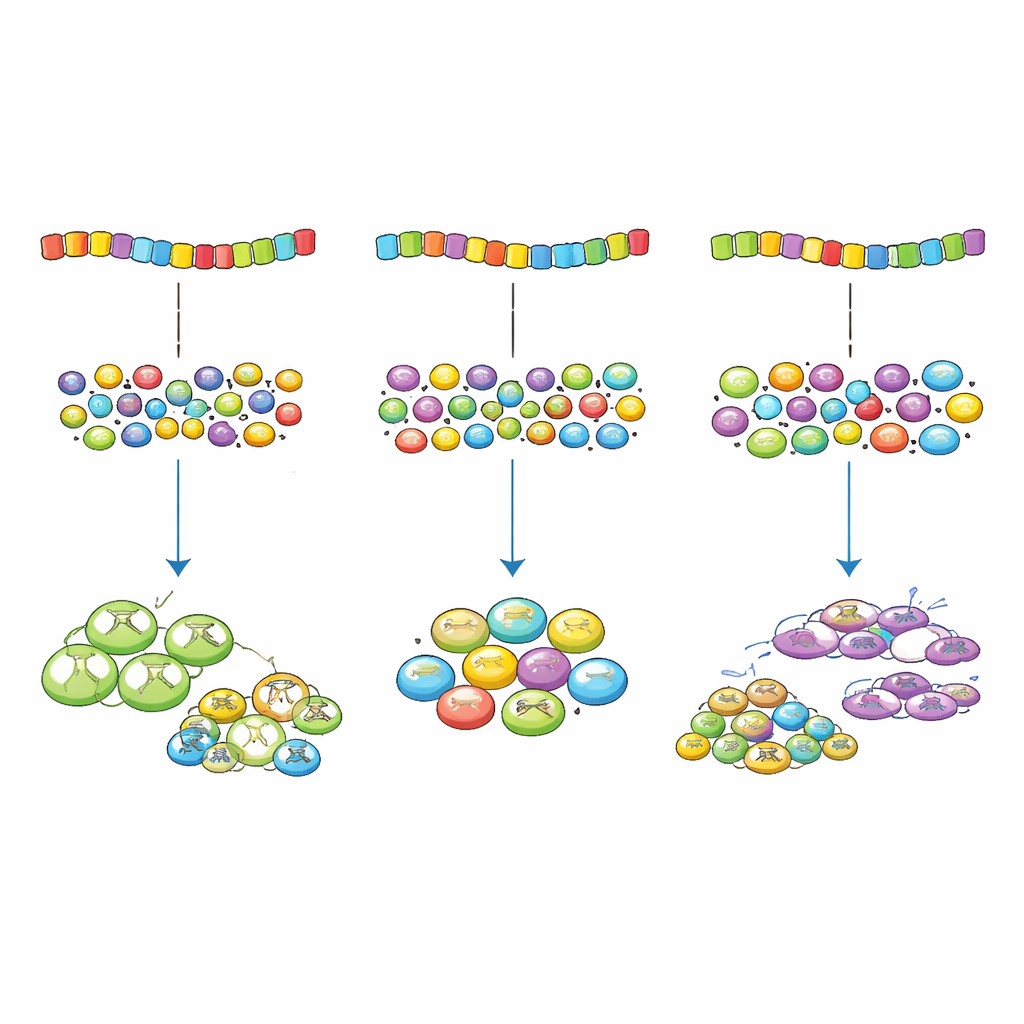
Waarom een beetje imperfectie helpt
Voor niet‑specialisten is de kernboodschap dat er zoiets bestaat als “te geoptimaliseerd” als het om genspellingswijze gaat. Een perfecte match tussen codons en de vertaaltuigen van de cel kan ertoe leiden dat bepaalde genen het gedeelde apparaat domineren, waardoor andere genen tekortkomen en de algehele groei vertraagt. De evolutie lijkt in plaats daarvan een gecontroleerde, lichte mismatch te bevoordelen die genoeg eiwit levert van belangrijke genen zonder het systeem te overbelasten. Dit inzicht verandert niet alleen onze kijk op zogenaamd “stille” mutaties, maar geeft ook praktisch houvast bij het ontwerpen van veiligere en efficiëntere genen in biotechnologie en geneeskunde.
Bronvermelding: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Trefwoorden: codongebruik‑bias, tRNA‑voorraad, synonieme mutaties, eiwitsynthese, antibioticaresistentie