Clear Sky Science · es
Una ligera descoordinación entre el uso de codones de un gen y el suministro celular de ARNt es beneficiosa
Cuando las decisiones “silenciosas” en el ADN no son tan silenciosas
Nuestros genes contienen muchas maneras de escribir la misma instrucción, usando diferentes “palabras” de tres letras en el ADN que todas significan el mismo aminoácido. Durante décadas, estas alternativas—llamadas codones sinónimos—se consideraron en gran medida detalles triviales. Este estudio trastoca esa visión. Muestra que cuán estrechamente el “acento” de codones de un gen coincide con la maquinaria de traducción de la célula puede marcar la diferencia entre un crecimiento lento y uno próspero, y que una ligera descoordinación puede ser, en realidad, lo mejor.
Cómo las células leen las instrucciones genéticas
Para convertir genes en proteínas, las células usan pequeñas moléculas adaptadoras llamadas ARNt que reconocen codones en el ARN mensajero y entregan los aminoácidos correctos. Cada aminoácido (con dos excepciones) tiene varios codones posibles, pero las células no los usan por igual. A lo largo de la evolución, los organismos desarrollan un patrón característico de uso de codones y ajustan su reserva de ARNt en consecuencia. La visión tradicional asume que la situación ideal es una coincidencia perfecta: los codones empleados en los genes reflejan los ARNt disponibles, lo que permite una traducción rápida y precisa. Cualquier desviación de esa coincidencia perfecta se pensaba que persistía solo por deriva genética aleatoria y mutación, no porque fuera útil.
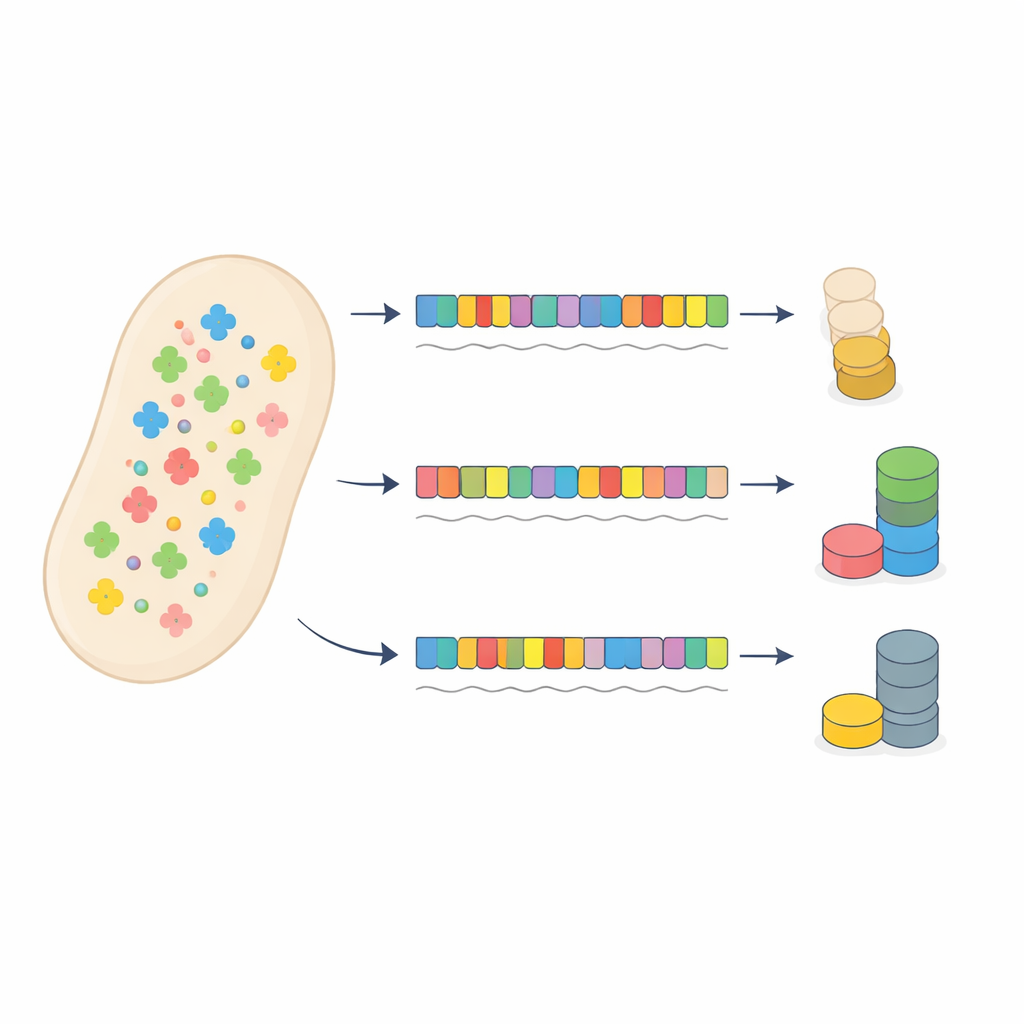
Un caso de prueba con resistencia a antibióticos
Los autores desafiaron este panorama convencional rediseñando cuidadosamente un gen de resistencia a antibióticos en bacterias. Crearon 53 versiones de un gen de resistencia a la gentamicina que codificaban la misma proteína pero usaban distintos patrones de codones sinónimos, que iban desde una coincidencia casi perfecta con la reserva de ARNt de la célula hasta una fuerte descoordinación. Cada versión se colocó en un plásmido y se fusionó a un marcador fluorescente para poder medir la producción de proteína. Una segunda proteína fluorescente en el mismo plásmido actuó como sensor de la carga total sobre el sistema de traducción, porque el uso intensivo de ARNt por el gen de resistencia ralentizaría la traducción de otras proteínas.
Encontrar el punto óptimo para el crecimiento
Cuando estas bacterias modificadas crecieron en medio con gentamicina, los genes cuyos codones coincidían extremadamente bien con la reserva de ARNt produjeron la mayor cantidad de proteína de resistencia, pero también impusieron la mayor carga sobre la maquinaria de traducción de la célula. Las bacterias que portaban dichos genes “sobreoptimizados” crecieron más despacio que aquellas con una descoordinación moderada. En otras palabras, aunque una mejor coincidencia aumentaba el beneficio de la proteína de resistencia, también elevaba el costo de usar recursos de traducción compartidos, y más allá de cierto punto el costo predominaba. Las células que crecieron más rápido fueron las cuyas versiones del gen mostraban una pequeña, no mínima, descoordinación con el suministro de ARNt, lo que indica que el verdadero óptimo equilibra beneficio y coste en lugar de maximizar uno solo.
Cuando cambia la importancia del gen, también cambia el óptimo
El equipo varió luego cuán crucial era el gen de resistencia cambiando la dosis del antibiótico. A niveles bajos de gentamicina, el beneficio de la proteína para la supervivencia era modesto, y los patrones de codones con mejor rendimiento mostraban una descoordinación relativamente grande, lo que reducía la presión innecesaria sobre el sistema de traducción. A medida que aumentó la concentración del antibiótico y el gen se volvió más importante, el patrón óptimo de codones se desplazó hacia una coincidencia más estrecha con la reserva de ARNt, y a dosis muy altas la coincidencia casi perfecta fue la mejor. Experimentos similares con un segundo gen de resistencia y con la alteración directa del suministro de ARNt respaldaron el mismo principio: el mejor uso de codones depende de cuánto beneficio aporta un gen y del coste que impone a la traducción.
Pistas en genomas naturales
Para ver si este compromiso se refleja en la evolución, los autores examinaron miles de genes de bacterias, levaduras, moscas de la fruta y humanos. Para los genes que importan más para la supervivencia—estimado por cuánto se ve afectado el crecimiento cuando se eliminan—el uso natural de codones tiende a coincidir más estrechamente con la reserva de ARNt, especialmente entre los genes altamente expresados. Al mismo tiempo, entre los genes de mayor expresión, los patrones de codones con una coincidencia perfectamente ajustada son en realidad menos comunes; en su lugar, estos genes conservan una descoordinación moderada, coherente con evitar un coste excesivo de traducción. Experimentos de acumulación de mutaciones y medidas precisas de la aptitud de mutaciones sinónimas individuales en levadura mostraron además que tanto aumentar como disminuir la descoordinación suele ser perjudicial, lo que implica que la evolución mantiene el uso de codones cerca de un óptimo intermedio en lugar de empujar indefinidamente hacia una coincidencia perfecta.
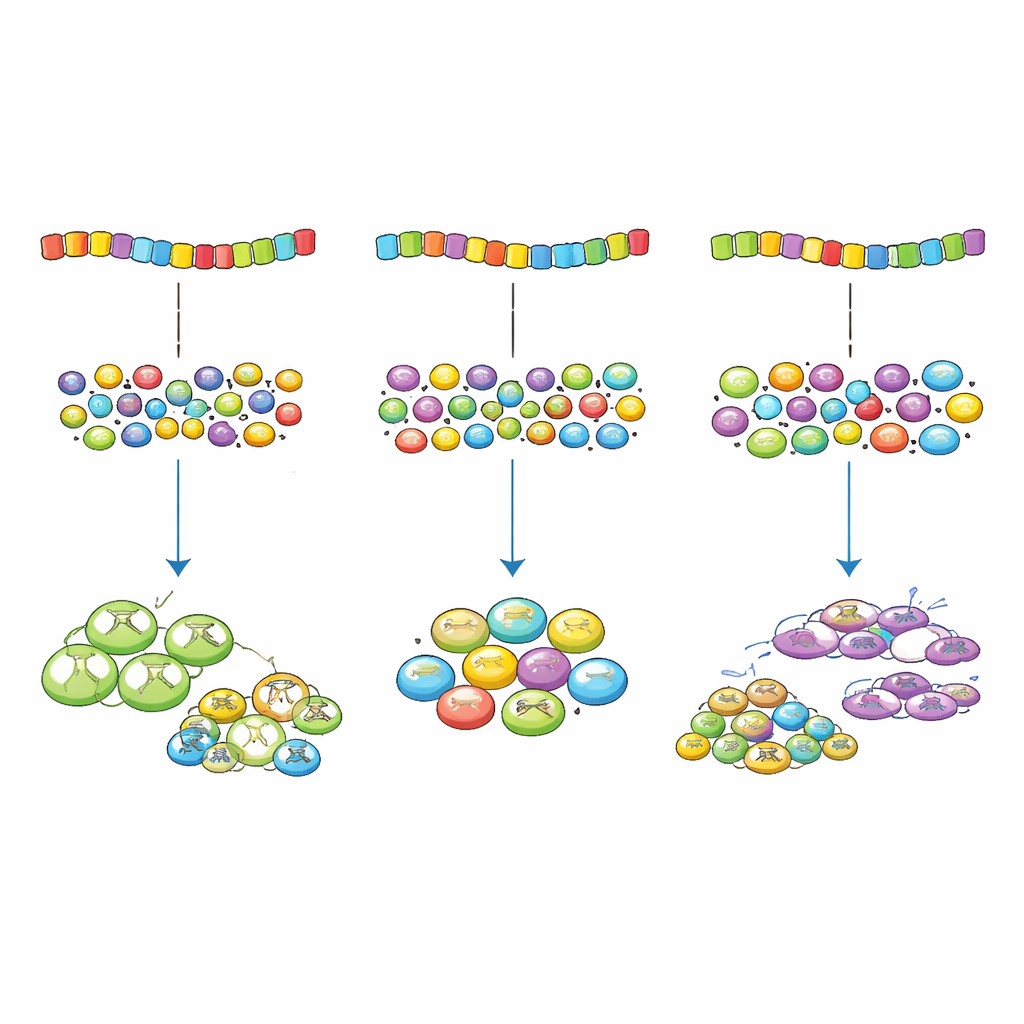
Por qué ayuda un poco de imperfección
Para un público no especializado, el mensaje clave es que existe algo así como “demasiado optimizado” cuando se trata de la ortografía genética. Una coincidencia perfecta entre codones y las herramientas de traducción de la célula puede hacer que ciertos genes acaparen la maquinaria compartida, dejando sin recursos a otros y ralentizando el crecimiento general. La evolución, en cambio, parece favorecer una descoordinación controlada y ligera que suministra suficiente proteína desde genes importantes sin sobrecargar el sistema. Esta idea no solo cambia nuestra forma de pensar sobre las mutaciones supuestamente “silenciosas”, sino que también ofrece orientación práctica para diseñar genes más seguros y eficientes en biotecnología y medicina.
Cita: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Palabras clave: sesgo en el uso de codones, suministro de ARNt, mutaciones sinónimas, traducción de proteínas, resistencia a antibióticos