Clear Sky Science · fr
Un léger décalage entre l’utilisation des codons d’un gène et l’offre en ARNt cellulaires est bénéfique
Quand des choix « silencieux » de l’ADN ne sont pas si silencieux
Nos gènes offrent souvent plusieurs manières d’écrire la même instruction, en utilisant différents « mots » d’ADN de trois lettres qui correspondent au même acide aminé. Pendant des décennies, ces orthographes alternatives — appelées codons synonymes — ont été considérées comme des détails pour l’essentiel négligeables. Cette étude renverse cette vision. Elle montre que la proximité entre « l’accent » en codons d’un gène et la machinerie de traduction de la cellule peut faire la différence entre une croissance ralentie et une prospérité, et qu’un léger décalage peut en réalité être optimal.
Comment les cellules lisent les instructions génétiques
Pour convertir les gènes en protéines, les cellules utilisent de petits adaptateurs appelés ARNt qui reconnaissent les codons sur l’ARN messager et apportent les acides aminés appropriés. Chaque acide aminé (à deux exceptions près) dispose de plusieurs codons possibles, mais les cellules ne les utilisent pas de manière égale. Au fil de l’évolution, les organismes développent un schéma caractéristique d’utilisation des codons et ajustent en conséquence leur pool d’ARNt. La vision traditionnelle suppose que la situation idéale est une correspondance parfaite : les codons employés dans les gènes reflètent les ARNt disponibles, assurant une traduction rapide et précise. Tout écart par rapport à cette concordance parfaite était pensé persister principalement du fait de la dérive génétique et des mutations aléatoires, et non parce qu’il serait utile.
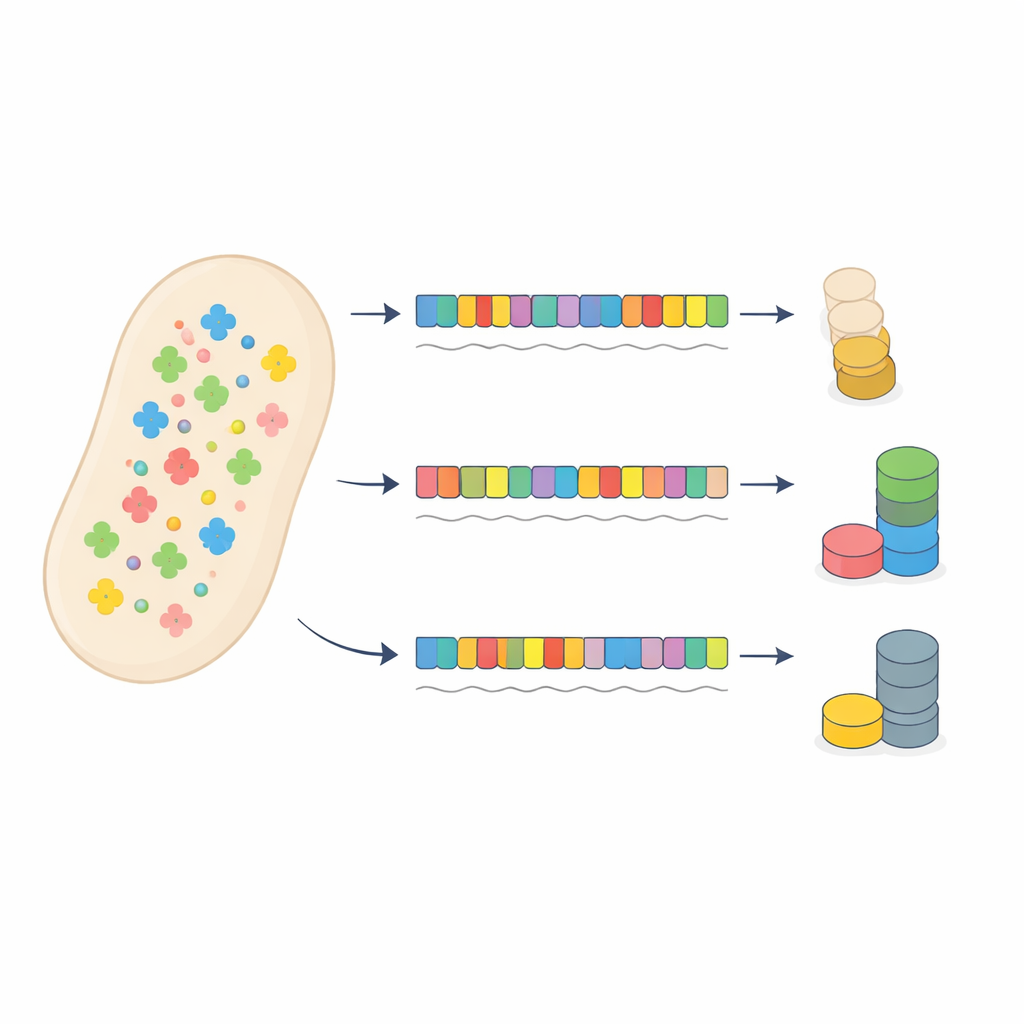
Un cas test utilisant la résistance aux antibiotiques
Les auteurs ont remis en question ce tableau conventionnel en redessinant soigneusement un gène de résistance aux antibiotiques chez des bactéries. Ils ont créé 53 versions d’un gène de résistance à la gentamicine codant toutes la même protéine mais utilisant des motifs différents de codons synonymes, allant d’une correspondance quasi parfaite avec le pool d’ARNt de la cellule à un fort décalage. Chaque version a été insérée sur un plasmide et fusionnée à un marqueur fluorescent pour pouvoir mesurer la production protéique. Une deuxième protéine fluorescente sur le même plasmide servait de capteur de la charge globale du système de traduction, car l’utilisation intensive des ARNt par le gène de résistance ralentirait la traduction d’autres protéines.
Trouver le point d’équilibre pour la croissance
Lorsque ces bactéries modifiées ont été cultivées dans un milieu contenant de la gentamicine, les gènes dont les codons correspondaient très bien au pool d’ARNt produisaient le plus de protéine de résistance — mais ils imposaient aussi la plus lourde charge à la machinerie de traduction de la cellule. Les bactéries porteuses de tels gènes « sur-optimisés » croissaient plus lentement que celles présentant un léger décalage. Autrement dit, si une meilleure correspondance augmentait l’avantage procuré par la protéine de résistance, elle augmentait aussi le coût d’utilisation de ressources de traduction partagées, et au-delà d’un certain point le coût l’emportait. Les cellules à la croissance la plus rapide étaient celles dont les versions du gène présentaient un petit, et non minimal, décalage avec l’offre en ARNt, indiquant que l’optimum réel équilibre gain et coût plutôt que de maximiser l’un ou l’autre isolément.
Quand l’importance d’un gène change, l’optimum change aussi
L’équipe a ensuite fait varier l’importance du gène de résistance en modifiant la dose d’antibiotique. À faibles niveaux de gentamicine, le bénéfice de la protéine pour la survie était limité, et les motifs de codons les plus performants présentaient un décalage relativement marqué, ce qui réduisait la surcharge inutile du système de traduction. À mesure que la concentration d’antibiotique augmentait et que le gène devenait plus crucial, le motif de codons optimal se rapprochait du pool d’ARNt, et à des doses très élevées la correspondance quasi parfaite donnait les meilleurs résultats. Des expériences similaires avec un second gène de résistance et en modulant directement l’offre en ARNt ont soutenu le même principe : l’utilisation de codons optimale dépend de l’importance du gène et du coût qu’il impose en traduction.
Indices tirés des génomes naturels
Pour savoir si ce compromis se reflète dans l’évolution, les auteurs ont examiné des milliers de gènes de bactéries, de levures, de drosophiles et d’humains. Pour les gènes ayant une plus grande importance pour la survie — évaluée par l’impact sur la croissance lorsqu’ils sont supprimés — l’utilisation naturelle des codons tend à mieux correspondre au pool d’ARNt, en particulier parmi les gènes fortement exprimés. En même temps, parmi les gènes les plus exprimés, les motifs de codons avec une correspondance parfaitement serrée sont en fait moins fréquents ; ces gènes conservent plutôt un léger décalage, compatible avec l’évitement d’un coût excessif en traduction. Des expériences d’accumulation de mutations et des mesures précises de fitness de mutations synonymes individuelles chez la levure ont en outre montré que l’augmentation comme la diminution du décalage sont souvent délétères, ce qui laisse penser que l’évolution maintient l’utilisation des codons près d’un optimum intermédiaire plutôt que de tendre sans cesse vers une correspondance parfaite.
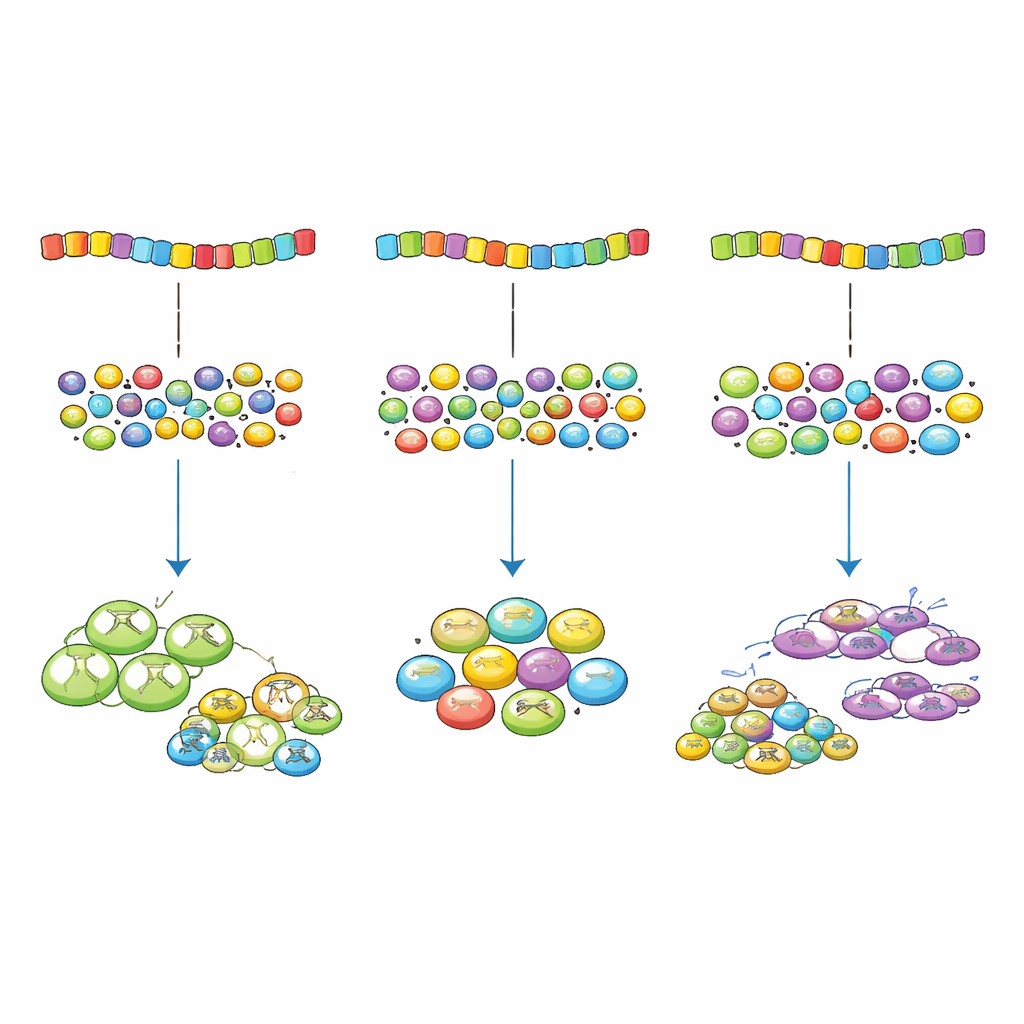
Pourquoi un peu d’imperfection aide
Pour un non-spécialiste, le message clé est qu’il existe une notion de « trop optimisé » en matière d’orthographe génétique. Une correspondance parfaite entre les codons et les outils de traduction de la cellule peut amener certains gènes à monopoliser la machinerie partagée, privant les autres et ralentissant la croissance globale. L’évolution semble plutôt favoriser un léger décalage contrôlé qui fournit suffisamment de protéine provenant des gènes importants sans surcharger le système. Cette perspective modifie non seulement notre manière d’envisager les mutations soi-disant « silencieuses », mais offre aussi des indications pratiques pour concevoir des gènes plus sûrs et plus efficaces en biotechnologie et en médecine.
Citation: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Mots-clés: biais d’utilisation des codons, offre en ARNt, mutations synonymes, traduction protéique, résistance aux antibiotiques