Clear Sky Science · de
Eine leichte Unstimmigkeit zwischen dem Codon‑Gebrauch eines Gens und dem zellulären tRNA‑Angebot ist vorteilhaft
Wenn „stille“ DNA‑Entscheidungen nicht so still sind
Unsere Gene bieten oft mehrere Möglichkeiten, dieselbe Anweisung zu schreiben, indem unterschiedliche drei‑letterige DNA‑„Wörter“ verwendet werden, die alle dieselbe Aminosäure bedeuten. Jahrzehntelang galten diese alternativen Schreibweisen – sogenannte synonyme Codons – weitgehend als nebensächlich. Diese Studie stellt diese Sichtweise in Frage. Sie zeigt, dass die Frage, wie sehr das „Akzent“ eines Gens in seiner Codon‑Verwendung mit der zellulären Übersetzungsmaschinerie übereinstimmt, über langsamwüchsiges oder florierendes Wachstum entscheiden kann – und dass eine leichte Unstimmigkeit tatsächlich am vorteilhaftesten sein kann.
Wie Zellen genetische Anweisungen lesen
Um Gene in Proteine zu verwandeln, nutzen Zellen kleine Adaptermoleküle, die tRNAs, die Codons auf der Boten‑RNA erkennen und die richtigen Aminosäuren liefern. Jede Aminosäure (mit zwei Ausnahmen) hat mehrere mögliche Codons, aber die Zellen verwenden sie nicht gleichmäßig. Im Verlauf der Evolution entwickelt ein Organismus ein charakteristisches Muster der Codon‑Verwendung und richtet seinen tRNA‑Vorrat entsprechend ein. Die traditionelle Ansicht nimmt an, dass die ideale Situation ein perfektes Matching ist: in Genen verwendete Codons spiegeln die verfügbaren tRNAs wider und ermöglichen schnelle, genaue Translation. Jede Abweichung von diesem perfekten Abgleich galt bisher als Folge von reinem genetischem Drift und Mutation, nicht als vorteilhaft.
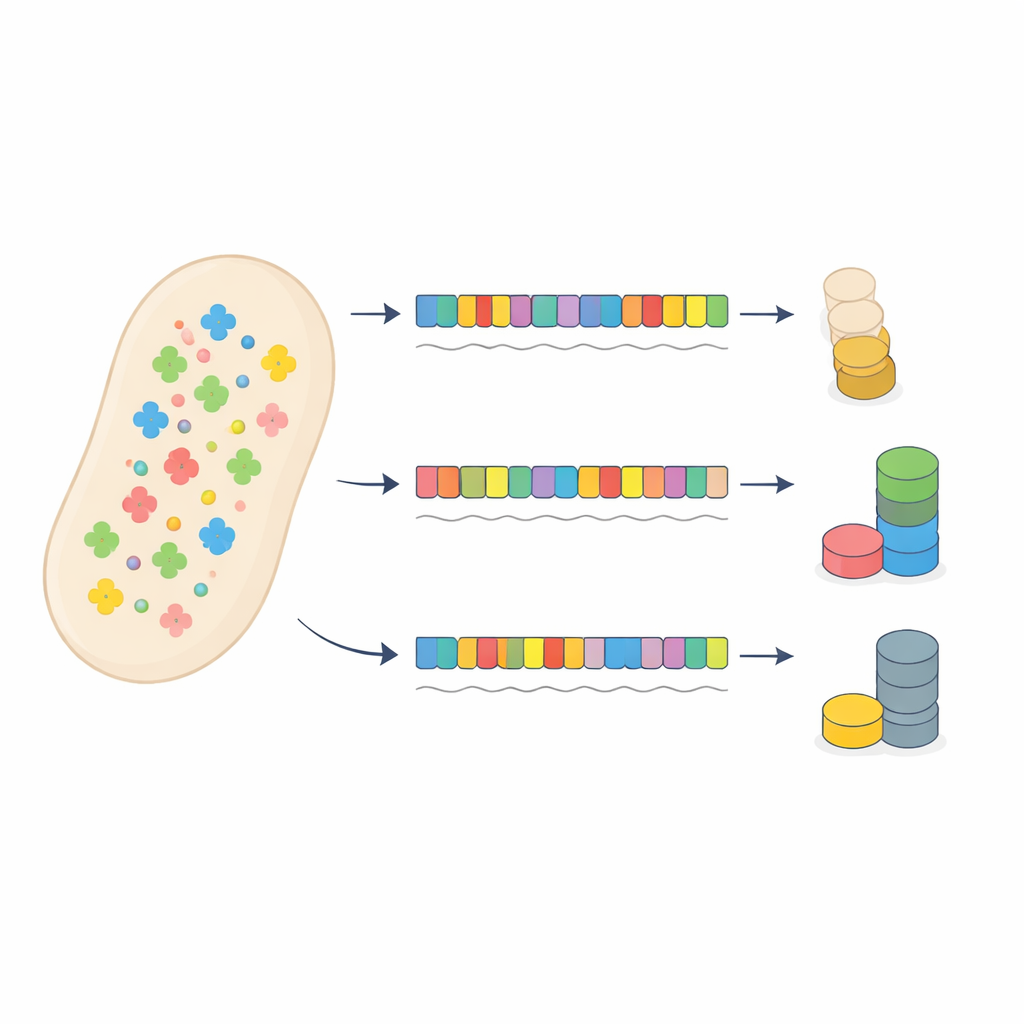
Ein Testfall mit Antibiotikaresistenz
Die Autoren stellten dieses konventionelle Bild infrage, indem sie ein Antibiotikaresistenzgen in Bakterien sorgfältig neu entwarfen. Sie erzeugten 53 Versionen eines Gentamicin‑Resistenzgens, die alle dasselbe Protein kodierten, aber unterschiedliche Muster synonymen Codongebrauchs verwendeten, von nahezu perfekter Übereinstimmung mit dem tRNA‑Vorrat der Zelle bis zu starker Unstimmigkeit. Jede Version wurde auf einem Plasmid platziert und mit einem fluoreszierenden Marker fusioniert, sodass die Proteinausbeute gemessen werden konnte. Ein zweites fluoreszierendes Protein auf demselben Plasmid diente als Sensor dafür, wie stark das Translationssystem insgesamt belastet war, denn intensive Nutzung der tRNAs durch das Resistenzgen würde die Translation anderer Proteine verlangsamen.
Das Optimum für Wachstum finden
Als diese gentechnisch veränderten Bakterien in einem Medium mit Gentamicin kultiviert wurden, produzierten Gene, deren Codons dem tRNA‑Vorrat extrem gut entsprachen, am meisten Resistenzprotein – sie belasteten aber auch die zelluläre Translationsmaschinerie am stärksten. Bakterien mit solchen „überoptimierten“ Genen wuchsen langsamer als solche mit einer moderaten Unstimmigkeit. Anders gesagt: Zwar erhöhte besseres Matching den Nutzen des Resistenzproteins, zugleich stieg aber auch die Kosten durch die Nutzung gemeinsamer Translationsressourcen, und ab einem gewissen Punkt überwog der Kostenfaktor. Am schnellsten wuchsen Zellen, deren Genvarianten eine kleine, nicht minimale Unstimmigkeit zum tRNA‑Angebot zeigten, was darauf hinweist, dass das wirkliche Optimum Gewinn und Kosten ausbalanciert anstatt eines von beiden zu maximieren.
Wenn sich die Wichtigkeit eines Gens ändert, ändert sich auch das Optimum
Das Team variierte dann, wie entscheidend das Resistenzgen war, indem es die Antibiotikadosis änderte. Bei niedrigen Gentamicin‑Spiegeln war der Überlebensvorteil des Proteins gering, und die leistungsstärksten Codonmuster wiesen eine relativ große Unstimmigkeit auf, was die Verschwendung durch Belastung des Translationssystems verringerte. Mit steigender Antibiotikakonzentration und wachsender Bedeutung des Gens verschob sich das optimale Codonmuster in Richtung engerer Übereinstimmung mit dem tRNA‑Vorrat, und bei sehr hohen Dosen schnitt die nahezu perfekte Übereinstimmung am besten ab. Ähnliche Experimente mit einem zweiten Resistenzgen und durch direkte Veränderung des tRNA‑Angebots stützten denselben Grundsatz: Die optimale Codonverwendung hängt davon ab, wie viel Nutzen ein Gen bringt und welche Translationskosten es verursacht.
Hinweise aus natürlichen Genomen
Um zu prüfen, ob dieser Zielkonflikt sich in der Evolution widerspiegelt, untersuchten die Autoren Tausende von Genen aus Bakterien, Hefen, Fruchtfliegen und Menschen. Bei Genen, die für das Überleben wichtiger sind – abgeschätzt anhand dessen, wie sehr das Wachstum leidet, wenn sie gelöscht werden – tendiert die natürliche Codonverwendung dazu, dem tRNA‑Vorrat enger zu entsprechen, besonders bei stark exprimierten Genen. Gleichzeitig sind bei den am höchsten exprimierten Genen Muster mit perfekter Übereinstimmung tatsächlich seltener; stattdessen behalten diese Gene eine moderate Unstimmigkeit bei, was mit dem Vermeiden übermäßiger Translationskosten übereinstimmt. Mutationsakkumulations‑Experimente und präzise Fitnessmessungen einzelner synonymen Mutationen in Hefe zeigten weiter, dass sowohl eine Verkleinerung als auch eine Vergrößerung der Unstimmigkeit oft schädlich ist, was nahelegt, dass die Evolution die Codonverwendung in der Nähe eines intermediären Optimums erhält, statt unablässig auf eine perfekte Übereinstimmung zuzusteuern.
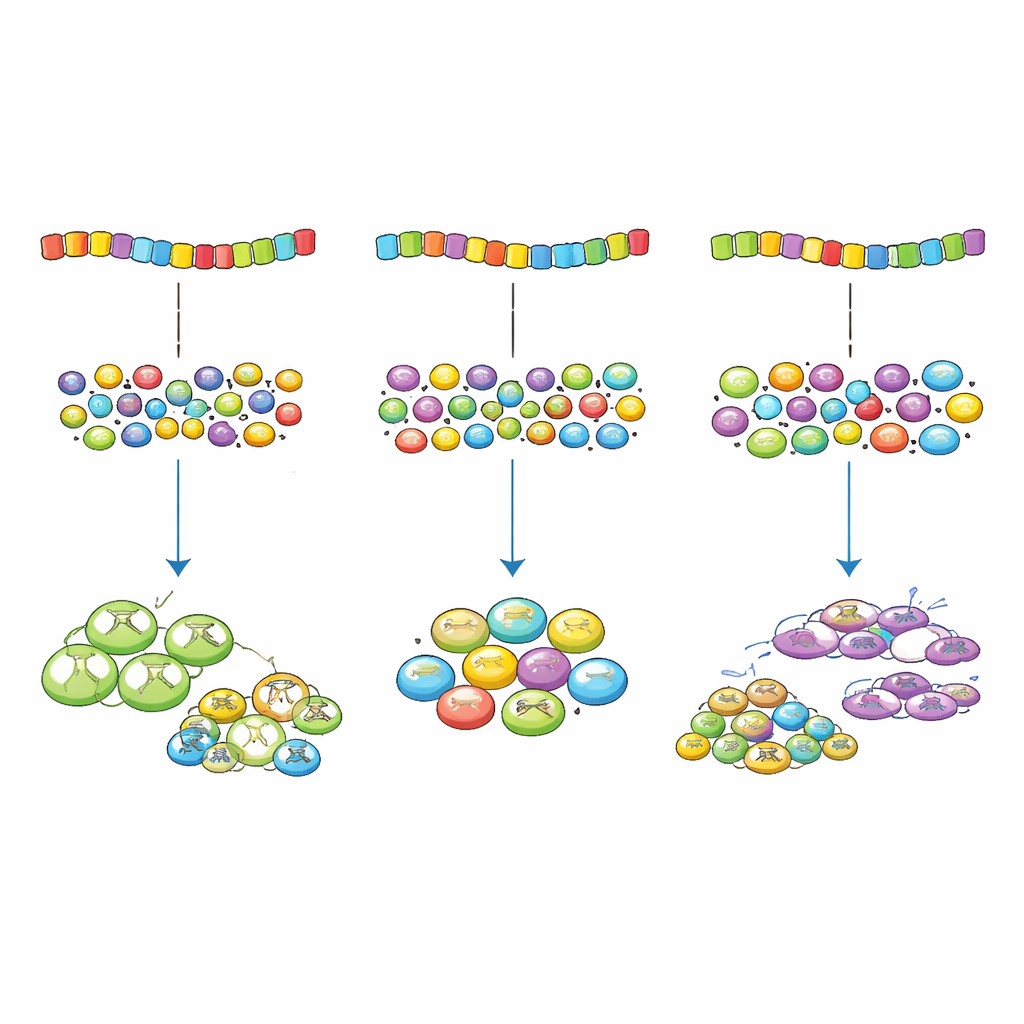
Warum eine kleine Imperfektion nützt
Für Nichtfachleute lautet die Kernbotschaft: Es gibt so etwas wie „zu optimiert“ bei der Gen‑Schreibung. Eine perfekte Übereinstimmung zwischen Codons und den zellulären Translationswerkzeugen kann dazu führen, dass bestimmte Gene die gemeinsame Maschinerie dominieren, andere dadurch auszehren und das Gesamtwachstum verlangsamen. Stattdessen scheint die Evolution eine kontrollierte, leichte Unstimmigkeit zu bevorzugen, die genug Protein von wichtigen Genen liefert, ohne das System zu überlasten. Diese Einsicht verändert nicht nur unser Verständnis vermeintlich „stiller“ Mutationen, sondern liefert auch praktische Hinweise für das sicherere und effizientere Design von Genen in Biotechnologie und Medizin.
Zitation: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Schlüsselwörter: Codon‑Nutzungsbias, tRNA‑Angebot, synonyme Mutationen, Proteintranslation, Antibiotikaresistenz