Clear Sky Science · it
Un leggero disallineamento tra l’uso dei codoni di un gene e la disponibilità di tRNA cellulare è vantaggioso
Quando le scelte “silenziose” del DNA non sono così silenziose
I nostri geni contengono molteplici modi per scrivere la stessa istruzione, usando diverse “parole” del DNA di tre lettere che indicano lo stesso amminoacido. Per decenni queste grafie alternative—chiamate codoni sinonimi—sono state considerate in gran parte dettagli trascurabili. Questo studio ribalta quella visione. Mostra che quanto l’“accento” dei codoni di un gene si allinea con la macchina di traduzione della cellula può fare la differenza tra crescita lenta e prosperità, e che un lieve disallineamento può in realtà risultare ottimale.
Come le cellule leggono le istruzioni genetiche
Per trasformare i geni in proteine, le cellule usano piccoli adattatori chiamati tRNA che riconoscono i codoni sull’RNA messaggero e consegnano gli amminoacidi corretti. Ogni amminoacido (con due eccezioni) ha diversi codoni possibili, ma le cellule non li usano in modo uguale. Nel corso dell’evoluzione, gli organismi sviluppano uno schema caratteristico di uso dei codoni e regolano di conseguenza la dotazione del loro pool di tRNA. La visione tradizionale assume che la situazione ideale sia una corrispondenza perfetta: i codoni usati nei geni rispecchiano i tRNA disponibili, garantendo una traduzione rapida e accurata. Qualsiasi deviazione da questa corrispondenza perfetta si pensava persistesse solo per deriva genetica casuale e mutazioni, non perché fosse utile.
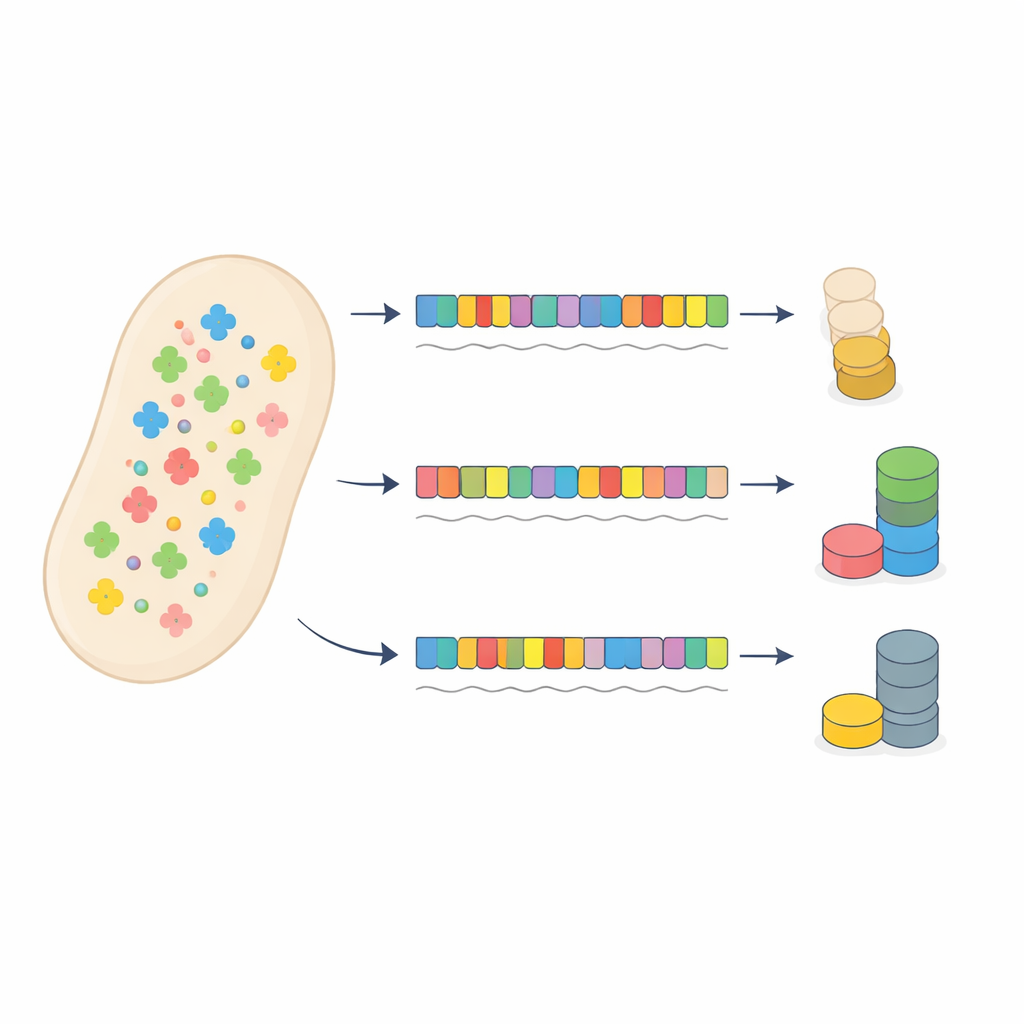
Un caso di prova usando la resistenza agli antibiotici
Gli autori hanno messo in discussione questo quadro convenzionale riprogettando con cura un gene di resistenza agli antibiotici nei batteri. Hanno creato 53 versioni di un gene di resistenza alla gentamicina che codificavano tutte la stessa proteina ma usavano pattern diversi di codoni sinonimi, variando da un quasi perfetto allineamento col pool di tRNA della cellula a un forte disallineamento. Ogni versione è stata inserita su un plasmide e fusa a un marcatore fluorescente in modo da poter misurare la produzione proteica. Una seconda proteina fluorescente sullo stesso plasmide fungeva da sensore del carico complessivo sul sistema di traduzione, perché l’uso intensivo di tRNA da parte del gene di resistenza avrebbe rallentato la traduzione di altre proteine.
Trovare il punto ottimale per la crescita
Quando questi batteri ingegnerizzati sono cresciuti in un terreno contenente gentamicina, i geni i cui codoni corrispondevano molto bene al pool di tRNA hanno prodotto la maggior quantità di proteina di resistenza—ma hanno anche imposto il carico maggiore sulla macchina di traduzione della cellula. I batteri che portavano tali geni “sovra-ottimizzati” crescevano più lentamente di quelli con un disallineamento moderato. In altre parole, mentre un migliore allineamento aumentava il beneficio della proteina di resistenza, aumentava anche il costo dell’uso di risorse di traduzione condivise, e oltre un certo punto il costo ha la meglio. Le cellule a crescita più rapida erano quelle le cui versioni geniche mostravano un piccolo, non minimo, disallineamento con la disponibilità di tRNA, indicando che il vero ottimo bilancia rendimento e costo invece di massimizzare uno dei due isolatamente.
Quando cambia l’importanza del gene, cambia anche l’ottimo
Il gruppo ha poi variato quanto fosse cruciale il gene di resistenza modificando la dose dell’antibiotico. A bassi livelli di gentamicina, il beneficio della proteina per la sopravvivenza era modesto, e i pattern di codoni migliori mostravano un disallineamento relativamente ampio, riducendo lo spreco e l’affaticamento del sistema di traduzione. Con l’aumentare della concentrazione dell’antibiotico e dell’importanza del gene, il pattern di codoni ottimale si è spostato verso un allineamento più stretto col pool di tRNA, e a dosi molto alte il quasi perfetto allineamento ha funzionato meglio. Esperimenti simili con un secondo gene di resistenza e modificando direttamente la fornitura di tRNA hanno supportato lo stesso principio: il miglior uso dei codoni dipende da quanto beneficio un gene fornisce e da quanto costo di traduzione impone.
Indizi dai genomi naturali
Per vedere se questo compromesso è riflesso dall’evoluzione, gli autori hanno esaminato migliaia di geni provenienti da batteri, lieviti, moscerini della frutta e esseri umani. Per i geni più importanti per la sopravvivenza—stimati da quanto la crescita ne risente quando vengono eliminati—l’uso naturale dei codoni tende a corrispondere più strettamente al pool di tRNA, in particolare tra i geni altamente espressi. Allo stesso tempo, tra i geni più espressi, pattern di codoni con un allineamento perfetto sono in realtà meno comuni; invece, questi geni mantengono un disallineamento moderato, coerente con l’evitare costi di traduzione eccessivi. Esperimenti di accumulo di mutazioni e misurazioni precise della fitness di singole mutazioni sinonime nel lievito hanno inoltre mostrato che sia aumentare sia diminuire il disallineamento è spesso dannoso, implicando che l’evoluzione mantiene l’uso dei codoni vicino a un ottimo intermedio piuttosto che spingerlo indefinitamente verso una corrispondenza perfetta.
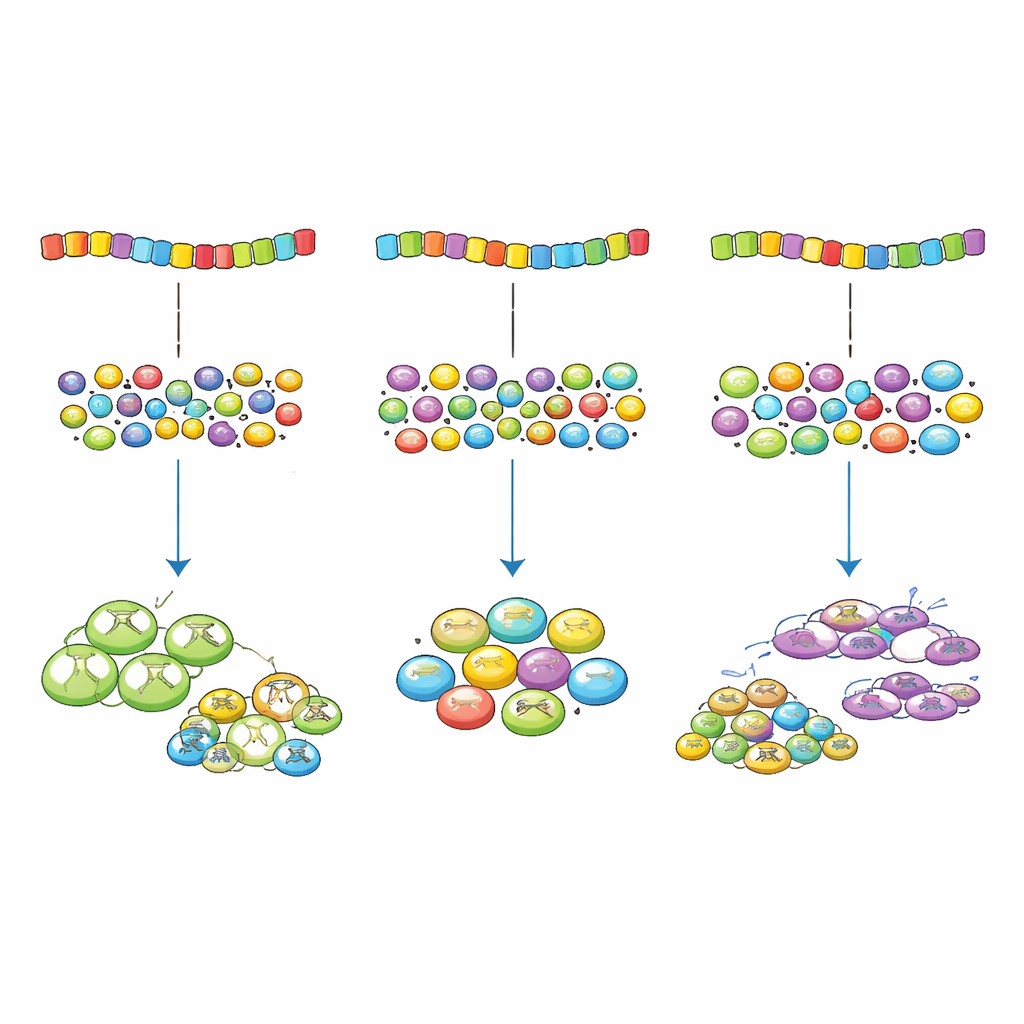
Perché un po’ di imperfezione aiuta
Per un lettore non specialista, il messaggio chiave è che esiste il concetto di “troppo ottimizzato” quando si parla della grafia genica. Un allineamento perfetto tra codoni e strumenti di traduzione della cellula può portare alcuni geni a monopolizzare la macchina condivisa, privando gli altri e rallentando la crescita complessiva. L’evoluzione sembra invece favorire un disallineamento controllato e lieve che fornisce abbastanza proteina dai geni importanti senza sovraccaricare il sistema. Questa intuizione non solo cambia il modo in cui consideriamo le mutazioni apparentemente “silenziose”, ma offre anche indicazioni pratiche per progettare geni più sicuri ed efficienti in biotecnologia e medicina.
Citazione: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Parole chiave: bias nell’uso dei codoni, fornitura di tRNA, mutazioni sinonime, traduzione delle proteine, resistenza agli antibiotici