Clear Sky Science · pl
Niewielkie niedopasowanie między użyciem kodonów w genie a zasobem tRNA w komórce jest korzystne
Kiedy „ciche” wybory DNA nie są takie ciche
Nasze geny mają wiele sposobów zapisania tej samej instrukcji, używając różnych trzyliterowych „słów” DNA, które oznaczają ten sam aminokwas. Przez dekady te alternatywne pisownie — zwane kodonami synonimicznymi — uważano za w dużej mierze błahe szczegóły. To badanie obala ten pogląd. Pokazuje, że to, jak bardzo „akcent” kodonowy genu odpowiada maszynerii translacyjnej komórki, może przesądzać o różnicy między ospałym wzrostem a rozwojem, a że niewielkie niedopasowanie może w rzeczywistości być najlepsze.
Jak komórki odczytują instrukcje genetyczne
Aby przekształcić geny w białka, komórki używają małych cząsteczek adapterowych zwanych tRNA, które rozpoznają kodony na mRNA i dostarczają odpowiednie aminokwasy. Każdy aminokwas (z dwiema wyjątkami) ma kilka możliwych kodonów, ale komórki nie używają ich w równym stopniu. W toku ewolucji organizmy rozwijają charakterystyczny wzorzec użycia kodonów i gromadzą odpowiedni zasób tRNA. Tradycyjny pogląd zakłada, że idealna sytuacja to perfekcyjne dopasowanie: kodony używane w genach odzwierciedlają dostępne tRNA, co daje szybką i dokładną translację. Każde odchylenie od tego idealnego dopasowania uważano za efekt dryfu genetycznego i mutacji, a nie za coś korzystnego.
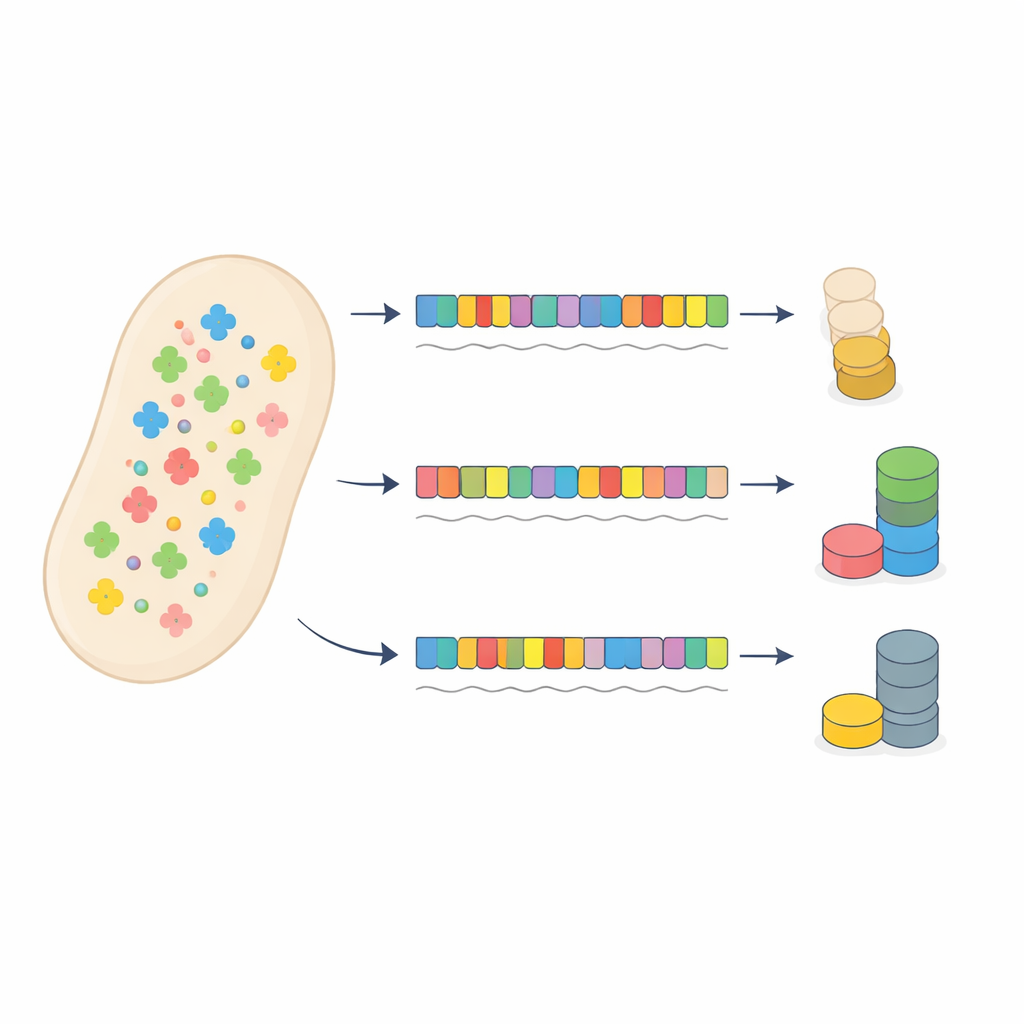
Przypadek testowy z użyciem oporności na antybiotyk
Autorzy zakwestionowali ten konwencjonalny obraz, starannie przeprojektowując gen odpowiadający za oporność na antybiotyk w bakteriach. Stworzyli 53 wersje genu nadającego oporność na gentamycynę, które wszystkie kodowały to samo białko, lecz używały różnych wzorców kodonów synonimicznych — od prawie idealnego dopasowania do puli tRNA komórki po silne niedopasowanie. Każda wersja została umieszczona na plazmidzie i połączona z markerem fluorescencyjnym, aby można było zmierzyć ilość wytwarzanego białka. Drugi białkowy fluorescencyjny wskaźnik na tym samym plazmidzie służył jako czujnik, jak bardzo system translacyjny pracuje ogólnie, ponieważ intensywne użycie tRNA przez gen oporności spowalniało translację innych białek.
Odnalezienie optymalnego punktu wzrostu
Gdy te zaprojektowane bakterie rosły w pożywce zawierającej gentamycynę, geny, których kodony bardzo dobrze pasowały do puli tRNA, produkowały najwięcej białka zapewniającego oporność — ale jednocześnie narzucały największe obciążenie na maszynerię translacyjną komórki. Bakterie niosące takie „nadoptymalizowane” geny rosły wolniej niż te z umiarkowanym niedopasowaniem. Innymi słowy, chociaż lepsze dopasowanie zwiększało korzyść płynącą z białka oporności, to również podnosiło koszt korzystania ze wspólnych zasobów translacyjnych, i powyżej pewnego progu koszt przeważał. Najszybciej rosnące komórki miały wersje genu wykazujące niewielkie, a nie minimalne, niedopasowanie do zasobu tRNA, co wskazuje, że prawdziwe optimum równoważy zysk i koszt, zamiast maksymalizować tylko jedno z nich.
Gdy znaczenie genu się zmienia, zmienia się też optimum
Zespół następnie zmieniał, jak istotny był gen oporności, modyfikując dawkę antybiotyku. Przy niskich stężeniach gentamycyny korzyść z białka dla przetrwania była niewielka, a najlepiej działające wzorce kodonów wykazywały stosunkowo duże niedopasowanie, co zmniejszało marnotrawstwo zasobów translacyjnych. W miarę wzrostu stężenia antybiotyku i rosnącej wagi genu optymalny wzorzec kodonów przesunął się ku bliższemu dopasowaniu do puli tRNA, a przy bardzo wysokich dawkach niemal perfekcyjne dopasowanie sprawdzało się najlepiej. Podobne eksperymenty z drugim genem oporności oraz bezpośrednie zmiany podaży tRNA potwierdziły tę samą zasadę: najlepsze użycie kodonów zależy od tego, jak dużą korzyść daje gen i jaki koszt translacyjny generuje.
Wskazówki z genomów naturalnych
Aby sprawdzić, czy ten kompromis odbija się w ewolucji, autorzy przeanalizowali tysiące genów z bakterii, drożdży, muszek owocowych i ludzi. Dla genów ważniejszych dla przeżycia — oszacowanych na podstawie tego, jak bardzo wzrost ucierpi po ich usunięciu — naturalne użycie kodonów ma tendencję do bliższego dopasowania do puli tRNA, szczególnie wśród genów silnie eksprymowanych. Jednocześnie wśród genów o najwyższej ekspresji wzorce kodonów z idealnie ścisłym dopasowaniem są w rzeczywistości mniej powszechne; zamiast tego te geny zachowują umiarkowane niedopasowanie, co jest zgodne z unikaniem nadmiernych kosztów translacji. Eksperymenty akumulacji mutacji i precyzyjne pomiary wpływu pojedynczych mutacji synonimicznych w drożdżach dodatkowo wykazały, że zarówno zwiększanie, jak i zmniejszanie niedopasowania często jest szkodliwe, co sugeruje, że ewolucja utrzymuje użycie kodonów w pobliżu pośredniego optimum, zamiast nieustannie dążyć do perfekcyjnego dopasowania.
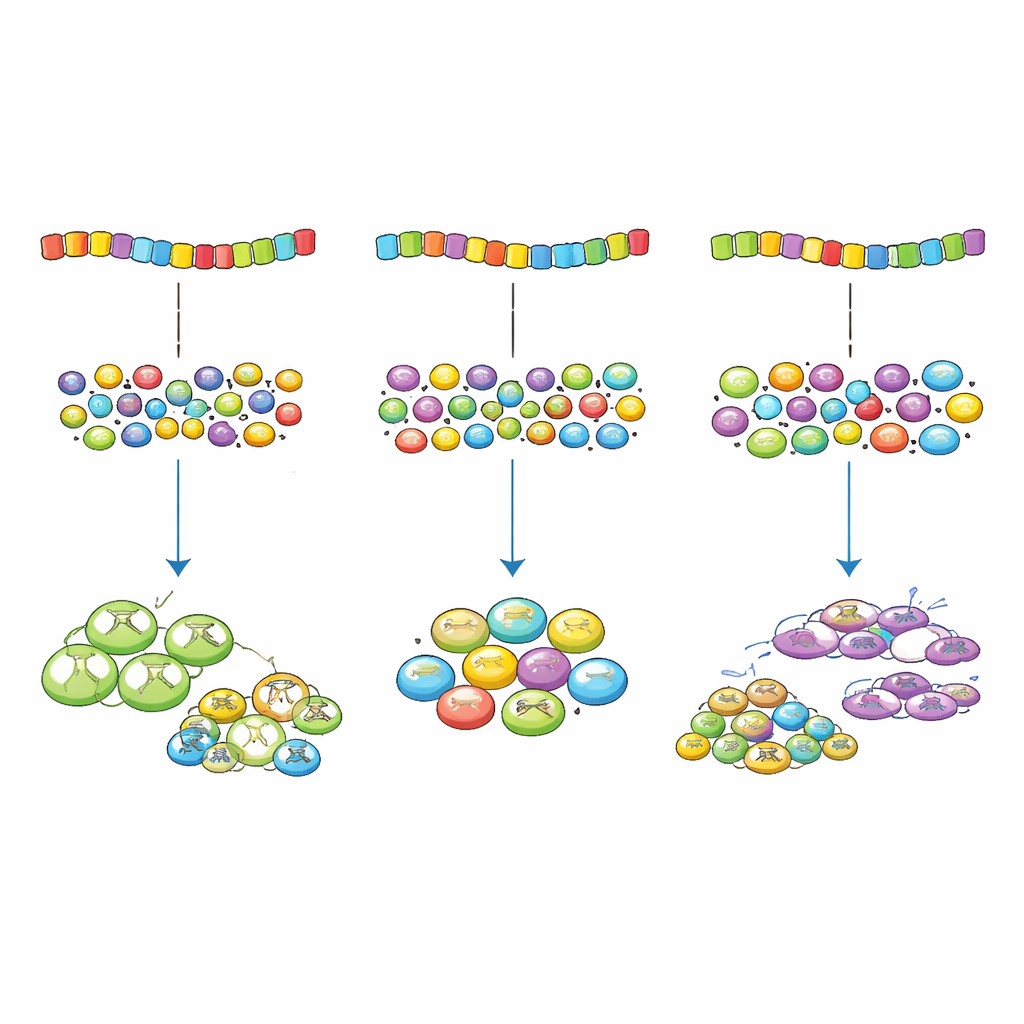
Dlaczego odrobina niedoskonałości pomaga
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że istnieje coś takiego jak „zbyt optymalny” zapis genu. Perfekcyjne dopasowanie między kodonami a narzędziami translacyjnymi komórki może sprawić, że niektóre geny będą monopolizować wspólną maszynerię, pozbawiając innych i spowalniając ogólny wzrost. Ewolucja zdaje się woleć kontrolowane, niewielkie niedopasowanie, które dostarcza wystarczającej ilości białka z ważnych genów bez nadmiernego obciążania systemu. Ta obserwacja nie tylko zmienia sposób myślenia o rzekomo „cichych” mutacjach, lecz także daje praktyczne wskazówki przy projektowaniu bezpieczniejszych i wydajniejszych genów w biotechnologii i medycynie.
Cytowanie: Chen, F., Liu, Y., Zhou, Z. et al. A slight mismatch between a gene’s codon usage and the cellular tRNA supply is beneficial. Nat Commun 17, 3371 (2026). https://doi.org/10.1038/s41467-026-69643-2
Słowa kluczowe: preferencje użycia kodonów, zasób tRNA, mutacje synonimiczne, translacja białek, oporność na antybiotyki