Clear Sky Science · pt
tRF-3005a regula o salto de éxons de SPAG4 ao interagir com RALY para impulsionar a progressão do câncer gástrico
Por que este estudo sobre câncer de estômago importa
O câncer de estômago continua entre os tipos mais letais do mundo, em parte porque frequentemente é detectado tardiamente e os tratamentos atuais não funcionam para todos. Este estudo revela uma camada de regulação previamente oculta dentro das células tumorais, envolvendo pequenos fragmentos de RNA e uma proteína que edita as mensagens genéticas. Ao mostrar como essa parceria molecular ajuda os tumores gástricos a crescer, o trabalho aponta para novos marcadores de alerta precoce e alvos terapêuticos que, no futuro, podem melhorar a sobrevida dos pacientes.
Pequenos pedaços de RNA com grande influência
Pesquisadores há muito tempo consideram os RNAs de transferência como auxiliares simples na construção de proteínas. Nos últimos anos, porém, pequenos trechos cortados dessas moléculas — chamados fragmentos derivados de tRNA — emergiram como reguladores potentes no câncer. Os autores concentraram-se em um desses fragmentos, tRF-3005a, após sequenciarem amostras tumorais de pacientes com câncer gástrico. Eles descobriram que tRF-3005a era muito mais abundante no tecido tumoral do que no tecido gástrico saudável adjacente, e níveis mais altos se associaram a tumores maiores, invasão mais profunda, disseminação para linfonodos e pior sobrevida global. Experimentos de imagem mostraram que, ao contrário das células gástricas normais, tRF-3005a nas células cancerosas localiza-se principalmente no núcleo, o centro de comando onde as mensagens genéticas são processadas.
Impulsionando crescimento, invasão e disseminação
Para testar o que tRF-3005a realmente faz, a equipe aumentou ou bloqueou seus níveis em um painel de linhas celulares de câncer gástrico. Quando tRF-3005a foi elevado, as células cancerosas cresceram mais rápido, formaram mais colônias e tornaram-se mais capazes de invadir através de membranas artificiais e migrar por superfícies — comportamentos que espelham a expansão e disseminação tumoral no organismo. Quando tRF-3005a foi suprimido, essas características agressivas foram fortemente reduzidas. Em camundongos, tumores implantados a partir de células com tRF-3005a diminuído permaneceram menores e mostraram atividade reduzida de proteínas-chave ligadas ao crescimento, confirmando que o fragmento de RNA promove o crescimento tumoral não só em cultura, mas também em organismos vivos.
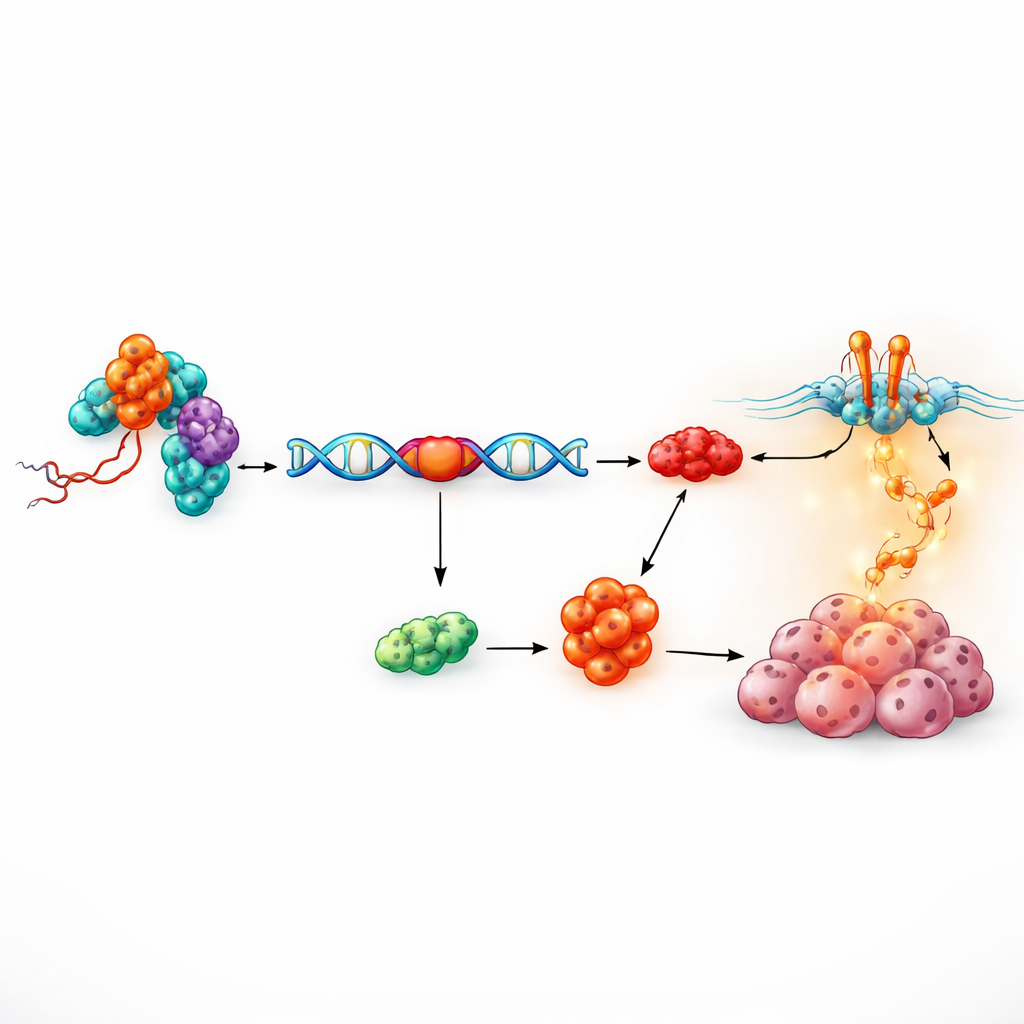
Uma parceira proteica que edita mensagens genéticas
A próxima pergunta foi como um fragmento de RNA de 17 nucleotídeos poderia ter efeitos tão fortes. Usando uma abordagem bioquímica de “pesca”, os pesquisadores isolaram proteínas que se ligam fisicamente a tRF-3005a. Entre 81 candidatos, uma proteína nuclear — RALY — sobressaiu. RALY faz parte de uma família de fatores que modelam como as mensagens genéticas brutas são cortadas e emendadas, um processo conhecido como splicing alternativo. Mapas detalhados mostraram que tRF-3005a se prende a uma região média flexível de RALY sem alterar sua quantidade global, sugerindo que ajusta o comportamento de RALY em vez de simplesmente ativá-lo ou desativá-lo. Experimentos de resgate funcional, nos quais os níveis de RALY foram aumentados ou reduzidos, mostraram que o efeito promotor de crescimento de tRF-3005a depende estritamente de RALY, definindo um eixo tRF-3005a–RALY que alimenta a proliferação das células cancerosas.
Reprogramando um único gene para favorecer uma forma prejudicial
Para ver quais mensagens genéticas são remodeladas por esse eixo, a equipe sequenciou o mRNA de células nas quais tRF-3005a foi bloqueado e analisou mudanças nos padrões de splicing. Os eventos mais afetados envolveram o salto de éxons específicos, e um gene, SPAG4, emergiu como um dos principais alvos. SPAG4 pode ser produzido em duas formas principais: uma versão longa que inclui o éxon 8 e uma versão curta que omite esse éxon. Os pesquisadores mostraram que RALY se liga principalmente à região em torno do éxon 8 e suprime sua omissão, empurrando as células a produzir mais da variante longa de SPAG4. Essa forma longa, e não a curta, impulsionou o crescimento das células cancerosas. Importante, tRF-3005a reforçou a interação física entre RALY e o RNA de SPAG4, reduzindo ainda mais o salto do éxon 8 e favorecendo a forma SPAG4-L promotora de tumor.
Ligação a uma via de crescimento importante no câncer
A jusante de SPAG4-L, o estudo identificou GRB14, uma proteína adaptadora de sinalização, e a conhecida via PI3K/AKT, que controla a sobrevivência e o crescimento celular em muitos cânceres. Quando SPAG4-L ou tRF-3005a eram aumentados, os níveis de GRB14 e da PI3K/AKT ativada subiam, juntamente com a proteína oncogênica c-Myc. Silenciar GRB14 ou bloquear quimicamente PI3K/AKT atenuou o aumento de crescimento causado por tRF-3005a ou SPAG4-L, enquanto restaurar GRB14 reverteu esse efeito. Esses resultados sustentam uma cadeia de eventos: tRF-3005a liga-se a RALY, RALY remodela o splicing de SPAG4 para favorecer a forma longa, e SPAG4-L ativa GRB14 e a sinalização PI3K/AKT, levando em última instância à divisão celular descontrolada.
O que isso significa para os pacientes
Em conjunto, o trabalho revela como um minúsculo fragmento de RNA pode agir como um interruptor mestre para uma via promotora de câncer em tumores gástricos. Ao ajustar finamente uma proteína de splicing, tRF-3005a direciona um único gene para uma versão prejudicial que alimenta um sinal de crescimento potente. Como tRF-3005a está elevado em tumores e associado a piores desfechos, ele poderia servir como biomarcador para identificar pacientes de alto risco. Em prazo mais longo, drogas ou terapias baseadas em RNA que bloqueiem tRF-3005a, interrompam sua interação com RALY ou revertam SPAG4 para sua forma mais segura podem oferecer novas formas de desacelerar ou impedir a progressão do câncer de estômago.
Citação: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Palavras-chave: câncer gástrico, fragmentos derivados de tRNA, splicing alternativo, sinalização PI3K AKT, biomarcadores