Clear Sky Science · de
tRF-3005a reguliert Exon-Skipping von SPAG4 durch Wechselwirkung mit RALY und treibt das Fortschreiten von Magenkrebs voran
Warum diese Studie zu Magenkrebs wichtig ist
Magenkrebs gehört weiterhin zu den tödlichsten Krebserkrankungen weltweit, teils weil er oft spät entdeckt wird und aktuelle Therapien nicht für alle Patienten wirken. Diese Studie offenbart eine bislang verborgene Kontrollebene in Tumorzellen, die winzige RNA-Fragmente und ein Protein umfasst, das Genbotschaften bearbeitet. Indem sie zeigt, wie diese molekulare Partnerschaft das Wachstum von Magentumoren fördert, liefert die Arbeit Hinweise auf neue Frühwarnmarker und therapeutische Zielstrukturen, die eines Tages die Überlebenschancen der Patienten verbessern könnten.
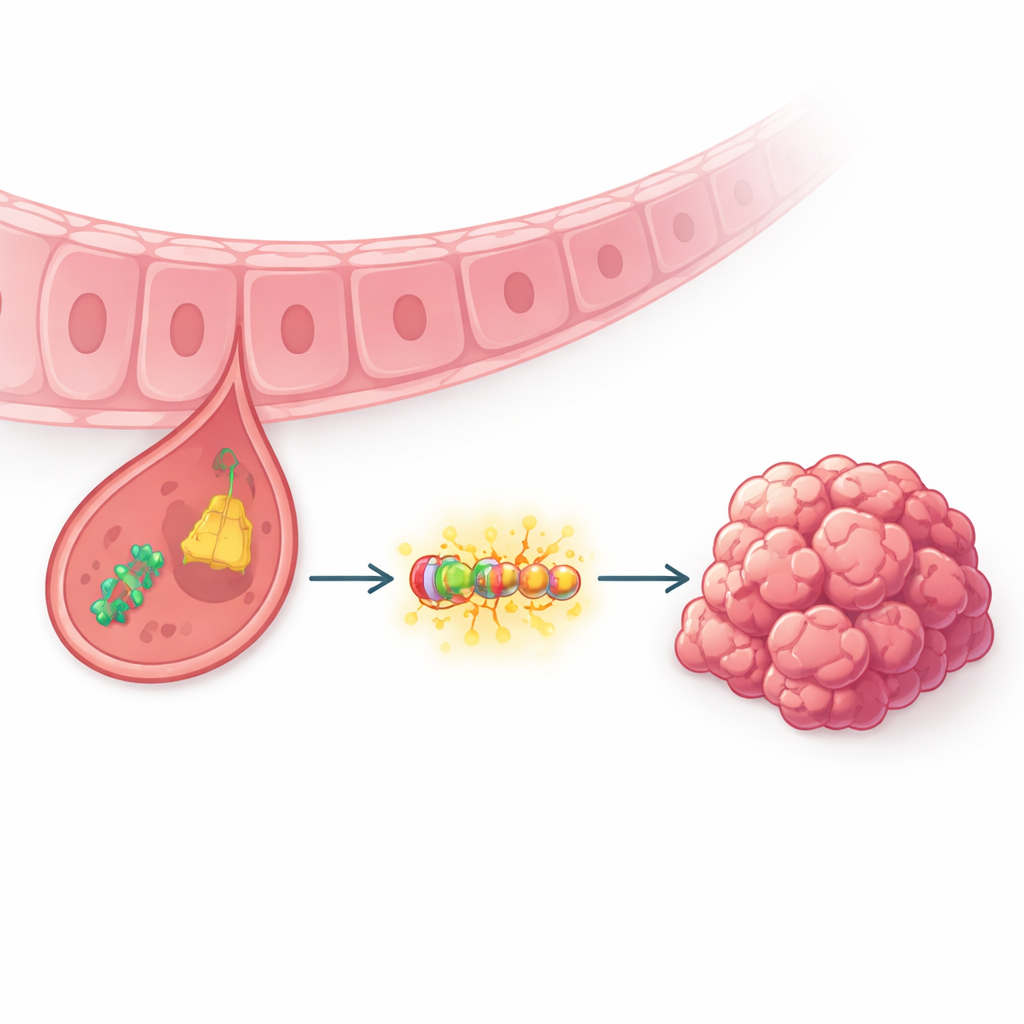
Kleine RNA‑Stücke mit großer Wirkung
Forscher betrachteten Transfer‑RNAs lange Zeit als einfache Helfer beim Proteinaufbau. In den letzten Jahren haben sich jedoch kleine, aus diesen Molekülen geschnittene Fragmente — sogenannte tRNA‑stammende Fragmente — als potente Regulatoren in Krebs etabliert. Die Autoren konzentrierten sich auf eines dieser Fragmente, tRF‑3005a, nachdem sie Tumorproben von Patienten mit Magenkrebs sequenziert hatten. Sie fanden heraus, dass tRF‑3005a in Krebsgewebe deutlich stärker vertreten war als im benachbarten gesunden Magengewebe; höhere Mengen korrelierten mit größeren Tumoren, tieferem Eindringen, Lymphknotenbefall und schlechterem Gesamtüberleben. Bildgebende Experimente zeigten, dass tRF‑3005a in Krebszellen, anders als in normalen Magenzellen, vorwiegend im Zellkern lokalisiert ist — dem Schaltzentrum, in dem Genbotschaften verarbeitet werden.
Fördert Wachstum, Invasion und Ausbreitung
Um die Funktion von tRF‑3005a zu testen, erhöhten oder blockierten die Forschenden dessen Niveau in einer Reihe von Magenkrebs‑Zelllinien. Bei Erhöhung von tRF‑3005a wuchsen die Krebszellen schneller, bildeten mehr Kolonien und waren stärker in der Lage, durch künstliche Membranen zu invasieren und über Oberflächen zu migrieren — Verhaltensweisen, die das Tumorwachstum und die Streuung im Körper widerspiegeln. Bei Unterdrückung von tRF‑3005a gingen diese aggressiven Merkmale deutlich zurück. In Mäusen blieben implantierte Tumoren aus Zellen mit reduziertem tRF‑3005a kleiner und zeigten geringere Aktivität von zentralen wachstumsrelevanten Proteinen, was bestätigt, dass das RNA‑Fragment das Tumorwachstum nicht nur in Zellkulturen, sondern auch in lebenden Organismen fördert.
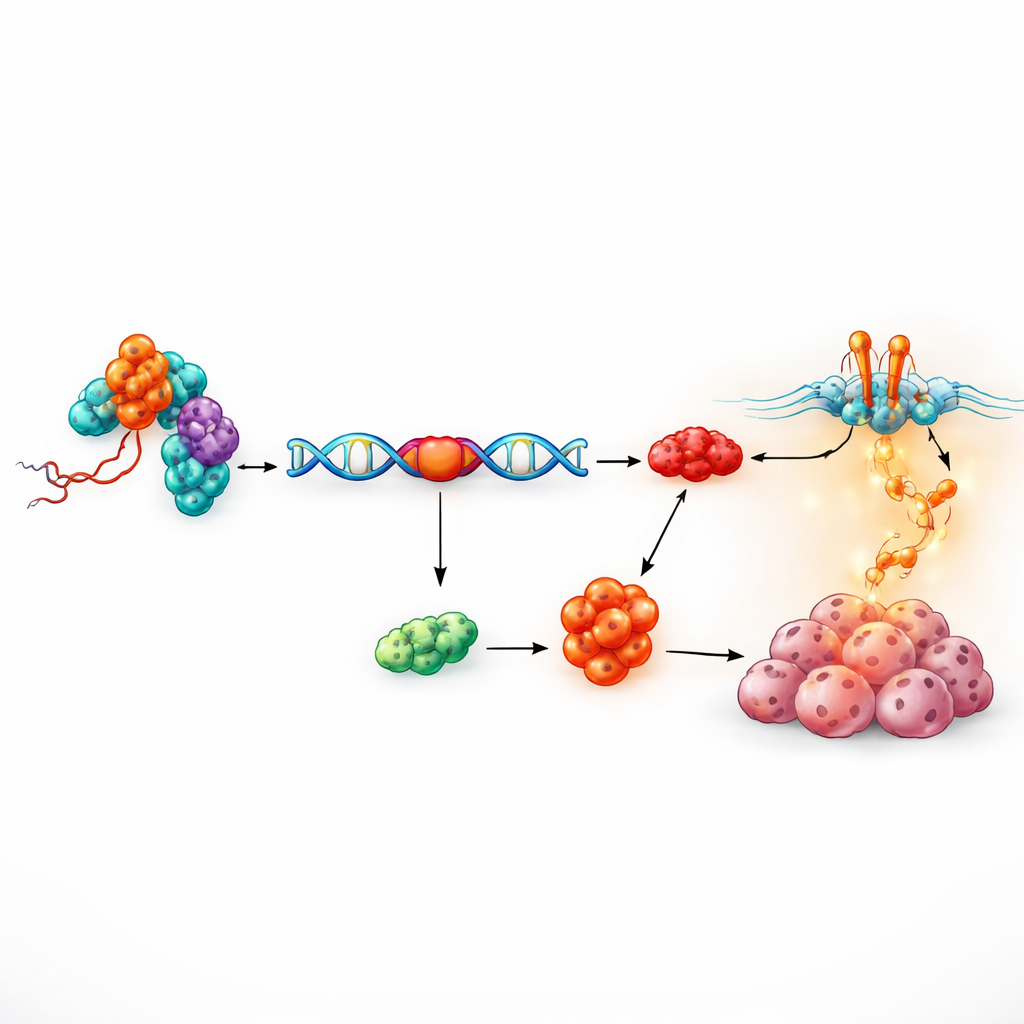
Ein Proteinpartner, der Genbotschaften bearbeitet
Die nächste Frage war, wie ein 17‑Nukleotid‑RNA‑Fragment so starke Effekte ausüben kann. Mit einem biochemischen „Fishing“-Ansatz zogen die Forschenden Proteine an, die physisch an tRF‑3005a binden. Unter 81 Kandidaten stach ein nukleäres Protein — RALY — hervor. RALY gehört zu einer Familie von Faktoren, die beeinflussen, wie rohe Genbotschaften zugeschnitten und zusammengesetzt werden, ein Prozess, der als alternatives Spleißen bekannt ist. Detaillierte Kartierungen zeigten, dass tRF‑3005a an eine flexible mittlere Region von RALY bindet, ohne dessen Gesamtmenge zu verändern, was darauf hindeutet, dass es das Verhalten von RALY moduliert, statt es einfach ein‑ oder auszuschalten. Funktionelle Rescue‑Experimente, bei denen RALY erhöht oder erniedrigt wurde, zeigten, dass der wachstumsfördernde Effekt von tRF‑3005a streng von RALY abhängt und damit eine tRF‑3005a–RALY‑Achse definiert, die die Proliferation von Krebszellen antreibt.
Umschalten eines einzelnen Gens zugunsten einer schädlichen Form
Um herauszufinden, welche Genbotschaften durch diese Achse verändert werden, sequenzierten die Forschenden mRNA aus Zellen, in denen tRF‑3005a blockiert war, und analysierten Veränderungen in den Spleißmustern. Am stärksten betroffen waren Ereignisse, die das Überspringen bestimmter Exons betrafen; ein Gen, SPAG4, trat dabei als Top‑Kandidat hervor. SPAG4 kann in zwei Hauptformen produziert werden: eine lange Variante, die Exon 8 enthält, und eine kurze Variante, die dieses Exon auslässt. Die Forscher zeigten, dass RALY überwiegend an die Region um Exon 8 bindet und dessen Überspringen unterdrückt, wodurch Zellen vermehrt die lange SPAG4‑Variante herstellen. Diese lange Form, nicht aber die kurze, förderte das Wachstum von Krebszellen. Wichtig ist, dass tRF‑3005a die physische Wechselwirkung zwischen RALY und SPAG4‑RNA verstärkte, wodurch Exon‑8‑Skipping weiter reduziert und das Gleichgewicht zugunsten der tumorfördernden SPAG4‑L‑Form verschoben wurde.
Verbindung zu einem wichtigen Wachstumsweg im Krebs
Stromabwärts von SPAG4‑L identifizierte die Studie GRB14, ein Adapterprotein der Signalübertragung, und den bekannten PI3K/AKT‑Signalweg, der in vielen Krebsarten Überleben und Wachstum von Zellen steuert. Bei Erhöhung von SPAG4‑L oder tRF‑3005a stiegen die Spiegel von GRB14 und aktivierter PI3K/AKT sowie das krebsfördernde Protein c‑Myc an. Das Stilllegen von GRB14 oder die chemische Hemmung von PI3K/AKT schwächte den durch tRF‑3005a oder SPAG4‑L verursachten Wachstumsschub ab, während die Wiederherstellung von GRB14 diesen Effekt umkehrte. Diese Ergebnisse stützen eine Abfolge von Ereignissen: tRF‑3005a bindet RALY, RALY verändert das Spleißen von SPAG4 zugunsten der langen Form, und SPAG4‑L aktiviert GRB14 und die PI3K/AKT‑Signalgebung, was letztlich unkontrollierte Zellteilung antreibt.
Was das für Patienten bedeutet
In der Summe zeigt die Arbeit, wie ein winziges RNA‑Fragment als Hauptschalter für einen krebserzeugenden Signalweg in Magentumoren wirken kann. Indem es ein Spleißprotein feinjustiert, lenkt tRF‑3005a ein einzelnes Gen in eine schädliche Variante, die ein starkes Wachstumssignal nährt. Da tRF‑3005a in Tumoren erhöht ist und mit schlechteren Verläufen einhergeht, könnte es als Biomarker dienen, um Hochrisiko‑Patienten zu identifizieren. Langfristig könnten Medikamente oder RNA‑basierte Therapien, die tRF‑3005a blockieren, seine Interaktion mit RALY stören oder SPAG4 wieder in die sichere Form lenken, neue Möglichkeiten bieten, das Fortschreiten von Magenkrebs zu verlangsamen oder zu stoppen.
Zitation: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Schlüsselwörter: Magenkrebs, aus tRNA stammende Fragmente, alternatives Spleißen, PI3K-AKT-Signalgebung, Biomarker