Clear Sky Science · ar
tRF-3005a ينظّم تخطي الإكسون في SPAG4 عبر التفاعل مع RALY لدفع تقدم سرطان المعدة
لماذا تهم هذه الدراسة عن سرطان المعدة
لا يزال سرطان المعدة واحدًا من أكثر السرطانات فتكًا على مستوى العالم، جزئيًا لأنه يُكتشف في كثير من الأحيان في مراحل متأخرة ولا تستجيب العلاجات الحالية للجميع. تكشف هذه الدراسة عن طبقة تحكم خفية داخل خلايا الورم، تشمل شظايا رنا صغيرة وبروتين يحرّر رسائل الجينات. من خلال توضيح كيف يساعد هذا التعاون الجزيئي الأورام المعدية على النمو، تشير الدراسة إلى مؤشرات إنذار مبكر وأهداف علاجية جديدة قد تحسن في المستقبل بقاء المرضى.
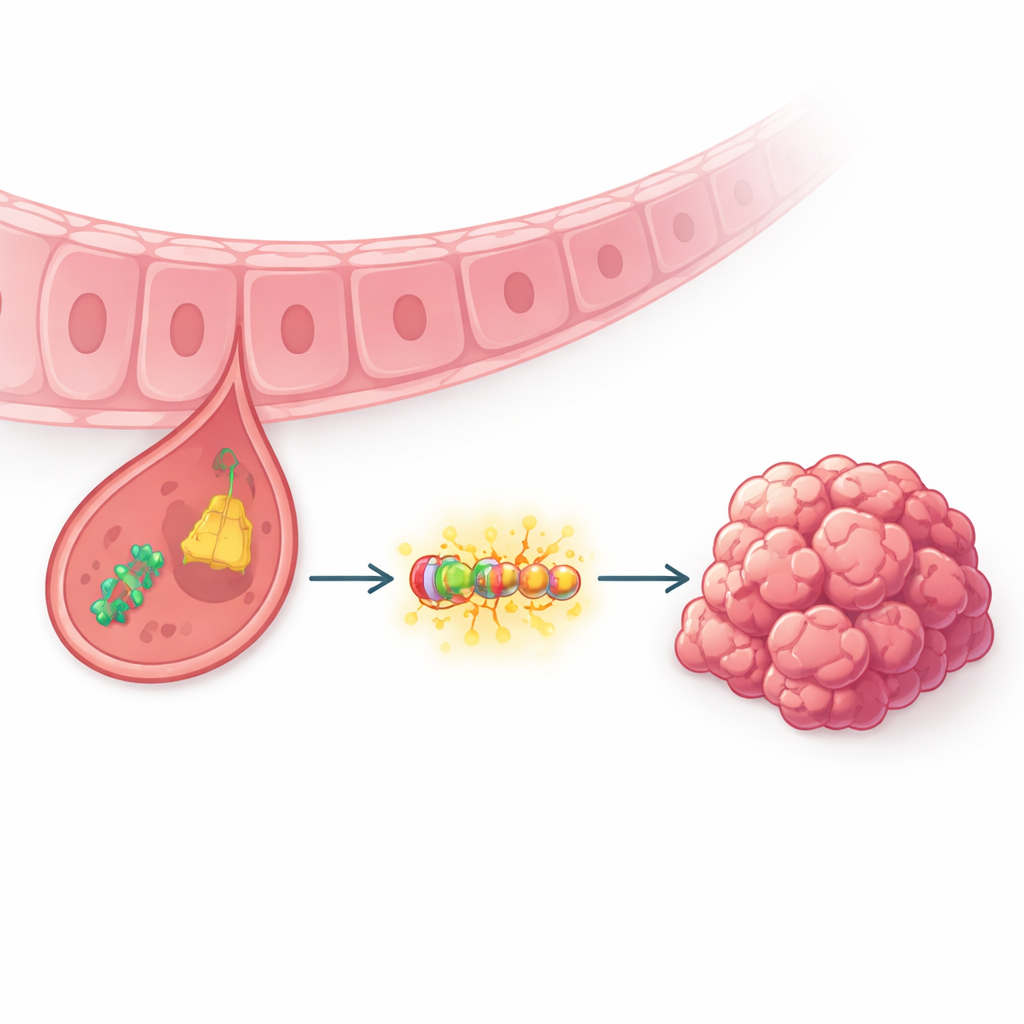
قطع رنا صغيرة ذات تأثير كبير
لطالما اعتبر الباحثون الرنا الناقل مساعدة بسيطة في عملية بناء البروتينات. ومع ذلك، برزت في السنوات الأخيرة قطع صغيرة مقطوعة من هذه الجزيئات — تُعرف بشظايا مشتقة من الرنا الناقل — بوصفها منظمين قويين في السرطان. ركز المؤلفون على إحدى هذه الشظايا، tRF-3005a، بعد تسلسل عينات أورام من مرضى سرطان المعدة. وجدوا أن tRF-3005a أكثر وفرة بكثير في نسيج الورم مقارنة بالنسيج المعدي السليم المجاور، وأن المستويات الأعلى ارتبطت بأورام أكبر، واختراق أعمق، وانتشار إلى العقد اللمفية، وبقاء إجمالي أسوأ. أظهرت تجارب التصوير أن tRF-3005a في الخلايا السرطانية، خلافًا للخلايا المعدية الطبيعية، يتمركز أساسًا في النواة، مركز القيادة حيث تُعالَج رسائل الجينات.
قيادة النمو والغزو والانتشار
لاختبار ما تفعله tRF-3005a فعليًا، زاد الفريق مستوياتها أو حجبها في مجموعة من خطوط خلايا سرطان المعدة. عندما ارتفعت مستويات tRF-3005a، نمت الخلايا السرطانية أسرع، شكّلت مستعمرات أكثر، وأصبحت أكثر قدرة على اختراق أغشية اصطناعية والهجرة عبر الأسطح — سلوكيات تعكس توسع الورم وانتشاره في الجسم. عندما كُبتت tRF-3005a، تراجعت هذه السمات العدوانية بشكل حاد. في الفئران، بقيت الأورام المزروعة من خلايا ذات مستويات منخفضة من tRF-3005a أصغر وأظهرت نشاطًا مخفضًا لبروتينات رئيسية مرتبطة بالنمو، مما يؤكد أن شظية الرنا تعزز نمو الورم ليس فقط في الأطباق المختبرية بل أيضًا في الكائنات الحية.
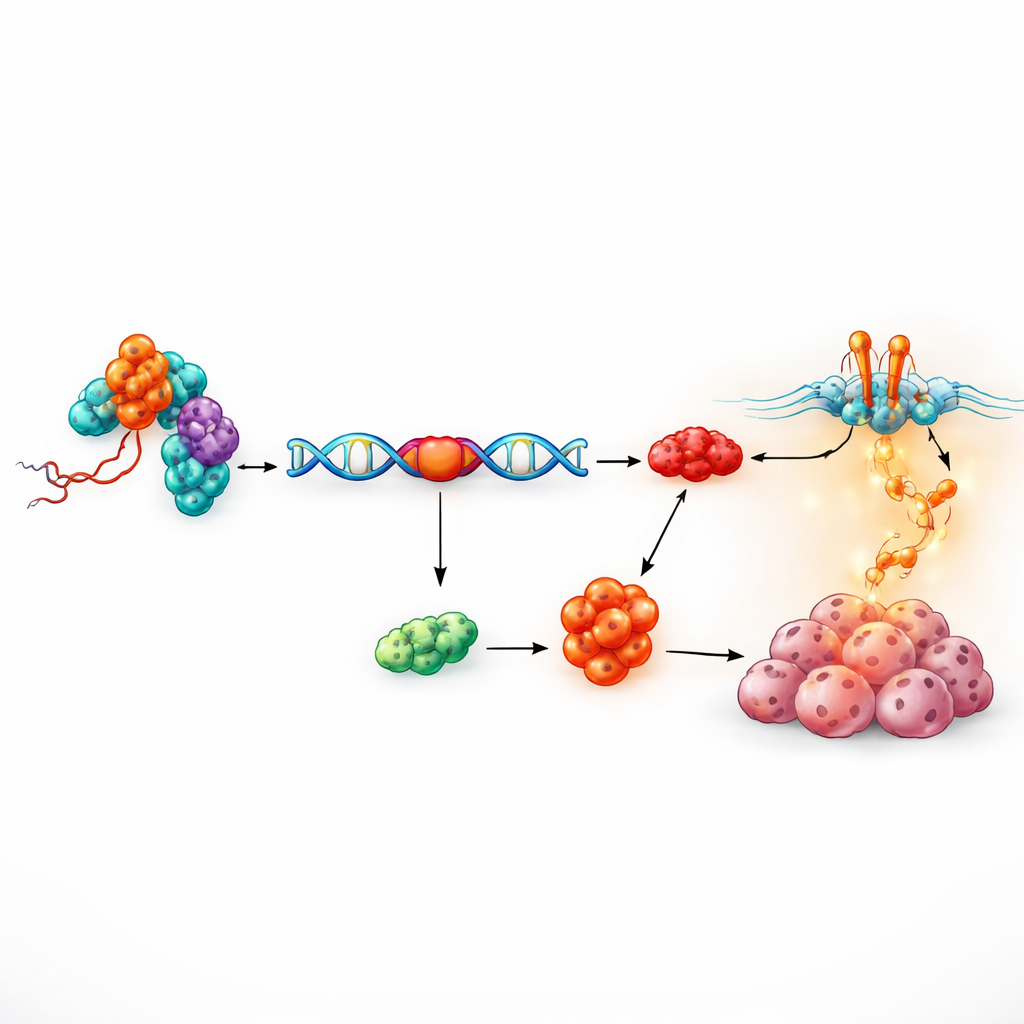
شريك بروتيني يحرّر رسائل الجينات
السؤال التالي كان كيف يمكن لشظية رنا مكونة من 17 نيوكليوتيدة أن تُحدث مثل هذه التأثيرات القوية. باستخدام نهج صيد حيوي كيميائي، سحب الباحثون البروتينات التي ترتبط ماديًا بـ tRF-3005a. من بين 81 مرشحًا، برز بروتين نووي واحد — RALY. ينتمي RALY إلى عائلة عوامل تشكل كيفية قصّ وربط رسائل الجينات الأولية، وهي عملية تُعرف بالطي البديل للنسخة. أظهر التحديد المفصل أن tRF-3005a تمسك بمنطقة وسطى مرنة في RALY دون تغيير كميته الإجمالية، ما يشير إلى أنه يضبط سلوك RALY بدلًا من تشغيله أو إيقافه ببساطة. أظهرت تجارب الاسترداد الوظيفي، حيث رُفعت أو خُفضت مستويات RALY، أن التأثير المحفز للنمو لـ tRF-3005a يعتمد بشكل صارم على RALY، محددة محور tRF-3005a–RALY الذي يغذي تكاثر الخلايا السرطانية.
إعادة توصيل جين واحد لصالح شكل ضار
لمعرفة أي رسائل جينية يعيد هذا المحور تشكيلها، سلّل الفريق الحمض النووي الريبوزي منقوص الأكسجين (mRNA) من خلايا حُجب فيها tRF-3005a وحلّل التغيرات في أنماط الطي. كانت أكثر الأحداث تأثرًا تتعلق بتخطي إكسونات محددة، وبرز جين واحد، SPAG4، كأبرز النتائج. يمكن إنتاج SPAG4 في شكلين رئيسيين: نسخة طويلة تتضمّن الإكسون 8 ونسخة قصيرة تتخلى عن هذا الإكسون. أظهر الباحثون أن RALY يرتبط أساسًا بالمنطقة المحيطة بالإكسون 8 ويمنع تخطيه، ما يدفع الخلايا لإنتاج المزيد من النسخة الطويلة من SPAG4. هذه النسخة الطويلة، وليس القصيرة، حفزت نمو الخلايا السرطانية. والأهم من ذلك، أن tRF-3005a قوّت التفاعل الفيزيائي بين RALY وRNA الخاص بـ SPAG4، مما قلّل أكثر من تخطي الإكسون 8 وميل التوازن نحو الشكل المحفز للورم SPAG4-L.
صلة بمسار نمو رئيسي في السرطان
أسفل SPAG4-L، حددت الدراسة البروتين الحامل للإشارات GRB14 ومسار PI3K/AKT المعروف، الذي يتحكم في بقاء الخلايا ونموها في العديد من السرطانات. عندما ارتفعت مستويات SPAG4-L أو tRF-3005a، ارتفعت مستويات GRB14 ومسارات PI3K/AKT المفعّلة، إلى جانب البروتين المحفز للسرطان c-Myc. أدى إسكات GRB14 أو حجب PI3K/AKT كيميائيًا إلى تلاشي الزيادة في النمو الناجمة عن tRF-3005a أو SPAG4-L، بينما أعاد استرجاع GRB14 هذا التأثير. تدعم هذه النتائج سلسلة أحداث: تلتصق tRF-3005a بـ RALY، يعيد RALY تشكيل طي SPAG4 لصالح الشكل الطويل، وSPAG4-L ينشط GRB14 وإشارة PI3K/AKT، مما يؤدي في النهاية إلى انقسام خلوي غير منضبط.
ما يعنيه هذا للمرضى
تُظهر هذه الدراسة مجتمعة كيف يمكن لشظية رنا صغيرة أن تعمل كمفتاح رئيسي لمسار يروّج للسرطان في أورام المعدة. من خلال ضبط بروتين الطي بدقة، توجه tRF-3005a جينًا واحدًا نحو نسخة ضارة تغذي إشارة نمو قوية. وبما أن tRF-3005a مرتفعة في الأورام ومرتبطة بنتائج أسوأ، فقد تكون علامة حيوية للإشارة إلى المرضى ذوي المخاطر العالية. وعلى المدى الطويل، قد توفر أدوية أو علاجات قائمة على الرنا تحجب tRF-3005a، تعطل تفاعلها مع RALY، أو تعيد SPAG4 إلى شكلها الآمن طرقًا جديدة لإبطاء أو إيقاف تقدم سرطان المعدة.
الاستشهاد: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
الكلمات المفتاحية: سرطان المعدة, شقوق مشتقة من الرنا الناقل, الطي البديل للنسخة, إشارة PI3K AKT, مؤشرات حيوية