Clear Sky Science · it
tRF-3005a regola l’esclusione di esoni di SPAG4 interagendo con RALY per promuovere la progressione del cancro gastrico
Perché questo studio sul cancro allo stomaco è importante
Il cancro gastrico resta una delle neoplasie più letali al mondo, in parte perché spesso viene scoperto in fase avanzata e le terapie attuali non sono efficaci per tutti. Questo studio mette in luce un livello di controllo finora nascosto all’interno delle cellule tumorali, che coinvolge minuscoli frammenti di RNA e una proteina che modula il processamento dei messaggi genetici. Rivelando come questa collaborazione molecolare favorisca la crescita dei tumori gastrici, il lavoro indica nuovi possibili marker precoci e bersagli terapeutici che un giorno potrebbero migliorare la sopravvivenza dei pazienti.
Pezzetti di RNA con grande influenza
Per lungo tempo i tRNA sono stati considerati semplici facilitatori nella sintesi proteica. Negli ultimi anni, però, piccoli frammenti ricavati da queste molecole—chiamati frammenti derivati da tRNA—sono emersi come potenti regolatori nel cancro. Gli autori si sono concentrati su uno di questi frammenti, tRF-3005a, dopo aver sequenziato campioni tumorali di pazienti con cancro gastrico. Hanno scoperto che tRF-3005a è molto più abbondante nei tessuti tumorali rispetto al tessuto gastrico sano adiacente, e che livelli più elevati si associano a tumori più grandi, maggiore invasione, coinvolgimento dei linfonodi e peggior sopravvivenza complessiva. Esperimenti di imaging hanno mostrato che, a differenza delle cellule gastriche normali, tRF-3005a nelle cellule tumorali si localizza principalmente nel nucleo, il centro di comando dove i messaggi genici vengono elaborati.
Promuovere crescita, invasione e diffusione
Per verificare cosa fa concretamente tRF-3005a, il gruppo ha aumentato o bloccato i suoi livelli in una serie di linee cellulari di cancro gastrico. Quando tRF-3005a veniva potenziato, le cellule tumorali crescevano più rapidamente, formavano più colonie e mostravano una maggiore capacità di invadere membrane artificiali e migrare su superfici—comportamenti che rispecchiano l’espansione e la diffusione del tumore nell’organismo. Quando tRF-3005a veniva soppresso, questi tratti aggressivi si riducevano nettamente. Nei topi, i tumori impiantati ottenuti da cellule con livelli ridotti di tRF-3005a rimasero più piccoli e mostrarono una ridotta attività di proteine chiave legate alla crescita, confermando che il frammento di RNA promuove la crescita tumorale non solo in vitro ma anche in organismi viventi.
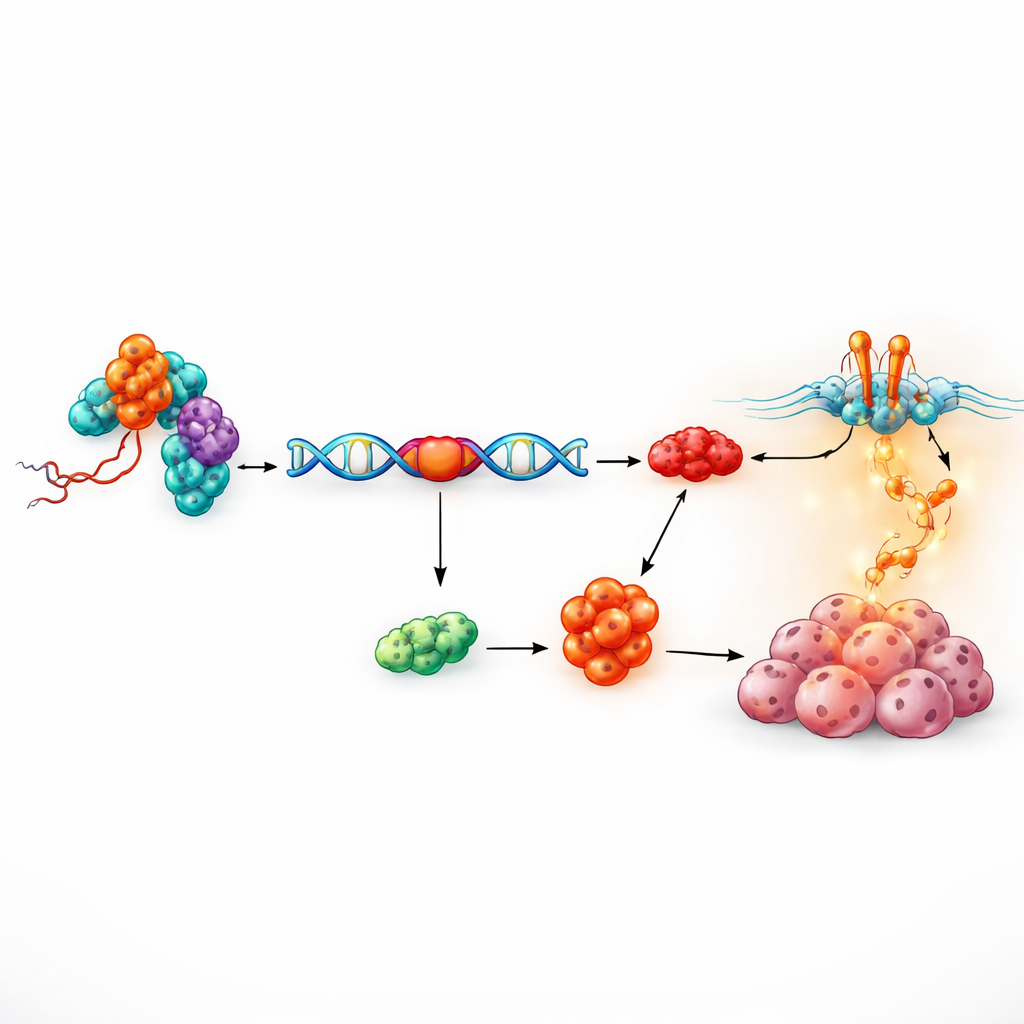
Un partner proteico che modula i messaggi genici
La domanda successiva era come un frammento di RNA di 17 nucleotidi potesse avere effetti così marcati. Usando un approccio biochimico di “pesca”, i ricercatori hanno isolato le proteine che si legano fisicamente a tRF-3005a. Tra 81 candidati, una proteina nucleare—RALY—è emersa come particolarmente rilevante. RALY fa parte di una famiglia di fattori che determinano come i messaggi genetici grezzi vengono tagliati e ricuciti, un processo noto come splicing alternativo. Un’analisi dettagliata ha mostrato che tRF-3005a si lega a una regione centrale flessibile di RALY senza modificarne la quantità complessiva, suggerendo che ne modula il comportamento piuttosto che attivarlo o disattivarlo. Esperimenti di recupero funzionale, in cui i livelli di RALY venivano aumentati o diminuiti, hanno dimostrato che l’effetto di promozione della crescita di tRF-3005a dipende strettamente da RALY, definendo un asse tRF-3005a–RALY che alimenta la proliferazione delle cellule tumorali.
Rimodellare un singolo gene per favorire una forma dannosa
Per vedere quali messaggi genici venivano rimodellati da questo asse, il team ha sequenziato l’mRNA di cellule in cui tRF-3005a era stato bloccato e ha analizzato i cambiamenti negli schemi di splicing. Gli eventi più colpiti riguardavano l’esclusione di esoni specifici, e un gene, SPAG4, è emerso come uno dei principali bersagli. SPAG4 può essere prodotto in due forme principali: una versione lunga che include l’esone 8 e una versione corta che lo esclude. I ricercatori hanno mostrato che RALY si lega principalmente alla regione intorno all’esone 8 e ne sopprime l’esclusione, spingendo le cellule a produrre più variante lunga di SPAG4. Questa forma lunga, ma non quella corta, promuoveva la crescita delle cellule tumorali. Importante, tRF-3005a rafforzava l’interazione fisica tra RALY e l’RNA di SPAG4, riducendo ulteriormente l’esclusione dell’esone 8 e spostando l’equilibrio verso la forma SPAG4-L favorevole al tumore.
Collegamento a una via di crescita importante nel cancro
A valle di SPAG4-L, lo studio ha identificato GRB14, una proteina adattatrice di segnalazione, e la nota via PI3K/AKT, che controlla la sopravvivenza e la crescita cellulare in molti tumori. Quando SPAG4-L o tRF-3005a venivano aumentati, aumentavano anche i livelli di GRB14 e l’attivazione della via PI3K/AKT, insieme alla proteina oncogenica c-Myc. Il silenziamento di GRB14 o il blocco chimico della via PI3K/AKT attenuavano il potenziamento della crescita indotto da tRF-3005a o SPAG4-L, mentre il ripristino di GRB14 invertiva questo effetto. Questi risultati supportano una catena di eventi: tRF-3005a si lega a RALY, RALY rimodella lo splicing di SPAG4 favorendo la forma lunga, e SPAG4-L attiva GRB14 e la segnalazione PI3K/AKT, promuovendo infine la divisione cellulare incontrollata.
Cosa significa per i pazienti
Nel complesso, il lavoro mostra come un minuscolo frammento di RNA possa agire come interruttore maestro di una via promotrice di tumore nei tumori gastrici. Modulando finemente una proteina dello splicing, tRF-3005a orienta un singolo gene verso una versione dannosa che alimenta un potente segnale di crescita. Poiché tRF-3005a è elevato nei tumori e associato a esiti peggiori, potrebbe fungere da biomarcatore per identificare pazienti ad alto rischio. A lungo termine, farmaci o terapie a base di RNA che bloccano tRF-3005a, interrompono la sua interazione con RALY o riportano SPAG4 verso la sua forma più sicura potrebbero offrire nuovi modi per rallentare o fermare la progressione del cancro gastrico.
Citazione: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Parole chiave: cancro gastrico, frammenti derivati da tRNA, splicing alternativo, segnalazione PI3K AKT, biomarcatori