Clear Sky Science · es
tRF-3005a regula el salto de exones de SPAG4 al interactuar con RALY para impulsar la progresión del cáncer gástrico
Por qué importa este estudio sobre el cáncer de estómago
El cáncer de estómago sigue siendo uno de los más letales a nivel mundial, en parte porque con frecuencia se detecta tarde y los tratamientos actuales no funcionan para todos. Este estudio descubre una capa de control previamente oculta dentro de las células tumorales, que involucra pequeños fragmentos de ARN y una proteína que modifica los mensajes génicos. Al revelar cómo esta asociación molecular ayuda al crecimiento de los tumores gástricos, el trabajo señala nuevos marcadores de alerta temprana y dianas terapéuticas que podrían, en el futuro, mejorar la supervivencia de los pacientes.
Pequeñas piezas de ARN con gran influencia
Durante mucho tiempo se consideró a los ARN de transferencia como simples ayudantes en la síntesis de proteínas. Sin embargo, en los últimos años han emergido pequeños fragmentos cortados de estas moléculas —llamados fragmentos derivados de ARNt— como potentes reguladores en el cáncer. Los autores se centraron en uno de esos fragmentos, tRF-3005a, tras secuenciar muestras tumorales de pacientes con cáncer gástrico. Encontraron que tRF-3005a era mucho más abundante en tejido canceroso que en el estómago sano adyacente, y que niveles más altos se asociaban con tumores de mayor tamaño, invasión más profunda, afectación de ganglios linfáticos y peor supervivencia global. Experimentos de imagen mostraron que, a diferencia de las células estomacales normales, tRF-3005a en las células cancerosas se localiza principalmente en el núcleo, el centro de control donde se procesan los mensajes génicos.
Impulsando crecimiento, invasión y diseminación
Para probar qué hace en realidad tRF-3005a, el equipo aumentó o bloqueó sus niveles en una serie de líneas celulares de cáncer gástrico. Cuando tRF-3005a se elevó, las células cancerosas crecieron más rápido, formaron más colonias y fueron más capaces de invadir membranas artificiales y migrar por superficies —comportamientos que reflejan la expansión y diseminación tumoral en el organismo. Al suprimir tRF-3005a, estos rasgos agresivos se redujeron drásticamente. En ratones, los tumores implantados a partir de células con niveles bajos de tRF-3005a permanecieron más pequeños y mostraron una menor actividad de proteínas clave relacionadas con el crecimiento, confirmando que el fragmento de ARN promueve el crecimiento tumoral no solo en placas de cultivo sino también en organismos vivos.
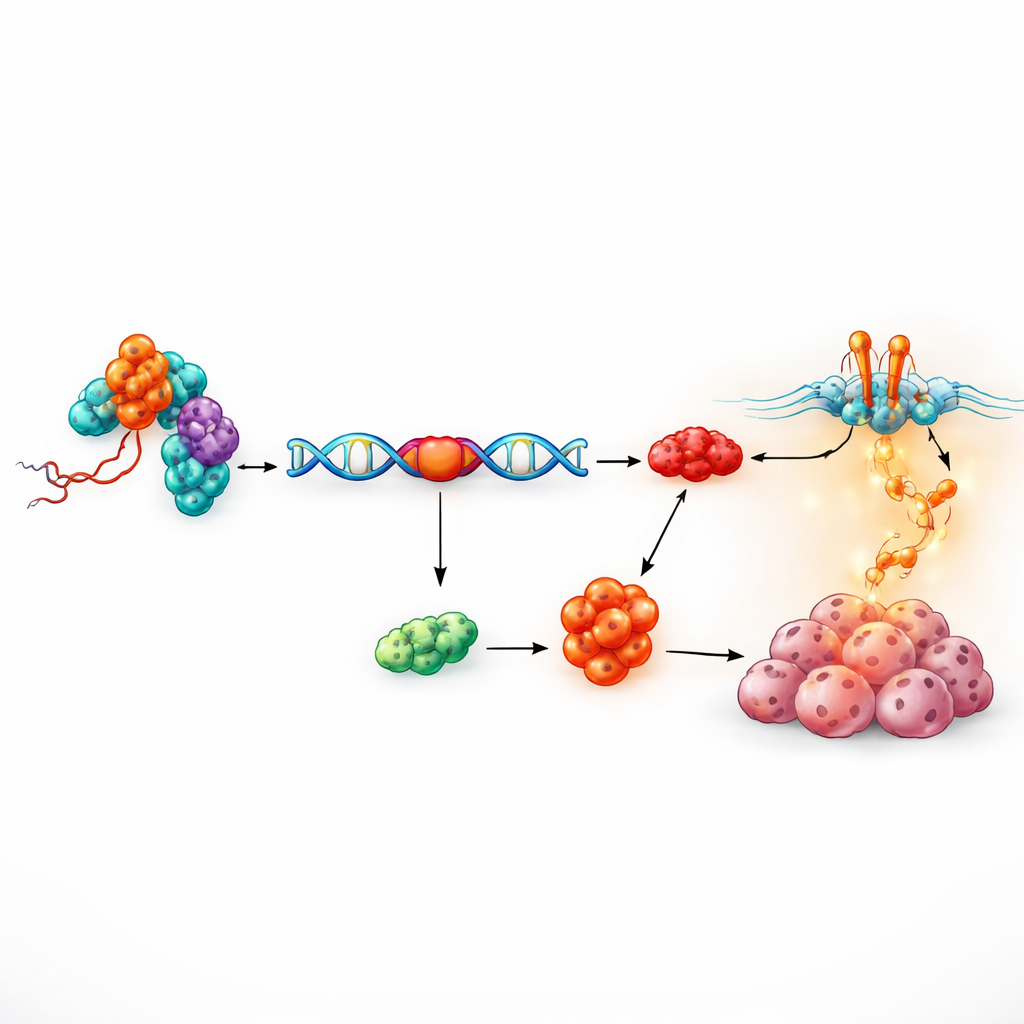
Una proteína compañera que edita mensajes génicos
La pregunta siguiente fue cómo un fragmento de ARN de 17 nucleótidos podía tener efectos tan potentes. Mediante un enfoque bioquímico de “pesca”, los investigadores identificaron proteínas que se unen físicamente a tRF-3005a. Entre 81 candidatas, destacó una proteína nuclear: RALY. RALY forma parte de una familia de factores que moldean cómo se cortan y cosen los mensajes génicos sin procesar, un proceso conocido como splicing alternativo. El mapeo detallado mostró que tRF-3005a se adhiere a una región media flexible de RALY sin alterar su cantidad total, lo que sugiere que modula el comportamiento de RALY más que activarlo o desactivarlo por completo. Experimentos de rescate funcional, en los que se aumentaron o disminuyeron los niveles de RALY, demostraron que el efecto promotor del crecimiento de tRF-3005a depende estrictamente de RALY, definiendo un eje tRF-3005a–RALY que impulsa la proliferación de las células cancerosas.
Reconfigurar un solo gen para favorecer una forma nociva
Para ver qué mensajes génicos se reconfiguran por este eje, el equipo secuenció ARNm de células en las que se bloqueó tRF-3005a y analizó los cambios en los patrones de splicing. Los eventos más afectados implicaban el salto de exones específicos, y un gen, SPAG4, emergió como uno de los principales. SPAG4 puede producirse en dos formas principales: una versión larga que incluye el exón 8 y una versión corta que lo omite. Los investigadores demostraron que RALY se une principalmente a la región en torno al exón 8 y suprime su omisión, empujando a las células a producir más de la variante larga de SPAG4. Esta forma larga, pero no la corta, promovió el crecimiento de las células cancerosas. De forma importante, tRF-3005a fortaleció la interacción física entre RALY y el ARN de SPAG4, reduciendo aún más el salto del exón 8 y favoreciendo el balance hacia la forma SPAG4-L promotora del tumor.
Vínculo con una vía principal de crecimiento en el cáncer
En la cascada que sigue a SPAG4-L, el estudio identificó a GRB14, una proteína adaptadora de señalización, y la conocida vía PI3K/AKT, que controla la supervivencia y el crecimiento celular en muchos cánceres. Cuando aumentaron SPAG4-L o tRF-3005a, subieron los niveles de GRB14 y de PI3K/AKT activada, junto con la proteína oncogénica c-Myc. Silenciar GRB14 o bloquear químicamente PI3K/AKT atenuó el impulso de crecimiento causado por tRF-3005a o SPAG4-L, mientras que restaurar GRB14 revirtió ese efecto. Estos resultados apoyan una cadena de eventos: tRF-3005a se une a RALY, RALY remodela el splicing de SPAG4 para favorecer la forma larga, y SPAG4-L activa GRB14 y la señalización PI3K/AKT, promoviendo finalmente la división celular descontrolada.
Qué implica esto para los pacientes
En conjunto, el trabajo revela cómo un diminuto fragmento de ARN puede actuar como un interruptor maestro de una vía promotora del cáncer en tumores gástricos. Al afinar la actividad de una proteína de splicing, tRF-3005a dirige un único gen hacia una versión dañina que alimenta una potente señal de crecimiento. Dado que tRF-3005a está elevado en tumores y se asocia con peores desenlaces, podría servir como biomarcador para identificar a pacientes de alto riesgo. A más largo plazo, fármacos o terapias basadas en ARN que bloqueen tRF-3005a, interrumpan su interacción con RALY o desplacen a SPAG4 hacia su forma más segura podrían ofrecer nuevas maneras de frenar o detener la progresión del cáncer de estómago.
Cita: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Palabras clave: cáncer gástrico, fragmentos derivados de ARNt, splicing alternativo, señalización PI3K AKT, biomarcadores