Clear Sky Science · pl
tRF-3005a reguluje pomijanie egzonu w SPAG4 poprzez interakcję z RALY, napędzając progresję raka żołądka
Dlaczego to badanie nad rakiem żołądka ma znaczenie
Rak żołądka pozostaje jednym z najgroźniejszych nowotworów na świecie, częściowo dlatego, że bywa wykrywany późno, a dostępne terapie nie działają u wszystkich. To badanie ujawnia wcześniej ukryty poziom kontroli w komórkach nowotworowych, obejmujący drobne fragmenty RNA oraz białko modyfikujące przekazy genetyczne. Pokazując, jak to molekularne partnerstwo wspiera wzrost guzów żołądka, praca wskazuje nowe wczesne markery ostrzegawcze i cele terapeutyczne, które w przyszłości mogą poprawić przeżycie pacjentów.
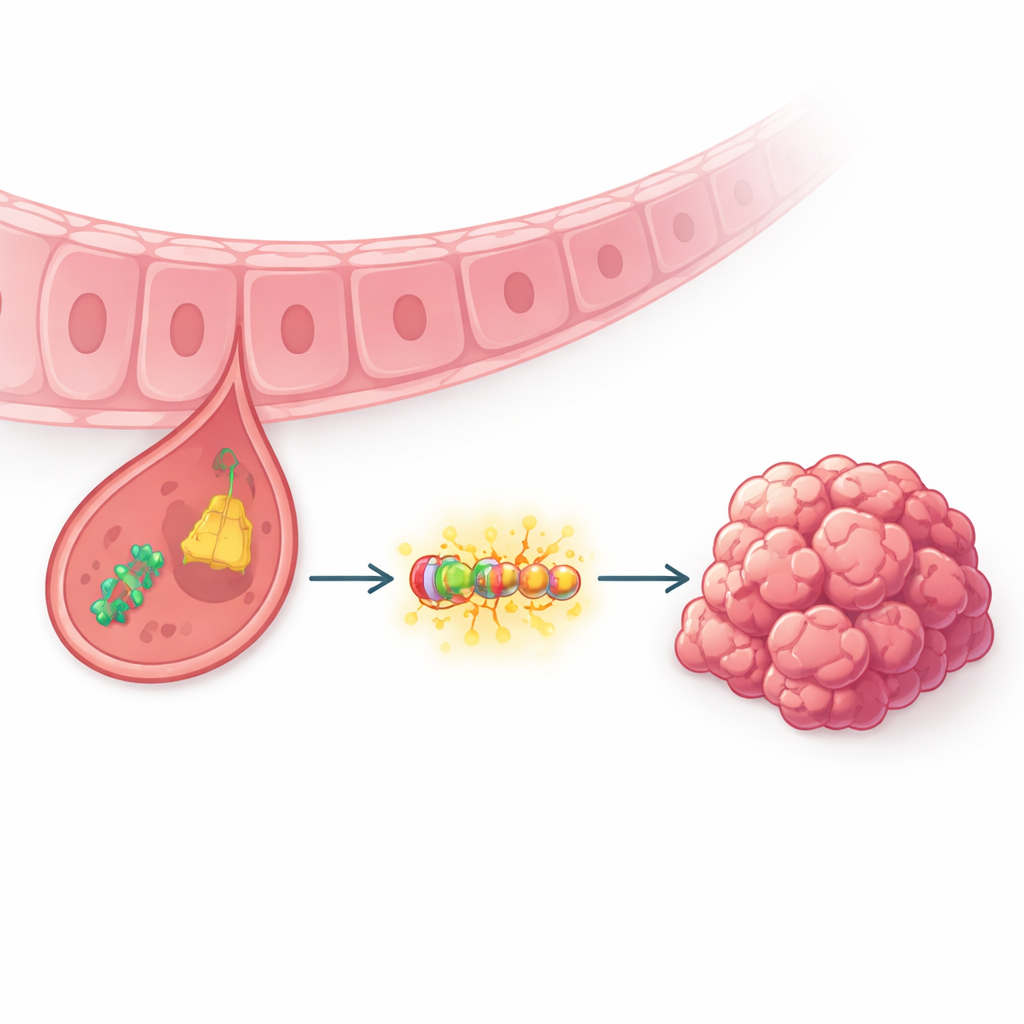
Maleńkie kawałki RNA o dużym wpływie
Naukowcy od dawna traktowali tRNA jako proste pomocniki przy budowie białek. W ostatnich latach jednak z tych cząsteczek wycinane małe fragmenty — zwane fragmentami pochodzącymi z tRNA — okazały się silnymi regulatorami w raku. Autorzy skupili się na jednym z takich fragmentów, tRF-3005a, po przesekwencjonowaniu próbek guzów od pacjentów z rakiem żołądka. Stwierdzili, że tRF-3005a był znacznie bardziej obfity w tkance nowotworowej niż w pobliskiej zdrowej tkance żołądka, a wyższe poziomy wiązały się z większymi guzami, głębszą inwazją, zajęciem węzłów chłonnych i gorszym ogólnym przeżyciem. Badania obrazowe wykazały, że w przeciwieństwie do normalnych komórek żołądka, tRF-3005a w komórkach raka lokalizuje się głównie w jądrze, centrum dowodzenia, gdzie przetwarzane są przekazy genetyczne.
Napędzanie wzrostu, inwazji i przerzutów
Aby sprawdzić, co tRF-3005a rzeczywiście robi, zespół zwiększał albo blokował jego poziomy w panelu linii komórkowych raka żołądka. Gdy tRF-3005a był podwyższony, komórki nowotworowe rosły szybciej, tworzyły więcej kolonii i wykazywały większą zdolność do inwazji przez sztuczne membrany oraz migracji po powierzchniach — zachowania odzwierciedlające ekspansję i rozprzestrzenianie się guza w organizmie. Gdy tRF-3005a został zahamowany, cechy te uległy wyraźnemu osłabieniu. U myszy implantowane guzy z komórek o obniżonym tRF-3005a pozostawały mniejsze i wykazywały zmniejszoną aktywność kluczowych białek związanych z wzrostem, potwierdzając, że fragment RNA promuje rozwój guza nie tylko in vitro, lecz także in vivo.
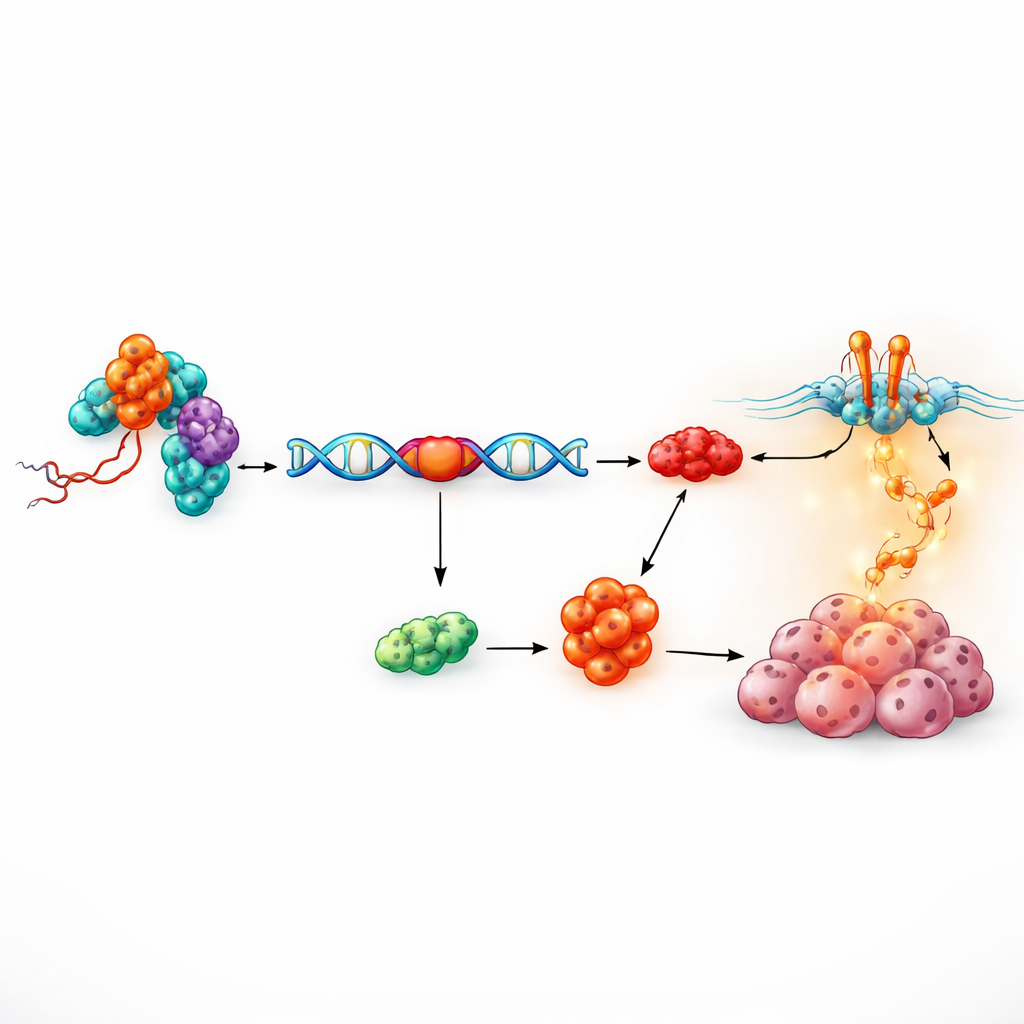
Białkowy partner, który modyfikuje przekazy genetyczne
Następne pytanie brzmiało, jak fragment RNA liczący 17 nukleotydów może mieć tak silne efekty. Stosując biochemiczne „łowienie”, badacze wyizolowali białka, które fizycznie wiążą się z tRF-3005a. Spośród 81 kandydatów wyróżniło się jedno białko jądrowe — RALY. RALY należy do rodziny czynników wpływających na to, jak surowe komunikaty genowe są cięte i sklejane, proces znany jako splicing alternatywny. Szczegółowe mapowanie pokazało, że tRF-3005a wiąże się z elastycznym środkowym regionem RALY bez zmiany jego ogólnej ilości, co sugeruje, że raczej dostraja zachowanie RALY niż go po prostu aktywuje lub hamuje. Eksperymenty przywracania funkcji, w których poziomy RALY były podnoszone lub obniżane, wykazały, że efekt promujący wzrost zależy ściśle od RALY, definiując oś tRF-3005a–RALY napędzającą proliferację komórek nowotworowych.
Przeprogramowanie pojedynczego genu na korzyść szkodliwej postaci
Aby ustalić, które przekazy genowe są przebudowywane przez tę oś, zespół zsekwencjonował mRNA z komórek, w których tRF-3005a był zablokowany, i przeanalizował zmiany w wzorcach splicingu. Najsilniej dotknięte były zdarzenia polegające na pomijaniu konkretnych egzonych, a jednym z najważniejszych genów okazał się SPAG4. SPAG4 może występować w dwóch głównych formach: długiej zawierającej egz 8 oraz krótszej, pomijającej ten egz 8. Badacze pokazali, że RALY wiąże się głównie z regionem wokół egzonu 8 i hamuje jego pomijanie, przesuwając produkcję w kierunku dłuższego wariantu SPAG4. Ta długa forma, a nie krótka, napędzała wzrost komórek nowotworowych. Co istotne, tRF-3005a wzmacniał fizyczną interakcję między RALY a RNA SPAG4, dalej ograniczając pomijanie egzonu 8 i przechylając równowagę na korzyść nowotworowo-promującej formy SPAG4-L.
Powiązanie z główną ścieżką wzrostu w raku
W dół kaskady od SPAG4-L badanie wskazało GRB14 — białko adaptorowe sygnalizacji — oraz dobrze znany szlak PI3K/AKT, który kontroluje przeżycie i wzrost komórek w wielu nowotworach. Gdy SPAG4-L lub tRF-3005a były zwiększone, wzrastały poziomy GRB14 oraz aktywowanego PI3K/AKT, wraz z onkoproteiną c-Myc. Wyciszenie GRB14 lub chemiczne zablokowanie PI3K/AKT osłabiało przyrost wzrostu wywołany przez tRF-3005a lub SPAG4-L, natomiast przywrócenie GRB14 odwracało ten efekt. Wyniki te wspierają łańcuch zdarzeń: tRF-3005a wiąże RALY, RALY przebudowuje splicing SPAG4 na korzyść długiej formy, a SPAG4-L aktywuje GRB14 i sygnalizację PI3K/AKT, ostatecznie napędzając niekontrolowane podziały komórkowe.
Co to oznacza dla pacjentów
Podsumowując, praca ujawnia, jak malutki fragment RNA może działać jako główny przełącznik dla szlaku sprzyjającego rakowi w guzach żołądka. Poprzez precyzyjne dostrajanie białka splicingowego, tRF-3005a kieruje pojedynczy gen w stronę szkodliwej formy, która wzmacnia silny sygnał wzrostu. Ponieważ tRF-3005a jest podwyższony w guzach i powiązany z gorszymi wynikami, może służyć jako biomarker do identyfikacji pacjentów o wysokim ryzyku. W dłuższej perspektywie leki lub terapie oparte na RNA, które blokują tRF-3005a, zaburzają jego interakcję z RALY lub przesuwają splicing SPAG4 z powrotem w kierunku bezpieczniejszej formy, mogłyby stanowić nowe sposoby spowolnienia lub zatrzymania progresji raka żołądka.
Cytowanie: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Słowa kluczowe: rak żołądka, fragmenty pochodzące z tRNA, splicing alternatywny, szlak PI3K AKT, biomarkery