Clear Sky Science · fr
tRF-3005a régule l’exclusion d’exon de SPAG4 en interagissant avec RALY pour favoriser la progression du cancer gastrique
Pourquoi cette étude sur le cancer de l’estomac est importante
Le cancer de l’estomac reste l’un des cancers les plus mortels au monde, en partie parce qu’il est souvent détecté tardivement et que les traitements actuels ne fonctionnent pas pour tous les patients. Cette étude met au jour un niveau de contrôle jusque-là caché à l’intérieur des cellules tumorales, impliquant de minuscules fragments d’ARN et une protéine qui édite les messages génétiques. En révélant comment ce partenariat moléculaire favorise la croissance des tumeurs gastriques, le travail pointe vers de nouveaux marqueurs d’alerte précoce et des cibles thérapeutiques susceptibles d’améliorer un jour la survie des patients.
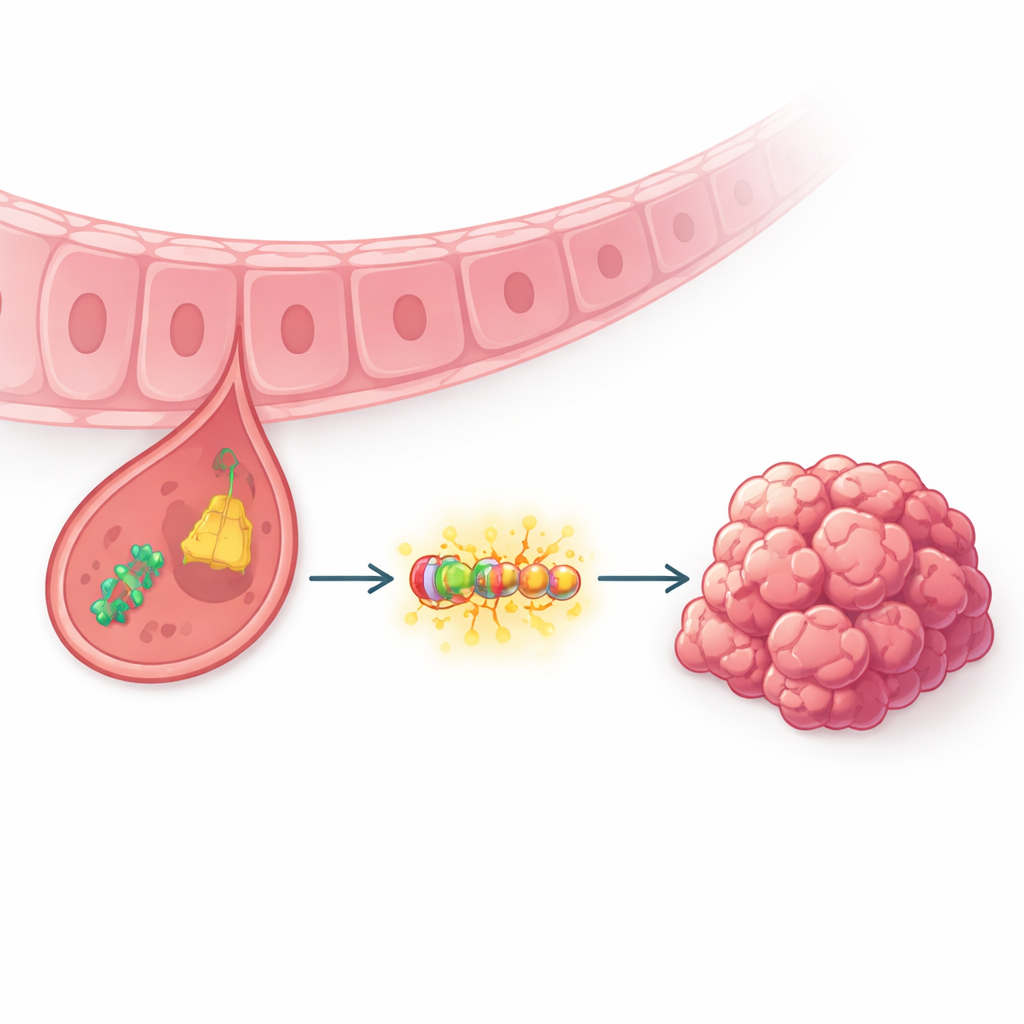
De petits morceaux d’ARN au pouvoir important
Les chercheurs ont longtemps considéré les ARN de transfert comme de simples auxiliaires de la synthèse protéique. Ces dernières années, toutefois, de petits fragments découpés à partir de ces molécules — appelés fragments dérivés d’ARNt — sont apparus comme de puissants régulateurs dans le cancer. Les auteurs se sont concentrés sur l’un de ces fragments, tRF-3005a, après avoir séquencé des échantillons tumoraux de patients atteints de cancer gastrique. Ils ont constaté que tRF-3005a était beaucoup plus abondant dans les tissus cancéreux que dans les tissus gastriques sains adjacents, et que des niveaux plus élevés étaient associés à des tumeurs plus volumineuses, une invasion plus profonde, une dissémination ganglionnaire et une survie globale plus courte. Des expériences d’imagerie ont montré que, contrairement aux cellules gastriques normales, tRF-3005a dans les cellules cancéreuses se localise principalement dans le noyau, le centre de commande où les messages génétiques sont traités.
Favoriser la croissance, l’invasion et la dissémination
Pour tester l’effet réel de tRF-3005a, l’équipe a augmenté ou bloqué ses niveaux dans un panel de lignées cellulaires de cancer gastrique. Lorsque tRF-3005a était surproduit, les cellules cancéreuses proliféraient plus vite, formaient davantage de colonies et montraient une capacité accrue à envahir des membranes artificielles et à migrer sur des surfaces — des comportements qui reflètent l’expansion et la dissémination tumorales in vivo. Lorsque tRF-3005a était supprimé, ces traits agressifs diminuaient fortement. Chez la souris, les tumeurs implantées à partir de cellules avec des niveaux réduits de tRF-3005a restaient plus petites et présentaient une activité réduite de protéines clés liées à la croissance, confirmant que ce fragment d’ARN favorise la croissance tumorale non seulement in vitro, mais aussi chez des organismes vivants.
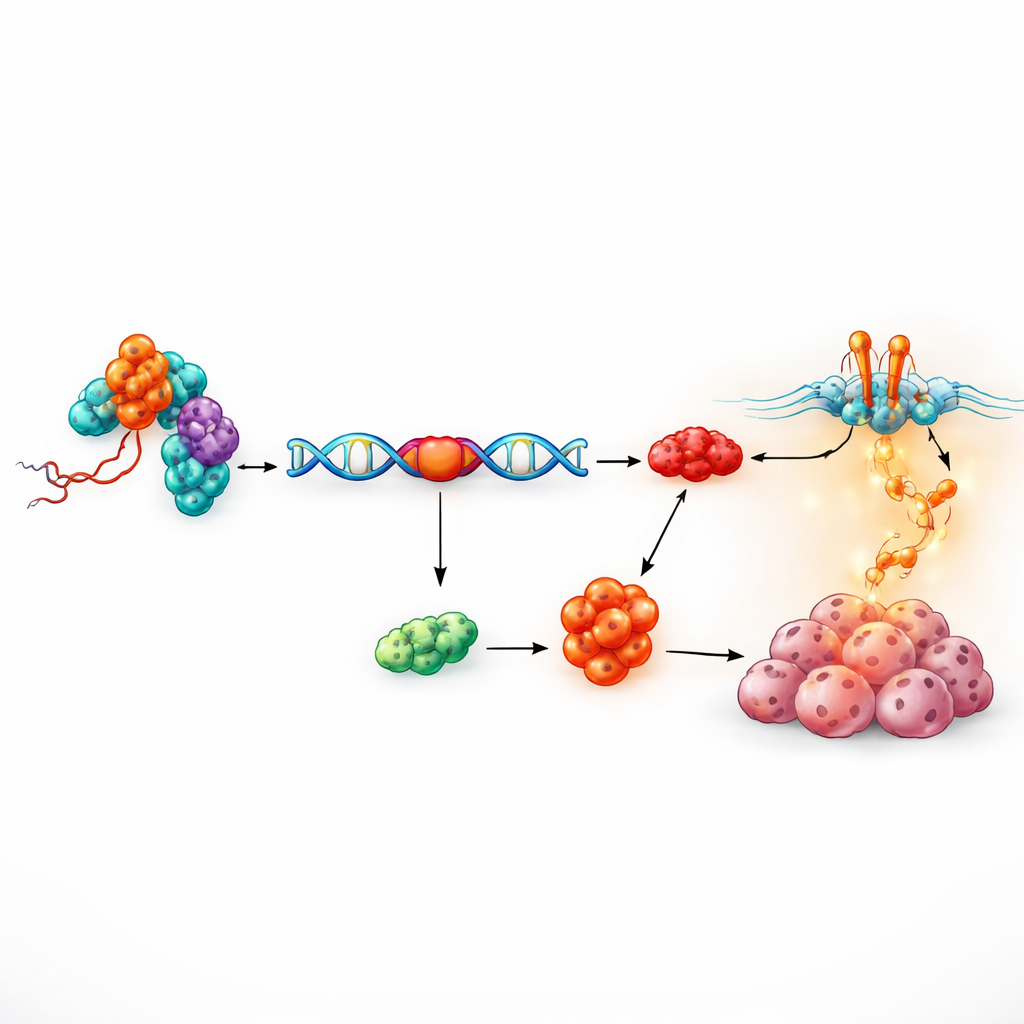
Un partenaire protéique qui édite les messages génétiques
La question suivante était de comprendre comment un fragment d’ARN de 17 nucléotides pouvait produire des effets aussi marqués. Grâce à une approche biochimique de type « pêche », les chercheurs ont isolé les protéines qui se lient physiquement à tRF-3005a. Parmi 81 candidats, une protéine nucléaire — RALY — s’est distinguée. RALY fait partie d’une famille de facteurs qui façonnent la manière dont les messages génétiques bruts sont découpés et assemblés, un processus connu sous le nom d’épissage alternatif. Un cartographage détaillé a montré que tRF-3005a se fixe principalement à une région médiane flexible de RALY sans en modifier la quantité globale, ce qui suggère qu’il module le comportement de RALY plutôt que de l’activer ou de l’inhiber simplement. Des expériences de réparation fonctionnelle, où les niveaux de RALY étaient augmentés ou diminués, ont montré que l’effet promoteur de croissance de tRF-3005a dépend strictement de RALY, définissant un axe tRF-3005a–RALY qui alimente la prolifération des cellules cancéreuses.
Modifier l’épissage d’un gène pour favoriser une forme nuisible
Pour identifier les messages génétiques remodelés par cet axe, l’équipe a séquencé l’ARNm de cellules dans lesquelles tRF-3005a était bloqué et a analysé les changements dans les schémas d’épissage. Les événements les plus affectés concernaient l’exclusion d’exons spécifiques, et un gène, SPAG4, est apparu comme un élément majeur. SPAG4 peut être produit sous deux formes principales : une version longue qui inclut l’exon 8 et une version courte qui l’exclut. Les chercheurs ont montré que RALY se lie principalement à la région entourant l’exon 8 et empêche son exclusion, poussant les cellules à produire davantage de la variante longue de SPAG4. Cette forme longue, mais pas la forme courte, stimule la croissance des cellules cancéreuses. Fait important, tRF-3005a renforce l’interaction physique entre RALY et l’ARN de SPAG4, réduisant encore l’exclusion de l’exon 8 et faisant pencher l’équilibre vers la forme SPAG4-L promotrice de tumeur.
Lien avec une voie majeure de croissance dans le cancer
En aval de SPAG4-L, l’étude a identifié GRB14, une protéine adaptatrice de signalisation, et la voie bien connue PI3K/AKT, qui contrôle la survie et la croissance cellulaires dans de nombreux cancers. Lorsque SPAG4-L ou tRF-3005a étaient augmentés, les niveaux de GRB14 et de PI3K/AKT activée augmentaient, de même que la protéine oncogénique c-Myc. L’inhibition de GRB14 ou le blocage chimique de PI3K/AKT atténuaient l’accroissement de croissance induit par tRF-3005a ou SPAG4-L, tandis que la restauration de GRB14 inversait cet effet. Ces résultats soutiennent une chaîne d’événements : tRF-3005a se lie à RALY, RALY reprogramme l’épissage de SPAG4 pour favoriser la forme longue, et SPAG4-L active GRB14 et la signalisation PI3K/AKT, conduisant en fin de compte à une division cellulaire incontrôlée.
Ce que cela signifie pour les patients
Dans l’ensemble, ce travail révèle comment un minuscule fragment d’ARN peut agir comme un commutateur maître d’une voie promotrice de cancer dans les tumeurs gastriques. En ajustant finement une protéine d’épissage, tRF-3005a oriente un gène unique vers une version néfaste qui alimente un signal de croissance puissant. Comme tRF-3005a est élevé dans les tumeurs et associé à de moins bons pronostics, il pourrait servir de biomarqueur pour identifier les patients à haut risque. À plus long terme, des médicaments ou des thérapies à base d’ARN visant à bloquer tRF-3005a, perturber son interaction avec RALY ou réorienter SPAG4 vers sa forme plus sûre pourraient offrir de nouvelles façons de ralentir ou d’arrêter la progression du cancer gastrique.
Citation: Cui, H., Yuan, Y., Yin, Y. et al. tRF-3005a regulates exon skipping of SPAG4 by interacting with RALY to drive gastric cancer progression. Cell Death Discov. 12, 169 (2026). https://doi.org/10.1038/s41420-026-03049-3
Mots-clés: cancer de l’estomac, fragments dérivés de l’ARNt, épissage alternatif, signalisation PI3K AKT, biomarqueurs