Clear Sky Science · pl
Wspólne modelowanie heterogeniczności komórek i efektów warunków za pomocą scPCA w pojedynczo-komórkowym RNA-seq
Dlaczego to ma znaczenie dla zrozumienia komórek
Współczesna biologia potrafi odczytać, które geny są aktywne w tysiącach pojedynczych komórek jednocześnie. Gdy naukowcy porównują komórki pomiędzy różnymi traktowaniami, wiekiem czy tle genetycznym, ogrom danych staje się przytłaczający, a techniczne niuanse łatwo mogą ukryć rzeczywiste zmiany biologiczne. W artykule wprowadzono nowe narzędzie analityczne, scPCA, które pomaga badaczom rozdzielić to, co naprawdę zmienia się w komórkach w różnych warunkach, od naturalnej różnorodności występującej między typami komórek.
Z zaszumionych danych komórkowych do wyraźnych wzorców
Pojedynczo-komórkowe sekwencjonowanie RNA mierzy aktywność tysięcy genów w każdej komórce, dając bardzo wysokowymiarowe dane. Aby je zrozumieć, badacze zazwyczaj kompresują dane metodami takimi jak analiza głównych składowych (PCA), która znajduje niewielki zestaw „osi” uchwycających główne wzorce zmienności. Tradycyjne podejścia jednak mieszają ze sobą dwie różne źródła zmienności: wrodzone różnice między typami komórek oraz zmiany wywołane eksperymentem, np. leczeniem lekiem. Autorzy argumentują, że takie wymieszanie może mylić dalsze analizy, jak grupowanie komórek według typów czy poszukiwanie efektów leczenia.
Nowy sposób współdzielenia struktury między warunkami
scPCA rozwiązuje ten problem poprzez jawne wskazanie modelowi faktoryzacji, z którego warunku pochodzi każda komórka, a następnie uczenie oddzielnego — lecz powiązanego — zestawu wzorców ekspresji genów dla każdego warunku. Zamiast wymuszać, by wszystkie próbki współdzieliły dokładnie tę samą strukturę, scPCA pozwala każdemu warunkowi mieć własną wersję każdej składowej, delikatnie przesuniętą względem wyznaczonego warunku referencyjnego. Zachowuje to wspólny układ odniesienia do porównywania komórek między warunkami, jednocześnie wychwytując systematyczne przesunięcia ekspresji wywołane leczeniem, starzeniem czy zmianami genetycznymi.
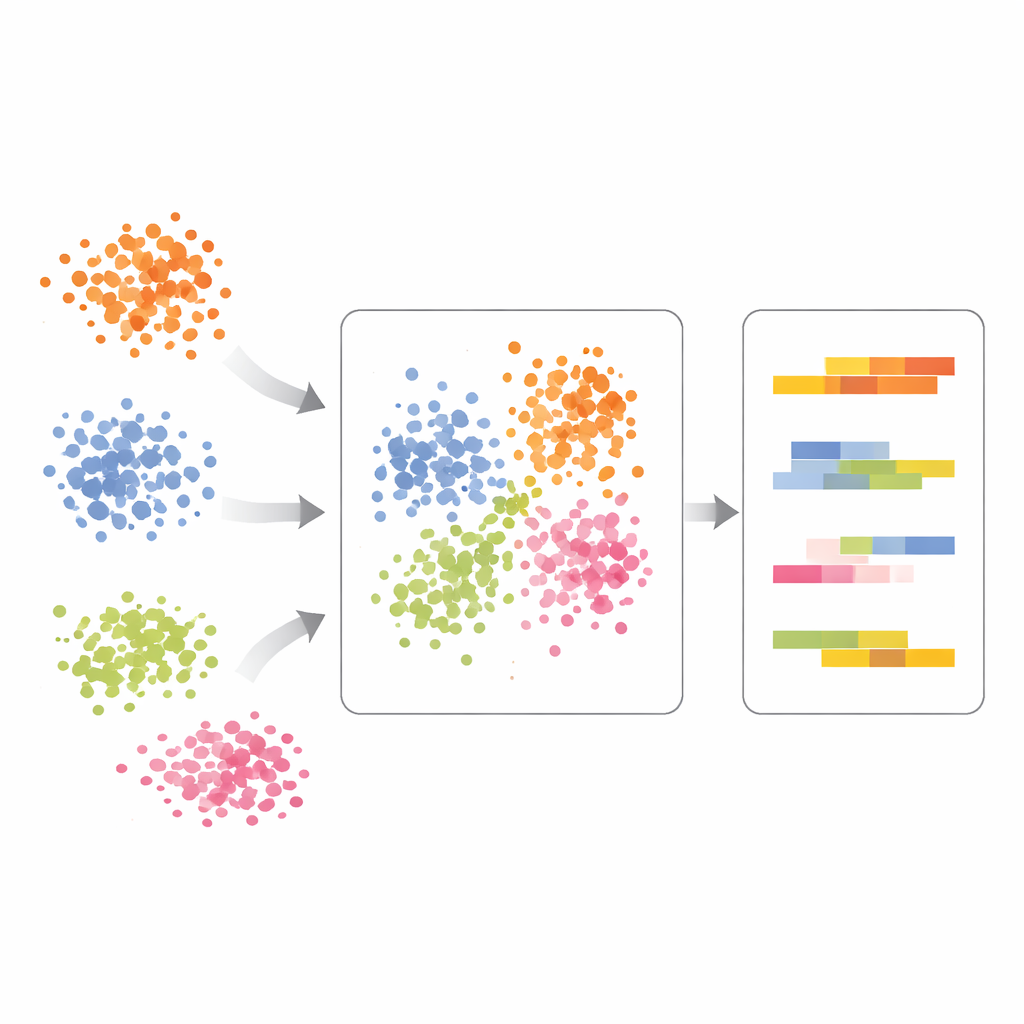
Wykrywanie rzeczywistych efektów leczenia w komórkach odpornościowych
Autorzy pokazują działanie scPCA na komórkach odpornościowych od pacjentów z toczniem, część pozostawiono bez leczenia, a część stymulowano interferonem-beta — silnym sygnałem immunologicznym. Standardowa analiza powodowała grupowanie komórek zarówno według typu komórki, jak i leczenia, co utrudniało interpretację. Dzięki scPCA komórki tego samego typu z różnych warunków wyrównywały się znacznie lepiej, ujawniając, że główna oś zmienności nadal odzwierciedlała linię komórek odpornościowych, a nie tylko efekt leczenia. Dopiero po uwzględnieniu typu komórki scPCA uwydatniła przesunięcia ekspresji wywołane leczeniem w konkretnych genach komórek mieloidalnych, w tym związanych z sygnalizacją interferonową i zmienionym przetwarzaniem białek wewnątrzkomórkowym. Pokazało to, że metoda potrafi czysto oddzielić to, kim są komórki, od tego, jak na coś reagują.
Rozplątywanie artefaktów technicznych i efektów starzenia
Eksperymenty często cierpią z powodu efektów partii: subtelnych różnic wywołanych przetwarzaniem próbek, a nie biologią. Na mieszance dwóch ludzkich linii komórkowych mierzonych w oddzielnych porcjach autorzy pokazują, że standardowa PCA zachowuje te techniczne różnice, podczas gdy scPCA może je w dużej mierze usunąć, traktując partię jako zmienną warunkującą. Metoda ujawnia wtedy, które geny odpowiadały za pozorny podział według partii, w tym markery specyficzne dla każdej linii komórkowej. W bardziej złożonym przykładzie scPCA zastosowano do komórek płuca młodych i starych myszy. Znajduje składowe zgodne z głównymi typami komórek — takimi jak pneumocyty, komórki migawkowe, makrofagi i limfocyty T — a następnie wskazuje zmiany ekspresji związane z wiekiem w każdym z nich, w tym geny stresu i odpowiedzi immunologicznej, które pasują do koncepcji „inflammaging”.
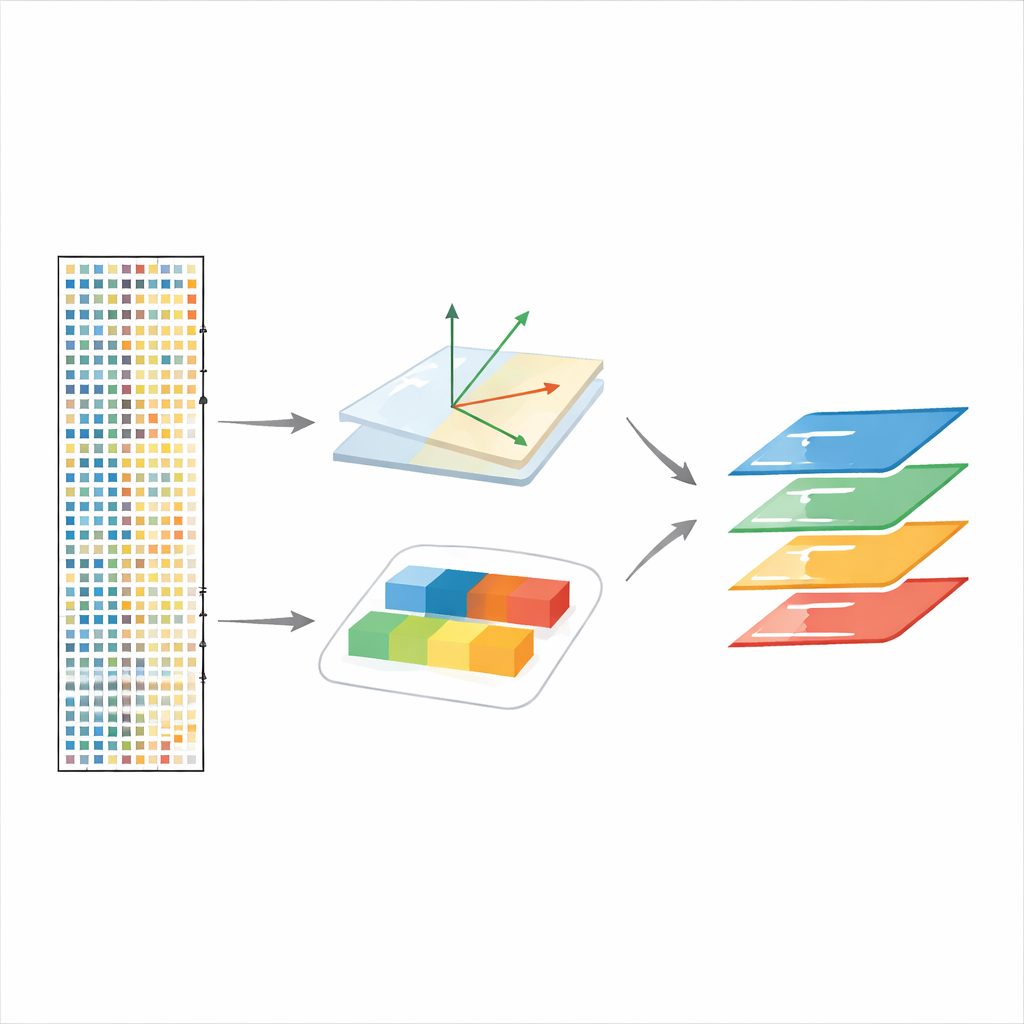
Śledzenie odpowiedzi komórek w czasie i przy różnych perturbacjach
scPCA radzi sobie także z eksperymentami mającymi więcej niż dwa warunki, na przykład neurony w korze wzrokowej myszy eksponowane na światło po okresie ciemności. Traktując punkty czasowe jako różne poziomy warunku, metoda odzyskuje wczesne i późne fale aktywności genów w kilku typach komórek mózgowych, oddzielając szybkie czynniki „wczesnej odpowiedzi” od wolniejszych programów „późnej odpowiedzi”. W doświadczeniu na danio pręgowanym, w którym kluczowy gen rozwojowy chordin jest usunięty, scPCA skutecznie integruje embriony pomimo dużych zmian w składzie typów komórek i ujawnia zmiany transkrypcyjne zgodne ze zmienionym wzorem ciała, w tym geny, które nie były podkreślone w oryginalnej analizie.
Co to oznacza dla przyszłych badań pojedynczych komórek
Mówiąc prostym językiem, scPCA daje badaczom wyraźniejszą soczewkę do oglądania danych pojedynczych komórek zbieranych w różnych warunkach. Tworzy zintegrowane mapy, w których podobne komórki ustawiają się w linii między traktowaniami, i wskazuje, które geny w każdym współdzielonym wzorcu są włączane lub wyciszane w odpowiedzi na bodziec, starzenie czy zmianę genetyczną. Metoda zakłada, że struktura leżąca u podstaw jest w dużej mierze współdzielona i najlepiej nadaje się do prac eksploracyjnych, które nadal wymagają dodatkowej walidacji, lecz oferuje bardziej przejrzystą i interpretowalną alternatywę dla wielu modeli typu czarna skrzynka. Powinno to pomóc naukowcom wyciągać bardziej wiarygodne wnioski z coraz bardziej złożonych badań pojedynczych komórek.
Cytowanie: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Słowa kluczowe: sekwencjonowanie RNA pojedynczej komórki, redukcja wymiarowości, heterogeniczność komórkowa, zmiany w ekspresji genów, efekty partii