Clear Sky Science · it
Modellizzazione congiunta dell'eterogeneità cellulare e degli effetti di condizione con scPCA in RNA-seq a singola cellula
Perché è importante per comprendere le cellule
La biologia moderna può ora leggere quali geni sono attivi in migliaia di singole cellule contemporaneamente. Ma quando gli scienziati confrontano cellule sottoposte a trattamenti diversi, età diverse o background genetici differenti, l'enorme quantità di dati può diventare travolgente e le peculiarità tecniche possono facilmente nascondere cambiamenti biologici reali. Questo articolo presenta un nuovo strumento analitico, scPCA, che aiuta i ricercatori a separare ciò che cambia realmente nelle cellule in condizioni diverse dalla diversità naturale che esiste tra i tipi cellulari.
Da dati cellulari rumorosi a pattern chiari
Il sequenziamento dell'RNA a singola cellula misura l'attività di migliaia di geni in ciascuna cellula, producendo dati a densità estremamente elevata. Per interpretarli, i ricercatori solitamente comprimono i dati con metodi come l'analisi delle componenti principali (PCA), che individua un piccolo insieme di "assi" che catturano i principali schemi di variazione. Tuttavia, gli approcci tradizionali mescolano assieme due fonti di variazione molto diverse: differenze intrinseche tra tipi cellulari e cambiamenti causati da un esperimento, come un trattamento farmacologico. Gli autori sostengono che questa mescolanza può fuorviare le analisi successive, come il clustering delle cellule in tipi o la ricerca di effetti del trattamento.
Un nuovo modo per condividere la struttura tra condizioni
scPCA affronta questo problema indicando esplicitamente al modello di fattorizzazione da quale condizione proviene ogni cellula e poi apprendendo un set separato — ma collegato — di schemi di espressione genica per ogni condizione. Invece di costringere tutti i campioni a condividere esattamente la stessa struttura sottostante, scPCA permette a ogni condizione di avere la propria versione di ciascuna componente, leggermente spostata rispetto a una condizione di riferimento designata. Questo conserva un sistema di coordinate comune per confrontare le cellule tra condizioni, pur catturando gli spostamenti sistematici di espressione indotti da trattamenti, invecchiamento o variazioni genetiche.
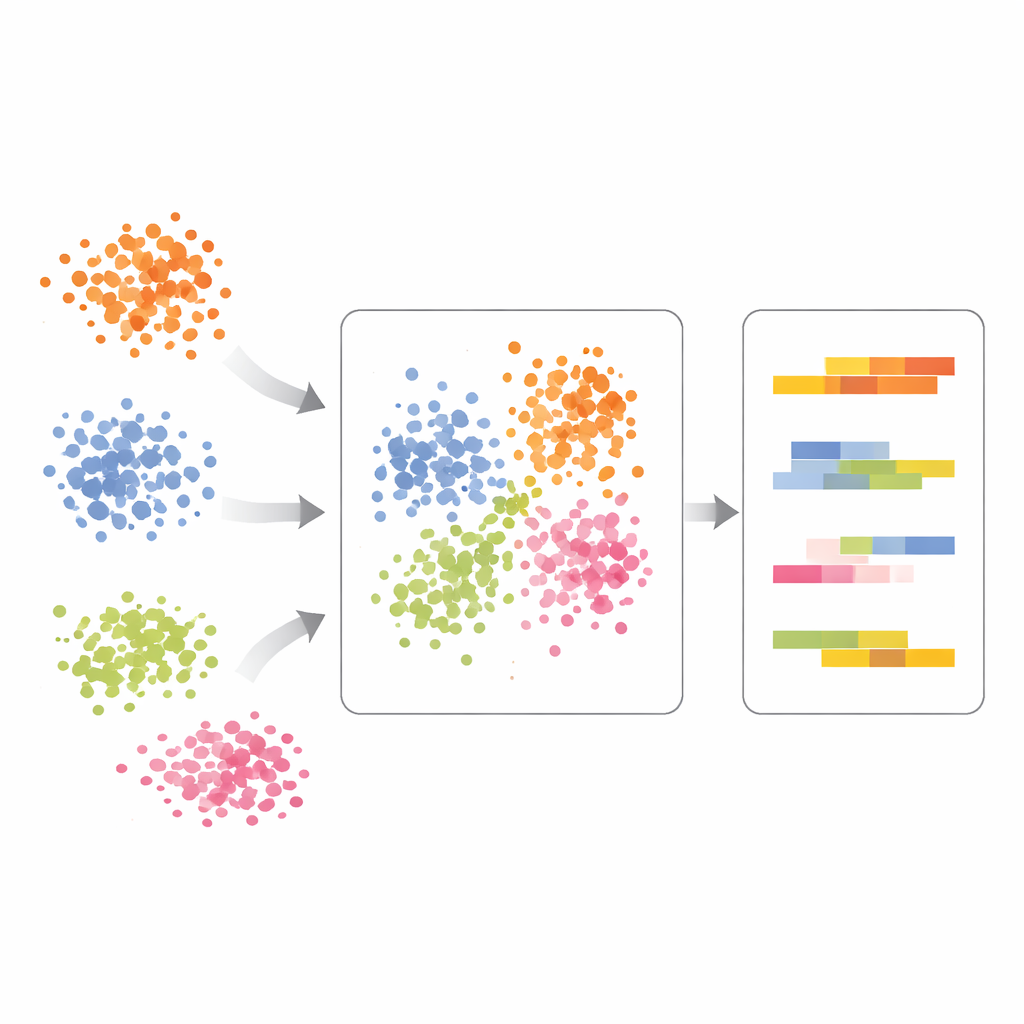
Individuare i veri effetti del trattamento nelle cellule immunitarie
Gli autori dimostrano scPCA su cellule immunitarie di pazienti con lupus, alcune non trattate e altre stimolate con interferone-beta, un forte segnale immunitario. L'analisi standard faceva raggruppare le cellule sia per tipo che per trattamento, rendendo i risultati difficili da interpretare. Con scPCA, le cellule dello stesso tipo provenienti da condizioni diverse si sono allineate molto meglio, rivelando che l'asse principale di variazione rifletteva ancora le linee cellulari immunitarie piuttosto che il trattamento da solo. Solo dopo aver tenuto conto del tipo cellulare scPCA ha evidenziato spostamenti indotti dal trattamento in geni specifici dei mieloidi, inclusi quelli legati alla segnalazione dell'interferone e alla gestione delle proteine all'interno della cellula. Questo ha mostrato che il metodo può separare in modo netto l'identità cellulare da come le cellule rispondono.
Sciogliere artefatti tecnici ed effetti dell'invecchiamento
Gli esperimenti spesso risentono di effetti di batch: differenze sottili causate dalla lavorazione dei campioni più che dalla biologia. Usando una miscela di due linee cellulari umane misurate in batch separati, gli autori mostrano che la PCA standard preserva queste differenze tecniche, mentre scPCA può rimuoverle in gran parte trattando il batch come variabile di condizionamento. Il metodo rivela quindi quali geni erano responsabili della apparente separazione per batch, inclusi marcatori specifici di ciascuna linea cellulare. In un esempio più complesso, scPCA è applicata a cellule polmonari di topi giovani e anziani. Trova componenti che si allineano con i principali tipi cellulari — come pneumociti, cellule ciliari, macrofagi e cellule T — e poi individua cambiamenti genici correlati all'età all'interno di ciascuno, inclusi geni di stress e di risposta immunitaria coerenti con il concetto di "inflammaging."
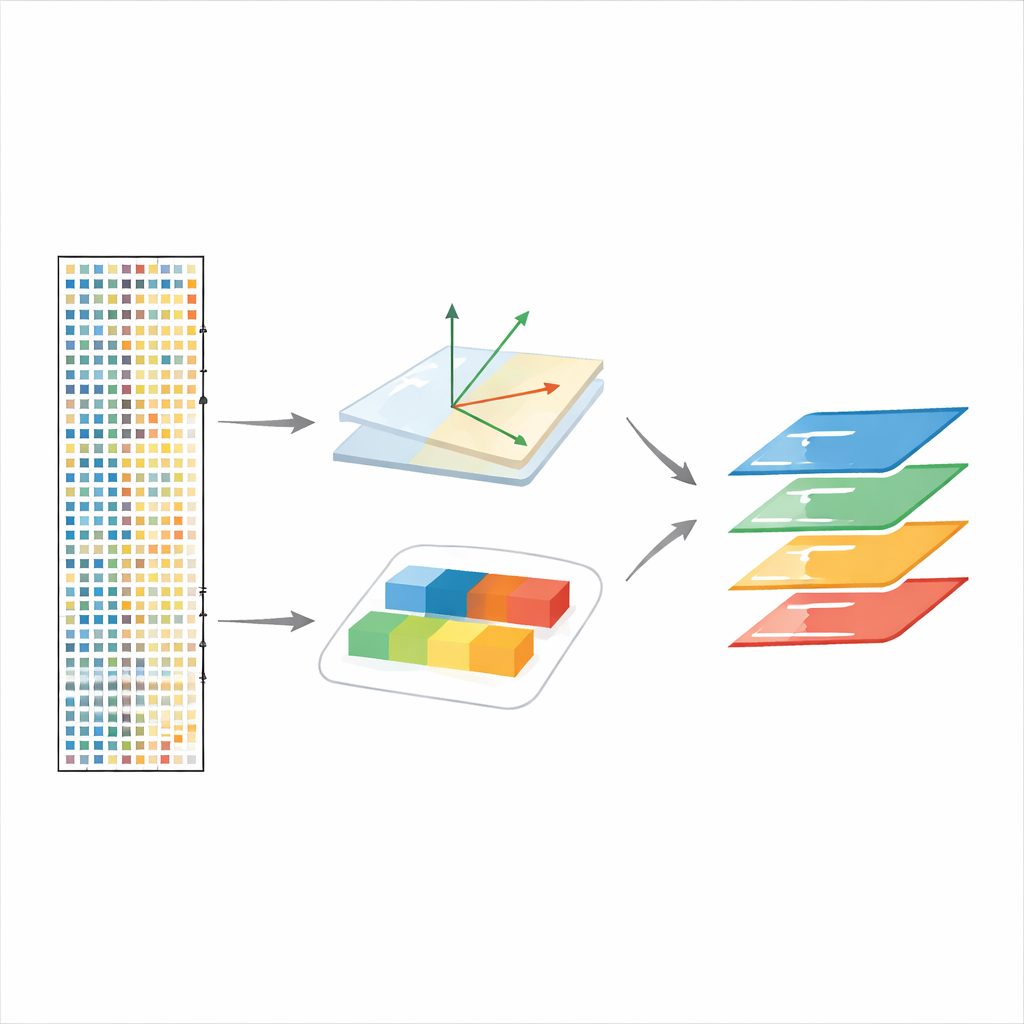
Seguirne le risposte nel tempo e attraverso perturbazioni
scPCA gestisce anche esperimenti con più di due condizioni, come neuroni nella corteccia visiva del topo esposti alla luce dopo un periodo di buio. Trattando i punti temporali come livelli diversi di una condizione, il metodo recupera onde precoci e tardive di attività genica in diversi tipi cellulari cerebrali, separando i fattori di "risposta precoce" rapida dai programmi di "risposta tardiva" più lenti. In un esperimento sul pesce zebra in cui un gene chiave dello sviluppo, chordin, viene eliminato, scPCA integra con successo gli embrioni nonostante grandi spostamenti nella composizione dei tipi cellulari e rivela cambiamenti trascrizionali coerenti con alterazioni del pattern corporeo, inclusi geni non enfatizzati nell'analisi originale.
Cosa significa per gli studi futuri a singola cellula
In termini semplici, scPCA fornisce ai ricercatori una lente più chiara per osservare i dati a singola cellula raccolti in condizioni diverse. Produce mappe integrate in cui cellule simili si allineano tra i trattamenti e mette in evidenza quali geni all'interno di ciascun pattern condiviso sono attivati o repressi in risposta a uno stimolo, all'invecchiamento o a una variazione genetica. Pur assumendo che la struttura sottostante sia in gran parte condivisa ed essendo più adatto a lavori esplorativi che richiedono comunque convalide successive, offre un'alternativa più trasparente e interpretabile rispetto a molti modelli "scatola nera". Questo dovrebbe aiutare gli scienziati a trarre conclusioni più affidabili da esperimenti a singola cellula sempre più complessi.
Citazione: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Parole chiave: sequenziamento dell'RNA a singola cellula, riduzione della dimensionalità, eterogeneità cellulare, cambiamenti nell'espressione genica, effetti di batch