Clear Sky Science · es
Modelado conjunto de la heterogeneidad celular y los efectos de la condición con scPCA en RNA-seq unicelular
Por qué esto importa para comprender las células
La biología moderna puede ahora leer qué genes están activos en miles de células individuales a la vez. Pero cuando los científicos comparan células entre diferentes tratamientos, edades o antecedentes genéticos, el volumen de datos se vuelve abrumador y las particularidades técnicas pueden ocultar con facilidad cambios biológicos reales. Este artículo presenta una nueva herramienta analítica, scPCA, que ayuda a los investigadores a desenredar qué cambia verdaderamente en las células bajo distintas condiciones frente a la diversidad natural que existe entre tipos celulares.
De datos celulares ruidosos a patrones claros
La secuenciación de ARN unicelular mide la actividad de miles de genes en cada célula, produciendo datos de dimensión extremadamente alta. Para interpretar esto, los investigadores suelen reducir la dimensionalidad con métodos como el análisis de componentes principales (PCA), que encuentra un pequeño conjunto de “ejes” que capturan los principales patrones de variación. Sin embargo, los enfoques tradicionales mezclan dos fuentes de variación muy diferentes: las diferencias inherentes entre tipos celulares y los cambios causados por un experimento, como un tratamiento farmacológico. Los autores sostienen que esta mezcla puede inducir a error análisis posteriores, como agrupar células por tipo o buscar efectos del tratamiento.
Una nueva forma de compartir estructura entre condiciones
scPCA aborda este problema indicando explícitamente al modelo de factorización de qué condición proviene cada célula y aprendiendo luego un conjunto separado —aunque vinculado— de patrones de expresión génica para cada condición. En lugar de obligar a todas las muestras a compartir exactamente la misma estructura subyacente, scPCA permite que cada condición tenga su propia versión de cada componente, desplazada suavemente respecto de una condición de referencia designada. Esto preserva un sistema de coordenadas común para comparar células entre condiciones, al tiempo que captura desplazamientos sistemáticos de la expresión impulsados por tratamientos, envejecimiento o cambios genéticos.
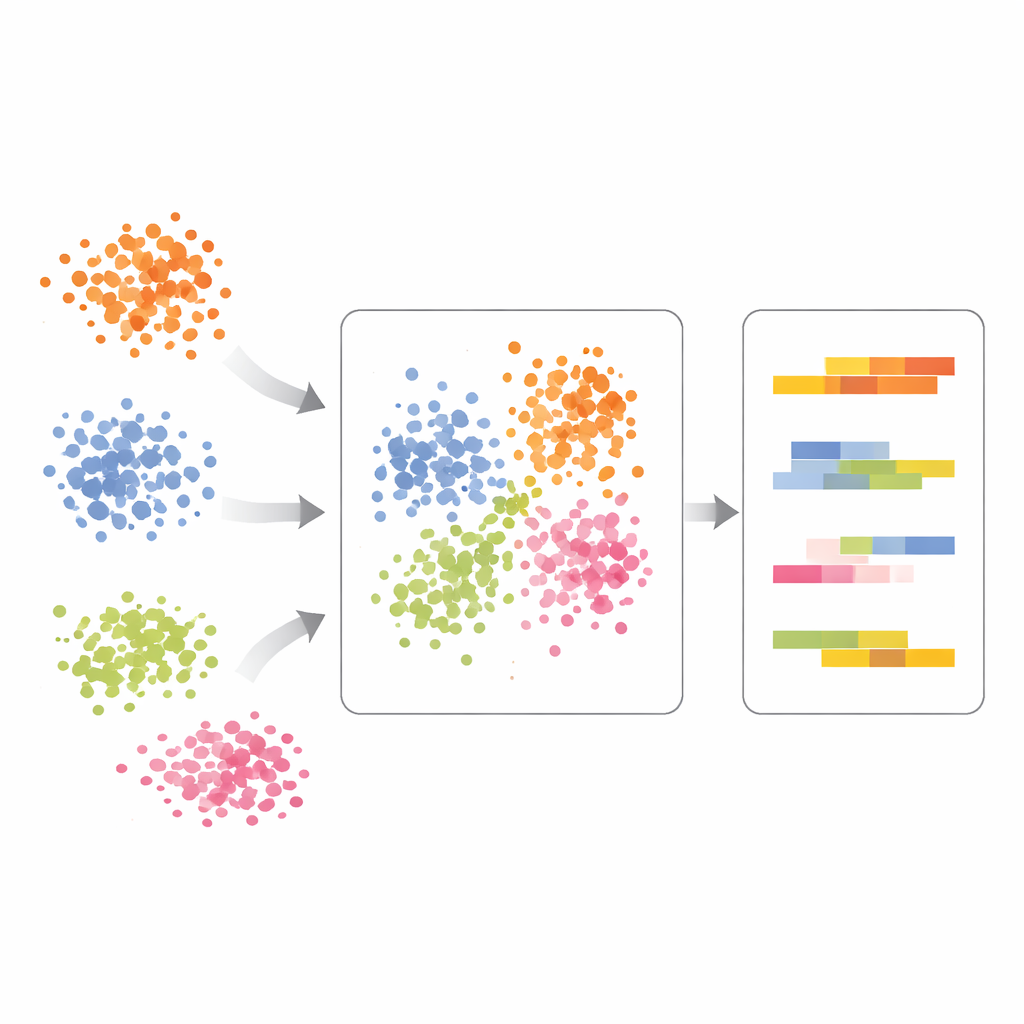
Ver los efectos reales del tratamiento en células inmunitarias
Los autores demuestran scPCA en células inmunitarias de pacientes con lupus, algunas sin tratar y otras estimuladas con interferón beta, una señal inmune potente. El análisis estándar hizo que las células se agruparan tanto por tipo celular como por tratamiento, dificultando la interpretación. Con scPCA, las células del mismo tipo procedentes de diferentes condiciones se alinearon mucho mejor, revelando que el eje principal de variación seguía reflejando las líneas celulares inmunitarias más que el tratamiento en sí. Solo después de tener en cuenta el tipo celular, scPCA destacó desplazamientos inducidos por el tratamiento en genes específicos de las células mieloides, incluidos genes ligados a la señalización por interferón y al manejo alterado de proteínas dentro de la célula. Esto mostró que el método puede separar con claridad quiénes son las células de cómo responden.
Desenredar artefactos técnicos y efectos del envejecimiento
Los experimentos suelen sufrir efectos de lote: diferencias sutiles causadas por el procesamiento de las muestras más que por la biología. Usando una mezcla de dos líneas celulares humanas medidas en lotes separados, los autores muestran que el PCA estándar preserva estas diferencias técnicas, mientras que scPCA puede eliminarlas en gran medida al tratar el lote como una variable condicionante. El método revela entonces qué genes fueron responsables de la aparente separación por lote, incluidos marcadores específicos de cada línea celular. En un ejemplo más complejo, scPCA se aplica a células pulmonares de ratones jóvenes y viejos. Encuentra componentes que se alinean con los principales tipos celulares —como neumocitos, células ciliadas, macrófagos y células T— y luego señala cambios génicos relacionados con la edad dentro de cada uno, incluidos genes de estrés y de respuesta inmune que encajan con la idea de la «inflamaging» (inflamación asociada al envejecimiento).
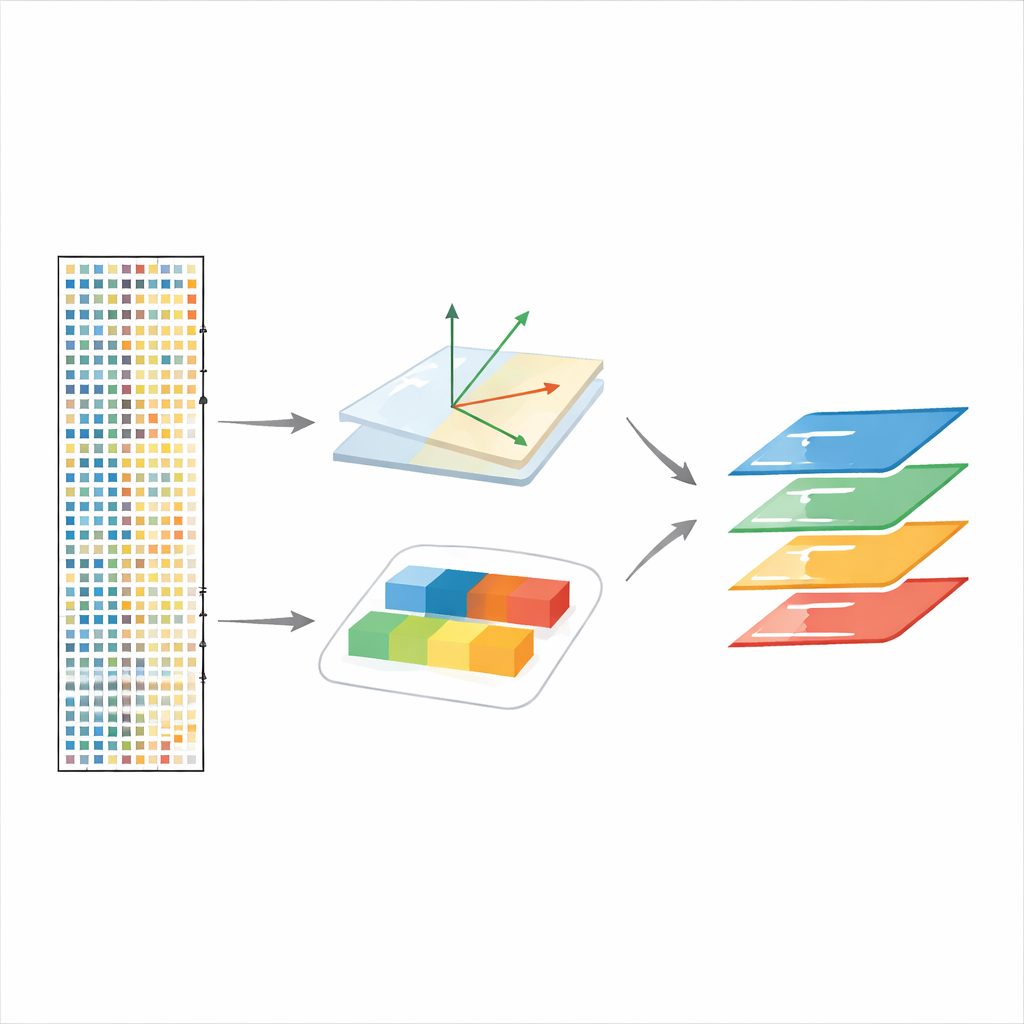
Seguir las respuestas celulares a lo largo del tiempo y entre perturbaciones
scPCA también maneja experimentos con más de dos condiciones, como neuronas de la corteza visual de ratón expuestas a la luz tras un período de oscuridad. Tratando los puntos temporales como niveles diferentes de una condición, el método recupera olas tempranas y tardías de actividad génica en varios tipos celulares cerebrales, separando factores de «respuesta temprana» rápidos de programas de «respuesta tardía» más lentos. En un experimento con pez cebra donde se inactiva un gen clave del desarrollo, chordin, scPCA integra con éxito embriones pese a grandes cambios en la composición por tipo celular y revela cambios transcripcionales consistentes con un patrón corporal alterado, incluidos genes que no fueron destacados en el análisis original.
Qué significa esto para futuros estudios unicelulares
En términos sencillos, scPCA ofrece a los investigadores una lente más nítida para analizar datos unicelulares recogidos bajo diferentes condiciones. Produce mapas integrados donde células similares se alinean entre tratamientos y resalta qué genes dentro de cada patrón compartido se activan o reprimen en respuesta a un estímulo, al envejecimiento o a un cambio genético. Aunque el método asume que la estructura subyacente está en gran medida compartida y es más adecuado para trabajos exploratorios que requieren validación posterior, ofrece una alternativa más transparente e interpretable frente a muchos modelos opacos. Esto debería ayudar a los científicos a extraer conclusiones más fiables de experimentos unicelulares cada vez más complejos.
Cita: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Palabras clave: secuenciación de ARN unicelular, reducción de dimensionalidad, heterogeneidad celular, cambios en la expresión génica, efectos de lote