Clear Sky Science · fr
Modélisation conjointe de l'hétérogénéité cellulaire et des effets de condition avec scPCA en RNA-seq unicellulaire
Pourquoi c'est important pour comprendre les cellules
La biologie moderne peut désormais mesurer quels gènes sont actifs dans des milliers de cellules individuelles simultanément. Mais lorsque les scientifiques comparent des cellules selon différents traitements, âges ou contextes génétiques, le volume massif de données devient écrasant et des artefacts techniques peuvent facilement masquer de véritables changements biologiques. Cet article présente un nouvel outil analytique, scPCA, qui aide les chercheurs à démêler ce qui change réellement dans les cellules selon les conditions de la diversité naturelle existant entre types cellulaires.
Des données cellulaires bruyantes à des schémas clairs
Le séquençage ARN unicellulaire mesure l'activité de milliers de gènes dans chaque cellule, produisant des données de très haute dimension. Pour en tirer sens, les chercheurs compressent généralement ces données avec des méthodes comme l'analyse en composantes principales (ACP), qui identifie un petit nombre d’« axes » capturant les principaux motifs de variation. Cependant, les approches traditionnelles mélangent deux sources de variation très différentes : les différences intrinsèques entre types cellulaires et les changements induits par une expérience, comme un traitement médicamenteux. Les auteurs soutiennent que ce mélange peut induire en erreur des analyses ultérieures, comme le regroupement des cellules en types ou la recherche d'effets de traitement.
Une nouvelle façon de partager la structure entre conditions
scPCA résout ce problème en informant explicitement le modèle de factorisation de la condition d’origine de chaque cellule, puis en apprenant un ensemble distinct — mais lié — de motifs d'expression génique pour chaque condition. Plutôt que d'imposer à tous les échantillons de partager exactement la même structure sous-jacente, scPCA permet à chaque condition d'avoir sa propre version de chaque composante, légèrement décalée par rapport à une condition de référence désignée. Cela préserve un système de coordonnées commun pour comparer les cellules entre conditions, tout en capturant les décalages d'expression systématiques induits par des traitements, le vieillissement ou des changements génétiques.
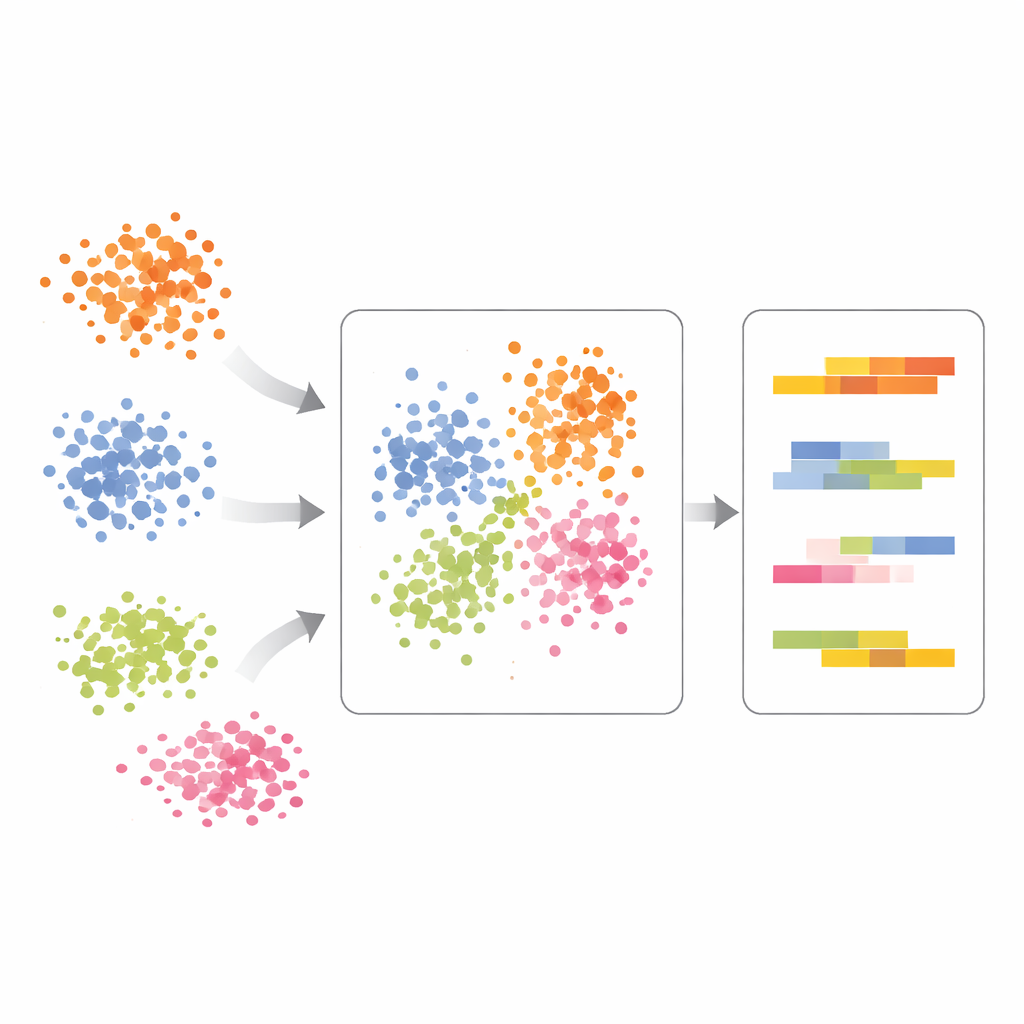
Voir les effets réels du traitement dans les cellules immunitaires
Les auteurs illustrent scPCA sur des cellules immunitaires de patients atteints de lupus, certaines non traitées et d'autres stimulées par l'interféron bêta, un puissant signal immunitaire. L'analyse standard faisait clusteriser les cellules selon le type cellulaire et le traitement, rendant les résultats difficiles à interpréter. Avec scPCA, les cellules d'un même type provenant de différentes conditions s'alignent beaucoup mieux, révélant que l'axe principal de variation reflète toujours les lignées cellulaires immunitaires plutôt que le traitement seul. Ce n'est qu'après avoir tenu compte du type cellulaire que scPCA met en évidence des décalages induits par le traitement dans des gènes spécifiques des cellules myéloïdes, y compris ceux liés à la signalisation de l'interféron et à l'altération du traitement des protéines intracellulaires. Cela montre que la méthode peut séparer proprement l'identité des cellules de leur réponse.
Démêler artefacts techniques et effets du vieillissement
Les expériences souffrent souvent d'effets de lot : des différences subtiles causées par le traitement des échantillons plutôt que par la biologie. En utilisant un mélange de deux lignées cellulaires humaines mesurées dans des lots distincts, les auteurs montrent que l'ACP standard conserve ces différences techniques, tandis que scPCA peut les éliminer en traitant le lot comme une variable de conditionnement. La méthode révèle alors quels gènes expliquaient la séparation apparente par lot, y compris des marqueurs spécifiques à chaque lignée. Dans un exemple plus complexe, scPCA est appliqué à des cellules pulmonaires de souris jeunes et âgées. Il identifie des composantes alignées sur les principaux types cellulaires — tels que pneumocytes, cellules ciliées, macrophages et cellules T — puis met en évidence des changements d'expression liés à l'âge au sein de chacun, notamment des gènes de stress et de réponse immunitaire cohérents avec le concept d’« inflammaging ».
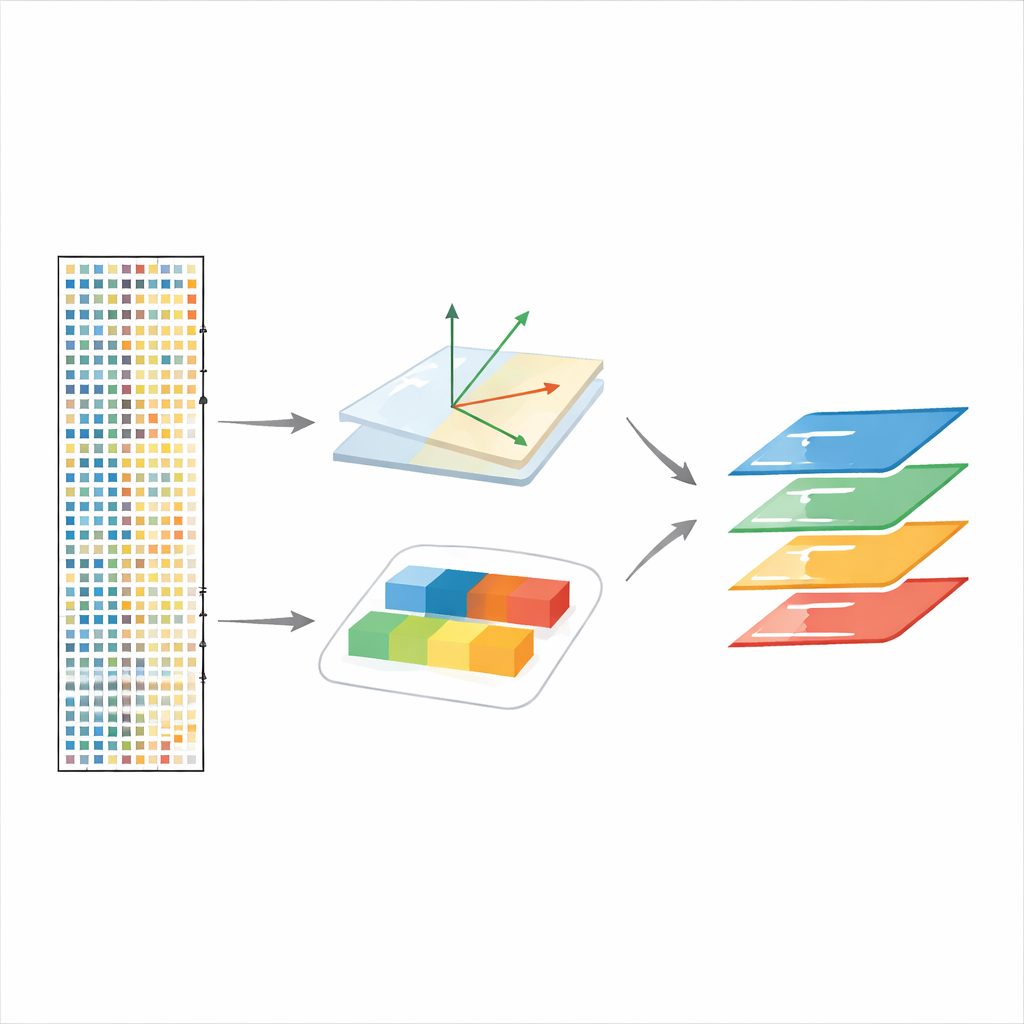
Suivre les réponses cellulaires dans le temps et à travers des perturbations
scPCA gère également les expériences comportant plus de deux conditions, comme des neurones du cortex visuel de souris exposés à la lumière après une période d'obscurité. En traitant les points temporels comme des niveaux différents d'une condition, la méthode récupère des vagues précoces et tardives d'activité génique à travers plusieurs types cellulaires cérébraux, séparant des facteurs de « réponse précoce » rapides de programmes de « réponse tardive » plus lents. Dans une expérience sur le poisson zèbre où un gène de développement clé, chordin, est supprimé, scPCA intègre avec succès les embryons malgré de grands changements de composition cellulaire et révèle des modifications transcriptionnelles cohérentes avec un altération du patterning corporel, y compris des gènes qui n'avaient pas été mis en avant dans l'analyse originale.
Ce que cela signifie pour les futures études unicellulaires
En termes simples, scPCA offre aux chercheurs une lentille plus claire pour examiner des données unicellulaires collectées sous différentes conditions. Il produit des cartes intégrées où des cellules similaires s'alignent à travers les traitements, et il met en évidence quels gènes, au sein de chaque motif partagé, sont augmentés ou diminués en réponse à un stimulus, au vieillissement ou à un changement génétique. Bien que la méthode suppose que la structure sous-jacente est largement partagée et soit mieux utilisée pour des explorations nécessitant encore une validation ultérieure, elle constitue une alternative plus transparente et interprétable à de nombreux modèles boîte noire. Cela devrait aider les scientifiques à tirer des conclusions plus fiables d'expériences unicellulaires de plus en plus complexes.
Citation: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Mots-clés: séquençage ARN unicellulaire, réduction de dimensionnalité, hétérogénéité cellulaire, changements d'expression génique, effets de lot