Clear Sky Science · nl
Gezamenlijke modellering van cellulaire heterogeniteit en conditie-effecten met scPCA in single-cell RNA-seq
Waarom dit belangrijk is voor het begrijpen van cellen
De moderne biologie kan nu aflezen welke genen actief zijn in duizenden individuele cellen tegelijk. Maar wanneer onderzoekers cellen vergelijken over verschillende behandelingen, leeftijden of genetische achtergronden, wordt de enorme hoeveelheid data onoverzichtelijk en kunnen technische eigenaardigheden echte biologische veranderingen makkelijk verhullen. Dit artikel introduceert een nieuw analysetool, scPCA, dat onderzoekers helpt te ontrafelen wat daadwerkelijk verandert in cellen onder verschillende condities en wat de natuurlijke diversiteit tussen celtypes is.
Van rumoerige celdata naar heldere patronen
Single-cell RNA-sequencing meet de activiteit van duizenden genen in elke cel en levert zeer hoog-dimensionale data op. Om dit te begrijpen comprimeren onderzoekers de data doorgaans met methoden zoals principal component analysis (PCA), die een klein aantal “assen” vindt die de belangrijkste variatiepatronen vangen. Traditionele benaderingen mengen echter twee heel verschillende bronnen van variatie: intrinsieke verschillen tussen celtypes en veranderingen veroorzaakt door een experiment, zoals een medicamenteuze behandeling. De auteurs stellen dat deze vermenging downstream-analyses kan misleiden, bijvoorbeeld bij het clusteren van cellen in types of bij het zoeken naar behandel-effecten.
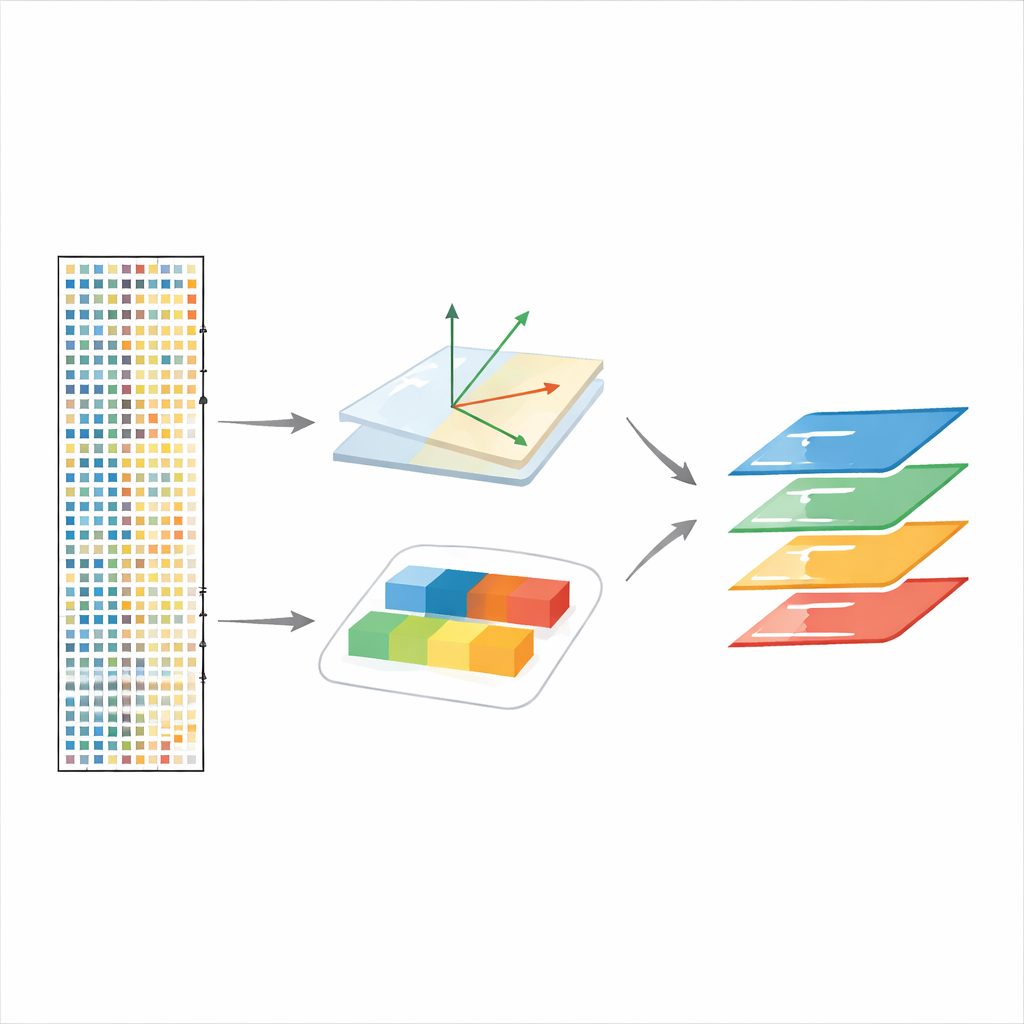
Een nieuwe manier om structuur over condities te delen
scPCA pakt dit probleem aan door het factorizatiemodel expliciet te vertellen uit welke conditie elke cel afkomstig is, en vervolgens voor elke conditie een aparte—maar gekoppelde—set genexpressiepatronen te leren. In plaats van alle monsters precies dezelfde onderliggende structuur te laten delen, staat scPCA elk conditioneel scenario toe zijn eigen versie van elk component te hebben, licht verschoven ten opzichte van een aangewezen referentieconditie. Dit behoudt een gemeenschappelijk coördinatensysteem voor het vergelijken van cellen over condities, terwijl het toch systematische expressieverschuivingen door behandelingen, veroudering of genetische veranderingen vangt.
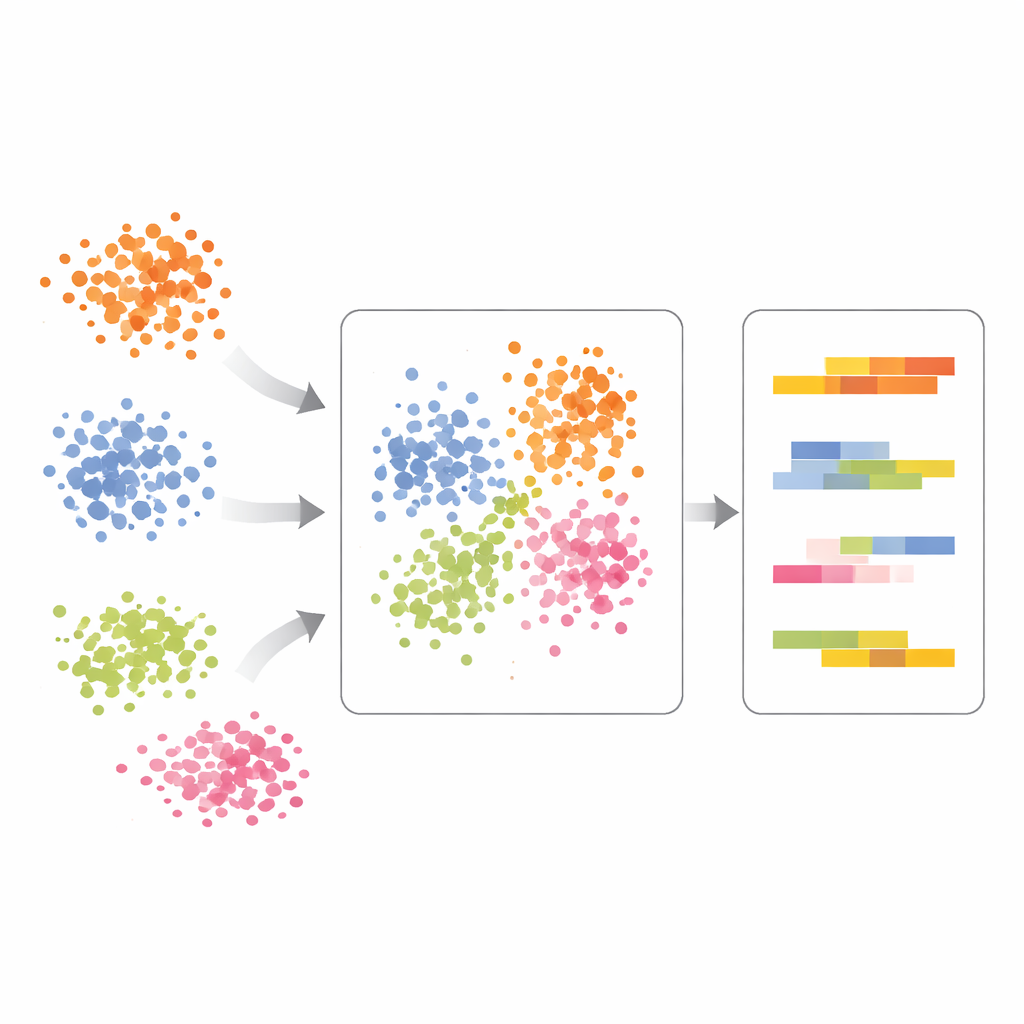
Werkelijke behandel-effecten zien in immuuncellen
De auteurs demonstreren scPCA op immuuncellen van patiënten met lupus, waarvan sommige onbehandeld zijn en andere gestimuleerd met interferon-beta, een sterke immuunstimulus. Standaardanalyses lieten cellen clusteren op zowel celtype als behandeling, waardoor de uitkomsten moeilijk te interpreteren waren. Met scPCA waren cellen van hetzelfde type uit verschillende condities veel beter uitgelijnd, wat aantoonde dat de belangrijkste variatie-as nog steeds immuuncellijnages weerspiegelde in plaats van alleen behandeling. Pas nadat celltype was geaccommodeerd, benadrukte scPCA behandelgestuurde verschuivingen in specifieke genen in myeloïde cellen, inclusief genen gekoppeld aan interferonsignalering en gewijzigde eiwithandling binnen de cel. Dit toonde aan dat de methode duidelijk onderscheid kan maken tussen wie de cellen zijn en hoe ze reageren.
Technische artefacten en veroudering ontwarren
Experimenten hebben vaak te lijden van batch-effecten: subtiele verschillen veroorzaakt door monsterverwerking en niet door biologie. Met een mengsel van twee humane cellijnen die in aparte batches zijn gemeten, laten de auteurs zien dat standaard PCA deze technische verschillen behoudt, terwijl scPCA ze grotendeels kan verwijderen door batch als conditioneringsvariabele te behandelen. De methode laat vervolgens zien welke genen verantwoordelijk leken voor de schijnbare batch-separatie, inclusief markers specifiek voor elke cellijn. In een complexer voorbeeld wordt scPCA toegepast op longcellen van jonge en oude muizen. Het vindt componenten die uitlijnen met de belangrijke celtypes—zoals pneumocyten, trilhaarcellen, macrofagen en T-cellen—en identificeert vervolgens leeftijdsgerelateerde genveranderingen binnen elk type, inclusief stress- en immuunresponsgenen die passen bij het concept van “inflammaging.”
Celresponsen volgen over tijd en over verstoringen heen
scPCA verwerkt ook experimenten met meer dan twee condities, zoals neuronen in de visuele cortex van muizen die na een periode in het donker aan licht worden blootgesteld. Door tijdspunten als verschillende niveaus van een conditie te behandelen, herstelt de methode vroege en late golven van genactiviteit in meerdere hersenceltypes, waarbij snelle “early-response”-factoren worden gescheiden van tragere “late-response”-programma’s. In een zebravis-experiment waarin een cruciaal ontwikkelingsgen, chordin, is uitgeschakeld, integreert scPCA embryo’s succesvol ondanks grote verschuivingen in samenstelling van celtypes en onthult transcriptieveranderingen die consistent zijn met gewijzigde lichaams-pattering, inclusief genen die in de oorspronkelijke analyse niet werden benadrukt.
Wat dit betekent voor toekomstige single-cell studies
Simpel gezegd geeft scPCA onderzoekers een helderder lens om naar single-cell data te kijken die onder verschillende condities zijn verzameld. Het produceert geïntegreerde kaarten waarin vergelijkbare cellen over behandelingen heen uitlijnen, en het laat zien welke genen binnen elk gedeeld patroon omhoog of omlaag gaan als reactie op een stimulus, veroudering of genetische verandering. Hoewel de methode ervan uitgaat dat de onderliggende structuur grotendeels gedeeld is en het het beste geschikt is voor verkennend werk dat nog bevestiging vereist, biedt het een transparantere en beter interpreteerbare alternatieven voor veel black-box-modellen. Dit zou wetenschappers moeten helpen betrouwbaardere conclusies te trekken uit steeds complexere single-cell experimenten.
Bronvermelding: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Trefwoorden: single-cell RNA-sequencing, dimensionaliteitsreductie, cellulaire heterogeniteit, veranderingen in genexpressie, batch-effecten