Clear Sky Science · de
Gemeinsame Modellierung zellulärer Heterogenität und Bedingungseffekte mit scPCA in Einzelzell-RNA-seq
Warum das für das Verständnis von Zellen wichtig ist
Die moderne Biologie kann mittlerweile ablesen, welche Gene in tausenden einzelnen Zellen gleichzeitig aktiv sind. Wenn Wissenschaftler Zellen jedoch zwischen verschiedenen Behandlungen, Altersstufen oder genetischen Hintergründen vergleichen, wird das Datenvolumen schnell überwältigend, und technische Besonderheiten können echte biologische Veränderungen leicht überdecken. Diese Arbeit stellt ein neues Analysewerkzeug, scPCA, vor, das Forschenden hilft, zu trennen, was sich in Zellen unter verschiedenen Bedingungen tatsächlich ändert, von der natürlichen Vielfalt zwischen Zelltypen.
Von verrauschten Zelldaten zu klaren Mustern
Die Einzelzell-RNA-Sequenzierung misst die Aktivität von tausenden Genen in jeder Zelle und erzeugt sehr hochdimensionale Daten. Um das zu interpretieren, komprimieren Forschende die Daten meist mit Methoden wie der Hauptkomponentenanalyse (PCA), die eine kleine Menge von „Achsen“ findet, die die wichtigsten Variationsmuster erfassen. Klassische Ansätze vermischen jedoch zwei sehr unterschiedliche Quellen von Variation: die inhärenten Unterschiede zwischen Zelltypen und die durch ein Experiment verursachten Veränderungen, etwa eine Wirkstoffbehandlung. Die Autoren argumentieren, dass dieses Vermischen nachgelagerte Analysen wie das Clustern von Zellen oder die Suche nach Behandlungseffekten in die Irre führen kann.
Eine neue Möglichkeit, Struktur über Bedingungen hinweg zu teilen
scPCA geht dieses Problem an, indem das Faktorisierungsmodell explizit mitgeteilt wird, aus welcher Bedingung jede Zelle stammt, und dann für jede Bedingung ein separates — aber verknüpftes — Set von Genexpressionsmustern gelernt wird. Anstatt alle Proben zu zwingen, genau dieselbe zugrundeliegende Struktur zu teilen, erlaubt scPCA jeder Bedingung, eine eigene Version jeder Komponente zu haben, die sanft gegenüber einer gewählten Referenzbedingung verschoben ist. Das bewahrt ein gemeinsames Koordinatensystem zum Vergleich von Zellen über Bedingungen hinweg und erfasst gleichzeitig systematische Expressionsverschiebungen, die durch Behandlungen, Altern oder genetische Veränderungen hervorgerufen werden.
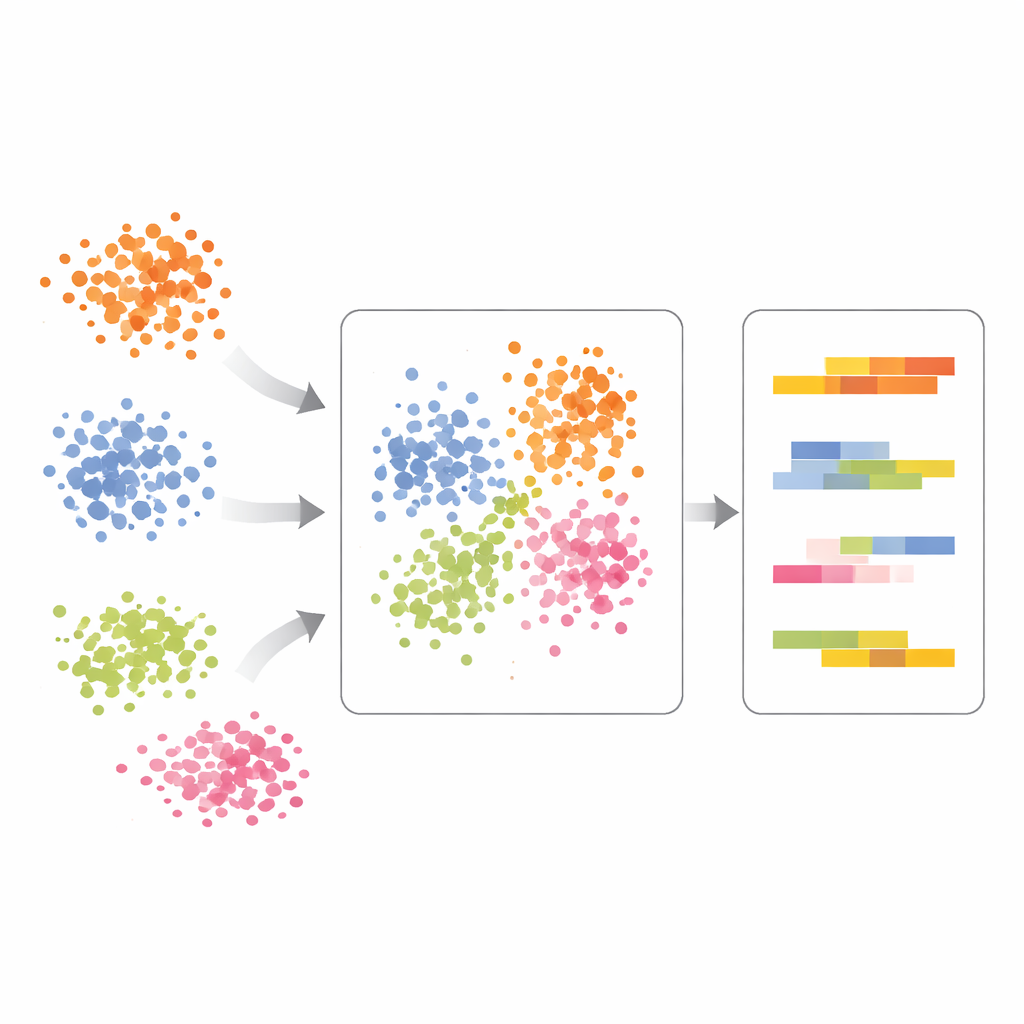
Wahre Behandlungseffekte in Immunzellen erkennen
Die Autoren demonstrieren scPCA an Immunzellen von Lupus-Patienten, von denen einige unbehandelt blieben und andere mit Interferon-Beta, einem starken Immunsignal, stimuliert wurden. Standardanalysen führten dazu, dass Zellen sowohl nach Zelltyp als auch nach Behandlung clusterten, was die Interpretation erschwerte. Mit scPCA ordneten sich Zellen desselben Typs aus verschiedenen Bedingungen deutlich besser ausgerichtet, wobei die Hauptvarianzachse weiterhin die Abstammungslinien der Immunzellen statt nur die Behandlung widerspiegelte. Erst nachdem der Zelltyp berücksichtigt wurde, hob scPCA behandlungsgetriebene Verschiebungen in spezifischen Genen in myeloiden Zellen hervor, einschließlich solcher, die mit Interferon-Signalgebung und veränderter Proteinverarbeitung innerhalb der Zelle verbunden sind. Das zeigte, dass die Methode sauber zwischen Identität der Zellen und ihrer Reaktion unterscheiden kann.
Technische Artefakte und Alterungseffekte entwirren
Experimente leiden oft unter Batch-Effekten: subtilen Unterschieden, die durch Probenverarbeitung statt durch Biologie verursacht werden. Anhand einer Mischung aus zwei menschlichen Zelllinien, die in getrennten Chargen gemessen wurden, zeigen die Autoren, dass die Standard-PCA diese technischen Unterschiede beibehält, während scPCA sie weitgehend entfernen kann, indem es die Charge als konditionierende Variable behandelt. Die Methode zeigt dann, welche Gene für die scheinbare Chargentrennung verantwortlich waren, einschließlich Marker, die für jede Zelllinie spezifisch sind. In einem komplexeren Beispiel wenden die Autoren scPCA auf Lungenzellen junger und alter Mäuse an. Sie finden Komponenten, die mit großen Zelltypen übereinstimmen — wie Pneumozyten, Flimmerzellen, Makrophagen und T‑Zellen — und identifizieren dann altersbezogene Genveränderungen innerhalb jedes Typs, einschließlich Stress- und Immunantwortgenen, die zum Konzept der „Inflammaging“ passen.
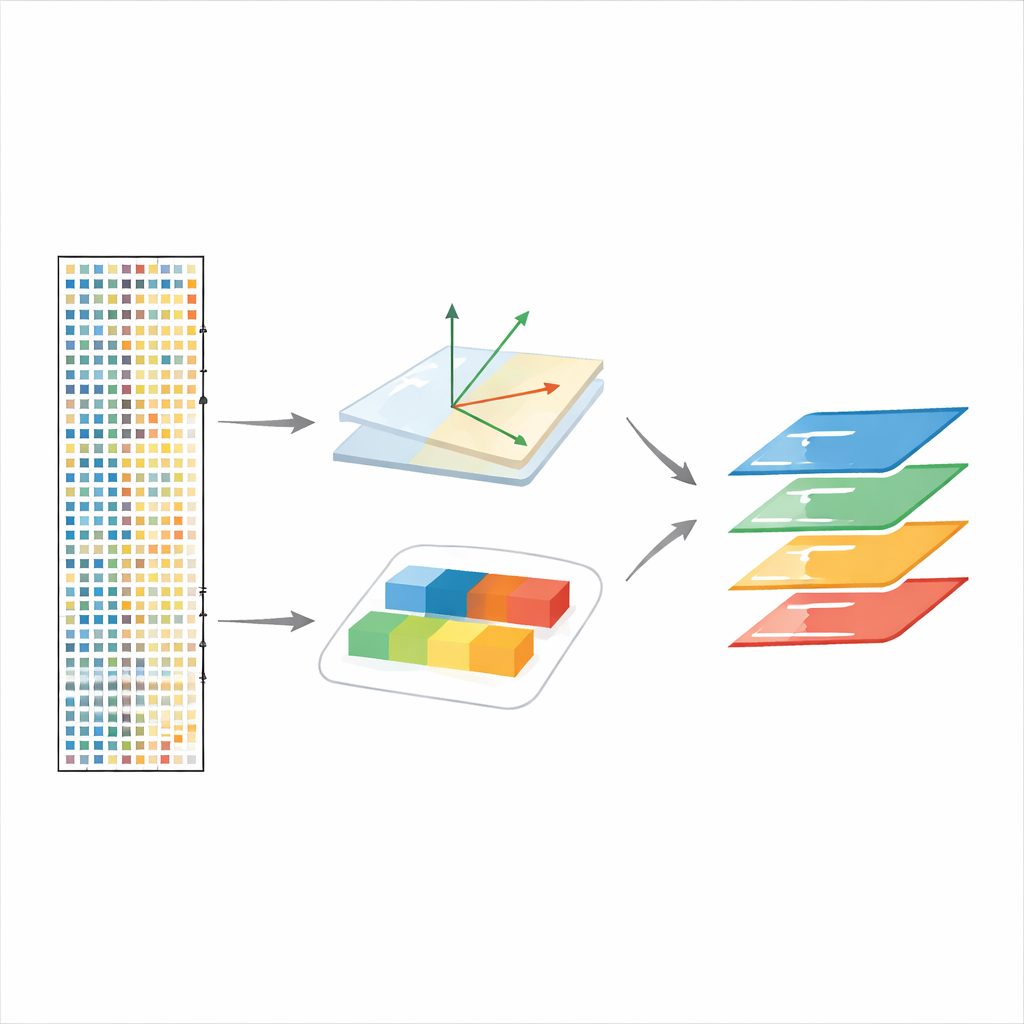
Verfolgen von Zellantworten über Zeit und Störungen hinweg
scPCA bewältigt auch Experimente mit mehr als zwei Bedingungen, etwa Neuronen im visuellen Kortex der Maus, die nach einer Dunkelphase Licht ausgesetzt werden. Indem Zeitpunkte als verschiedene Stufen einer Bedingung behandelt werden, rekonstruiert die Methode frühe und späte Wellen der Genaktivität über mehrere Gehirnzelltypen und trennt schnelle „Frühantwort“-Faktoren von langsameren „Spätantwort“-Programmen. In einem Zebrafisch-Experiment, in dem ein wichtiges Entwicklungsgen, chordin, ausgeschaltet wird, integriert scPCA Embryonen erfolgreich trotz großer Verschiebungen in der Zellzusammensetzung und zeigt transkriptionelle Veränderungen, die mit veränderter Körpermusterbildung konsistent sind, einschließlich Gene, die in der Originalanalyse nicht hervorgehoben wurden.
Was das für zukünftige Einzelzellstudien bedeutet
Einfach gesagt bietet scPCA Forschenden eine klarere Linse für die Betrachtung von Einzelzell-Daten, die unter verschiedenen Bedingungen erhoben wurden. Es erzeugt integrierte Karten, auf denen ähnliche Zellen über Behandlungen hinweg ausgerichtet sind, und hebt hervor, welche Gene innerhalb jedes gemeinsamen Musters als Reaktion auf einen Stimulus, Alterungsprozesse oder genetische Veränderungen hoch- oder runterreguliert werden. Während die Methode annimmt, dass die zugrundeliegende Struktur größtenteils geteilt ist und am besten für explorative Arbeiten geeignet ist, die weiterhin Validierung erfordern, bietet sie eine transparentere und besser interpretierbare Alternative zu vielen Black‑Box‑Modellen. Das sollte Wissenschaftlern helfen, aus zunehmend komplexen Einzelzellexperimenten zuverlässigere Schlussfolgerungen zu ziehen.
Zitation: Vöhringer, H. Joint modeling of cellular heterogeneity and condition effects with scPCA in single-cell RNA-seq. Commun Biol 9, 492 (2026). https://doi.org/10.1038/s42003-026-09651-6
Schlüsselwörter: Einzelzell-RNA-Sequenzierung, Dimensionsreduktion, zelluläre Heterogenität, Genexpressionsänderungen, Batch-Effekte