Clear Sky Science · pl
Deubikwitynaza USP7 stabilizuje FAN1, wspierając naprawę mostków DNA i hamując ekspansję powtórzeń CAG
Ochrona instrukcji obsługi naszego DNA
Każda komórka w naszym ciele polega na DNA jako głównym podręczniku instrukcji. Ta delikatna sekwencja jest jednak nieustannie narażona na ataki chemiczne, promieniowanie i nawet na normalne procesy komórkowe. Gdy uszkodzenia pozostaną nienaprawione, mogą prowadzić do nowotworów lub zaburzeń mózgu, takich jak choroba Huntingtona. W tym badaniu odkryto, jak dwaj komórkowi „majstrowie”, białka USP7 i FAN1, współpracują, by chronić DNA przed szczególnie groźnym rodzajem uszkodzenia i spowalniać zmiany genetyczne napędzające chorobę Huntingtona.
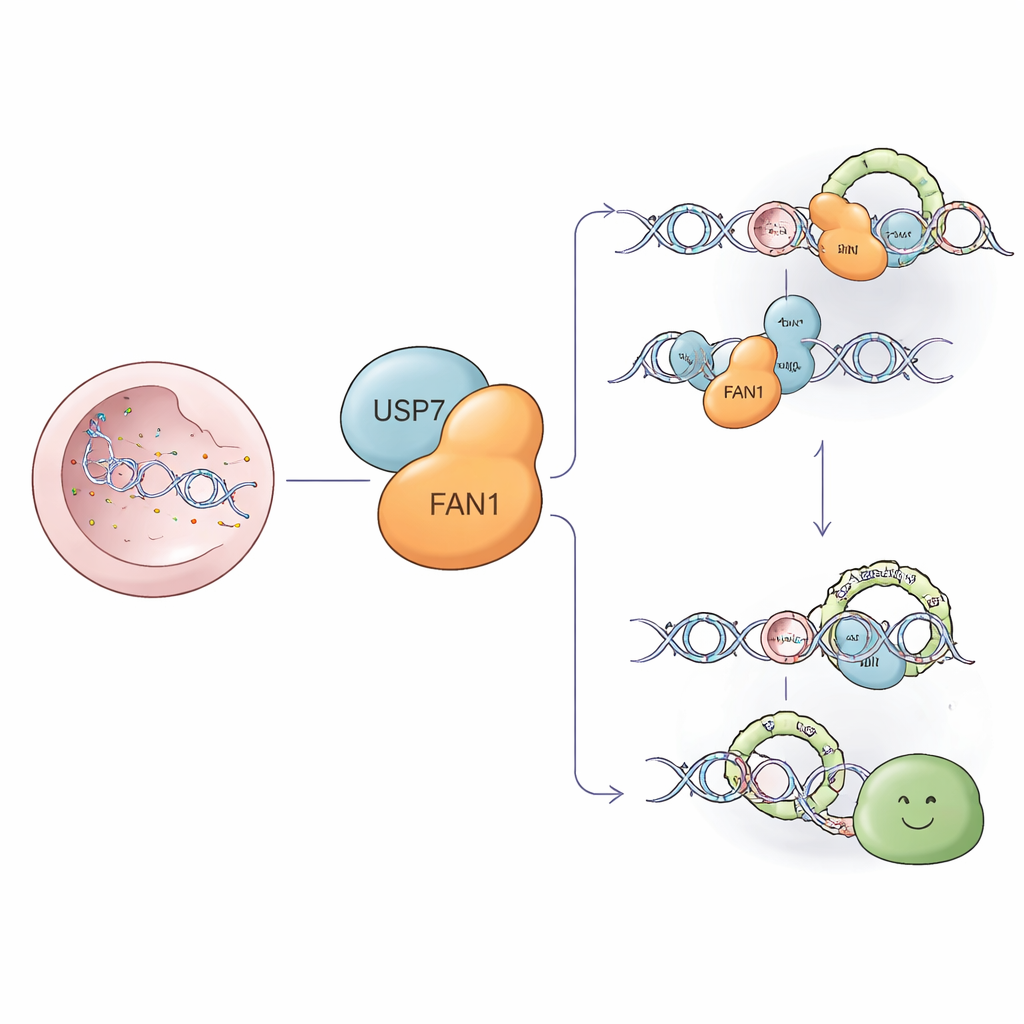
Komórkowy zespół sprzątający dla uporczywych uszkodzeń DNA
Niektóre z najgroźniejszych uszkodzeń DNA to międzyłańcuchowe usztywnienia—molekularne „zszywki”, które sklejają ze sobą dwa nici podwójnej helisy DNA. Te zszywki blokują maszynerię kopiującą DNA, zagrażając przeżyciu komórki. FAN1 to wyspecjalizowana nukleaza, która potrafi wyciąć fragment wokół takich zszywek i pomóc je usunąć, aby naprawa mogła przebiec. FAN1 przycina także problematyczne dodatkowe pętle, które powstają w odcinkach z powtarzającymi się literami DNA, w tym powtórzenia CAG w genie powiązanym z chorobą Huntingtona. Utrzymanie odpowiedniego poziomu i lokalizacji FAN1 jest zatem kluczowe zarówno dla zapobiegania nowotworom, jak i dla prawidłowego funkcjonowania mózgu.
USP7: ochroniarz białkowy
Białka w komórkach są nieustannie znakowane do zniszczenia małymi cząsteczkami zwanymi ubikwityną. To znakowanie przypomina naklejanie etykiety „do wyrzucenia” na białko, aby komórkowe mechanizmy recyklingu je rozłożyły. USP7 to deubikwitynaza—enzym usuwający te znaczniki i ratujący wybrane białka przed niszczącym wirusem. Badacze użyli spektrometrii mas, techniki katalogowania partnerów białkowych, i odkryli, że USP7 fizycznie wiąże się z FAN1, szczególnie w jego elastycznym regionie N‑terminalnym. Poprzez przyczepianie się dwoma odmiennymi powierzchniami USP7 może wielokrotnie rozpoznawać FAN1 i zrywać z nim znaczniki prowadzące do zniszczenia.
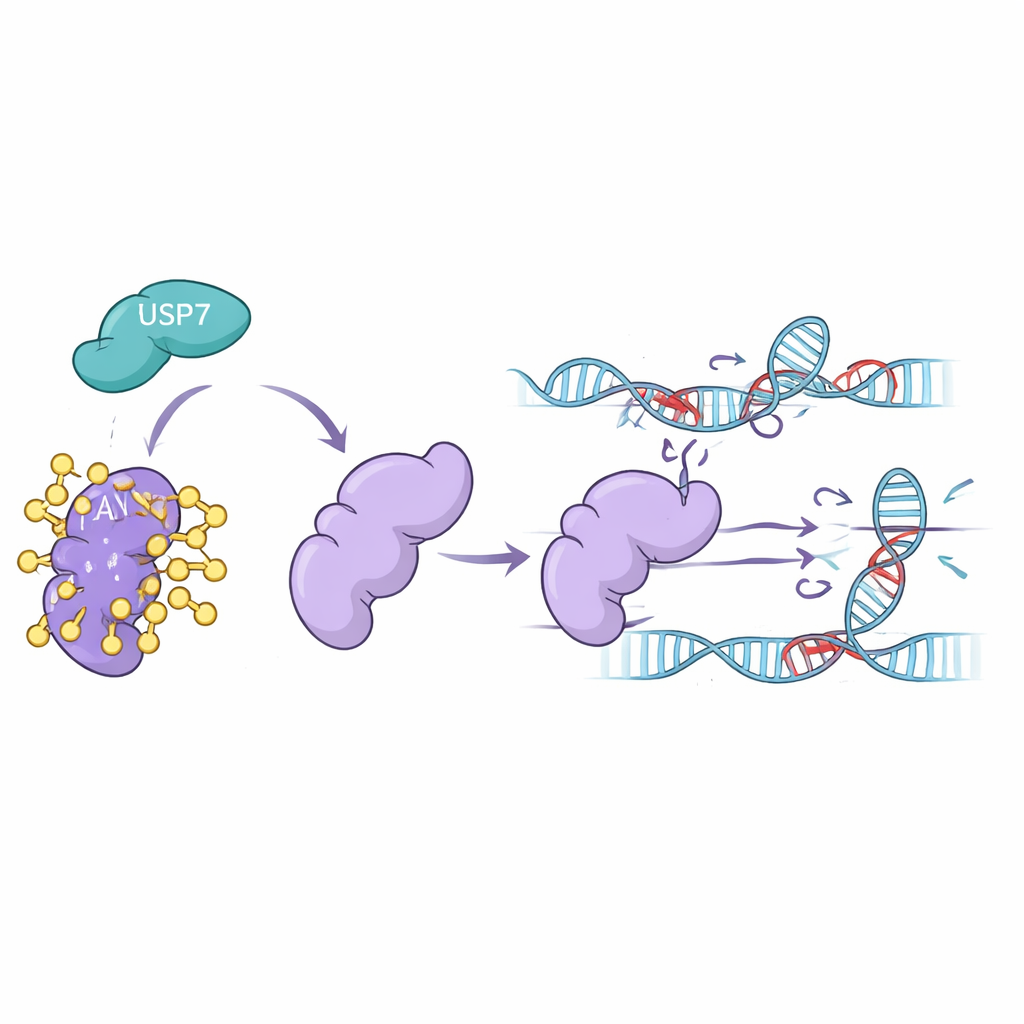
Jak USP7 utrzymuje FAN1 przy pracy
Eksperymenty laboratoryjne na ludzkich liniach komórkowych wykazały, że gdy poziomy USP7 były obniżone—albo przez wyciszenie genu, albo przez leczenie komórek lekami blokującymi USP7—poziomy FAN1 gwałtownie spadały. FAN1 stał się silnie ubikwitynowany i kierowany do proteasomu, komórkowego centrum recyklingu białek. Zablokowanie proteasomu ratowało FAN1, co potwierdza, że USP7 normalnie chroni FAN1 przed tym losem. Zespół pokazał również, że tylko aktywna forma USP7 potrafi usunąć specyficzny rodzaj łańcucha ubikwitynowego, który oznacza FAN1 do zniszczenia. Bez USP7 FAN1 znikał szybciej i nie gromadził się skutecznie w miejscach uszkodzeń DNA, gdzie należało usunąć międzyłańcuchowe zszywki.
Konsekwencje dla naprawy DNA i choroby Huntingtona
Gdy komórki narażono na lek chemioterapeutyczny tworzący międzyłańcuchowe usztywnienia, te pozbawione USP7 wykazywały mniej ognisk naprawczych FAN1 na DNA, większą śmiertelność komórek i większą wrażliwość na uszkodzenia. Przy umiarkowanym stresie usunięcie USP7 lub FAN1 powodowało podobną podatność, co sugeruje, że FAN1 jest głównym celem USP7 w tej ścieżce naprawczej. Autorzy zwrócili się następnie ku chorobie Huntingtona, gdzie ekspansja powtórzeń CAG w genie huntingtyny pogarsza przebieg choroby w czasie. W modelu ludzkich komórek siatkówki zaprojektowanym tak, by mieć długi powtórzony odcinek, utrata FAN1 przyspieszała wzrost powtórzeń, podczas gdy unieszkodliwienie czynnika naprawy błędów (mismatch repair) go spowalniało. Co uderzające, wyciszenie USP7 przyspieszało ekspansję powtórzeń CAG niemal tak bardzo, jak utrata FAN1, wskazując, że USP7 pośrednio hamuje wzrost powtórzeń, utrzymując stabilność FAN1.
Dlaczego to odkrycie ma znaczenie
Praca ta ujawnia USP7 jako kluczowego strażnika FAN1, łącząc dwa główne zagrożenia dla zdrowia genomu: trudne do naprawy międzyłańcuchowe uszkodzenia DNA i niekontrolowaną ekspansję powtórzeń CAG w chorobie Huntingtona. Dla czytelnika nieznającego szczegółów najważniejszy wniosek jest taki, że USP7 działa jak ochroniarz, osłaniając FAN1 przed przedwczesnym zniszczeniem, aby mógł kontynuować naprawę DNA i spowalniać dryf genetyczny napędzający neurodegenerację. Wyniki sugerują delikatną równowagę dla przyszłych terapii: blokowanie USP7 może uczynić komórki nowotworowe bardziej podatnymi na niektóre chemioterapie, podczas gdy wzmocnienie partnerstwa USP7–FAN1 mogłoby pomóc stabilizować szkodliwe powtórzenia DNA w mózgu.
Cytowanie: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Słowa kluczowe: naprawa DNA, stabilność genomu, choroba Huntingtona, degradacja białek, powtórzenia trójnukleotydowe