Clear Sky Science · fr
La déubiquitinase USP7 stabilise FAN1 pour soutenir la réparation des liaisons croisées de l’ADN et freiner l’expansion des répétitions CAG
Protéger le manuel d’instructions de notre ADN
Chaque cellule de notre corps s’appuie sur l’ADN comme manuel d’instructions principal. Mais ce code fragile est constamment attaqué par des produits chimiques, des radiations et même par des processus cellulaires routiniers. Lorsqu’une lésion n’est pas réparée, elle peut conduire à un cancer ou à des troubles cérébraux comme la maladie de Huntington. Cette étude dévoile comment deux « bricoleurs » cellulaires, des protéines nommées USP7 et FAN1, s’associent pour protéger l’ADN contre un type de dommage particulièrement dangereux et pour ralentir les changements génétiques qui alimentent la maladie de Huntington.
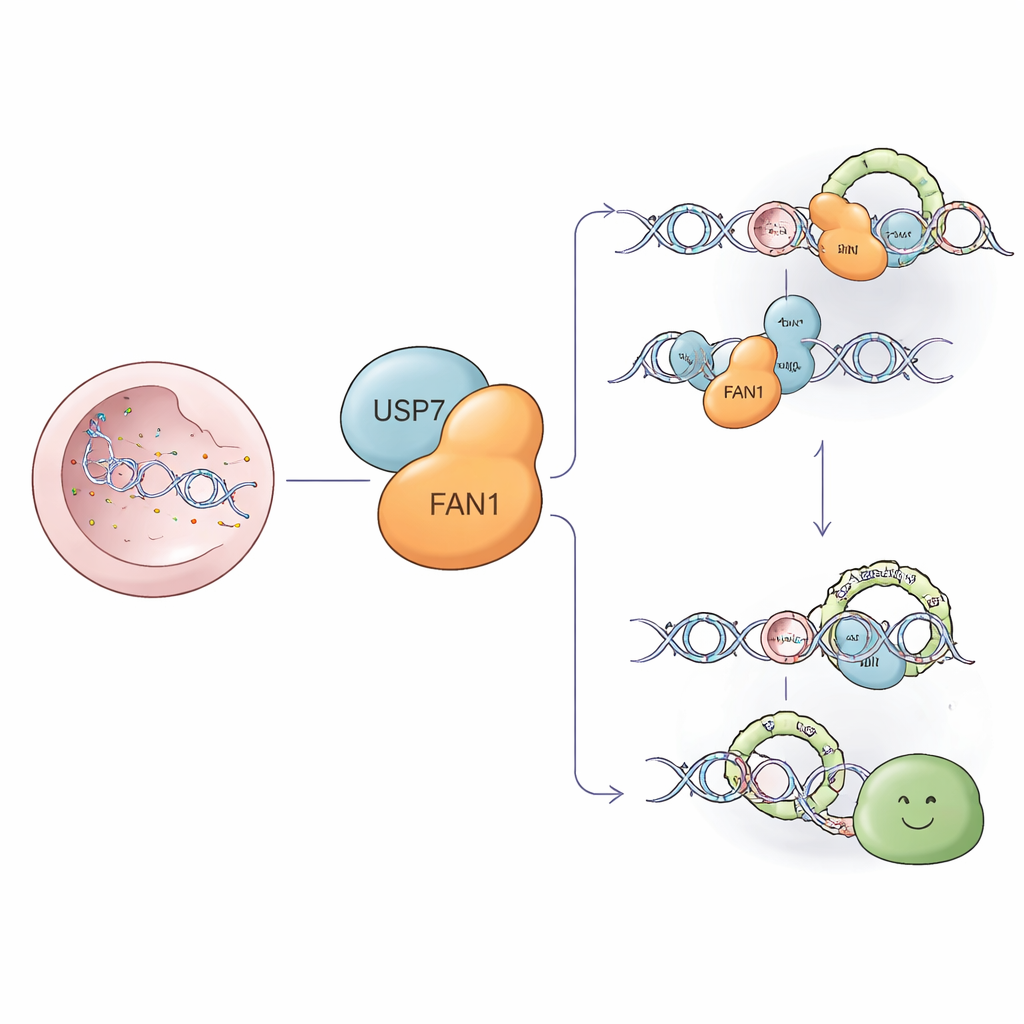
Une équipe de nettoyage moléculaire pour des dommages tenaces
Parmi les blessures les plus nocives pour l’ADN se trouvent les liaisons interbrins — de véritables « agrafes » moléculaires qui collent ensemble les deux brins de la double hélice. Ces agrafes bloquent la machinerie qui copie l’ADN, menaçant la survie cellulaire. FAN1 est une enzyme spécialisée qui peut découper autour de ces agrafes et aider à les éliminer afin que la réparation puisse avoir lieu. FAN1 raccourcit aussi des boucles gênantes qui se forment dans des segments d’ADN répétitifs, y compris les répétitions CAG du gène associé à la maladie de Huntington. Maintenir FAN1 au bon niveau et au bon emplacement est donc crucial à la fois pour la prévention du cancer et pour le bon fonctionnement cérébral.
USP7 : le garde du corps des protéines
Les protéines cellulaires sont constamment marquées pour destruction par de petites molécules appelées ubiquitines. Ce marquage revient à coller un autocollant « poubelle » sur une protéine afin que la machinerie de recyclage cellulaire la dégrade. USP7 est une déubiquitinase — une enzyme qui enlève ces marques et sauve certaines protéines de la destruction. Les chercheurs ont utilisé la spectrométrie de masse, une technique de catalogage des partenaires protéiques, et ont découvert que USP7 se lie physiquement à FAN1, en particulier sur la région N‑terminale flexible de FAN1. En s’accrochant via deux surfaces distinctes, USP7 reconnaît à plusieurs reprises FAN1 et retire les marques de destruction.
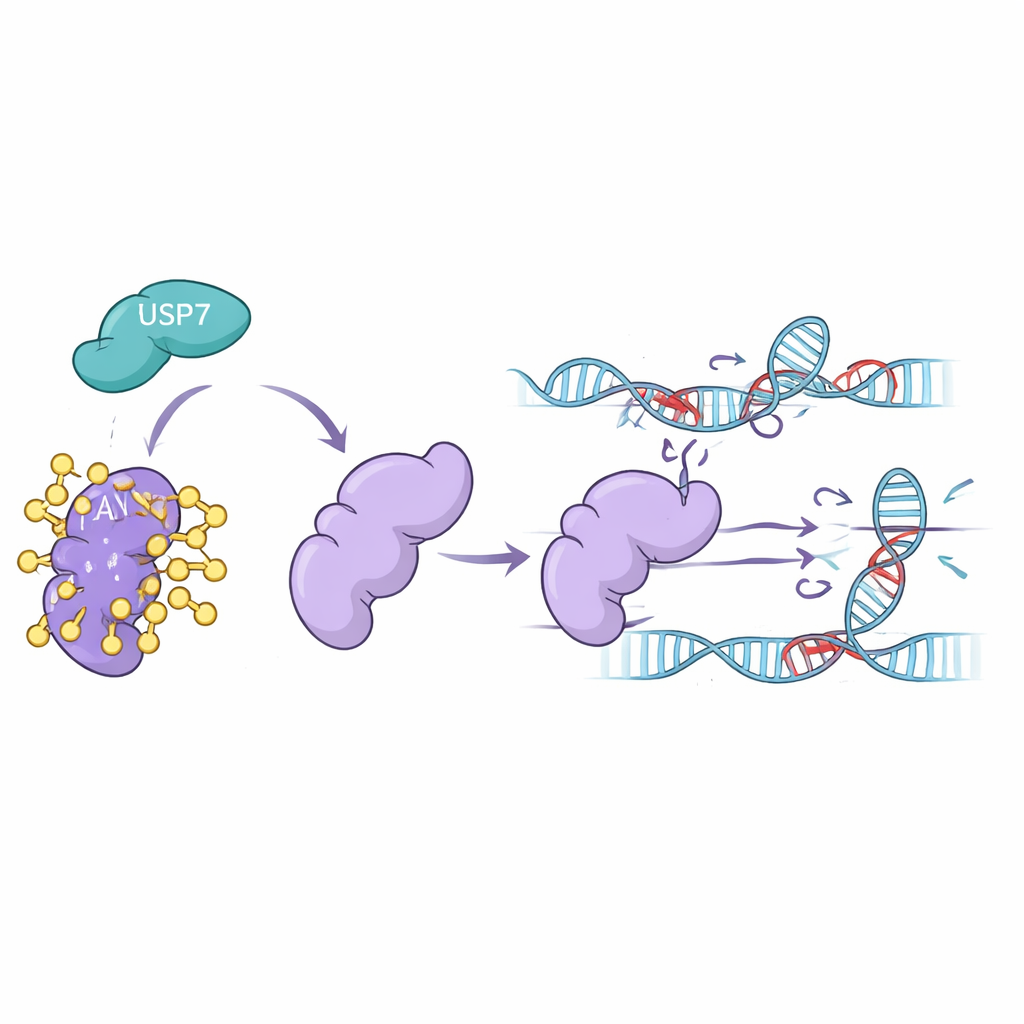
Comment USP7 maintient FAN1 en activité
Des expériences en laboratoire sur des lignées cellulaires humaines ont montré que lorsque les niveaux d’USP7 étaient réduits — soit en silencant son gène, soit en traitant les cellules avec des médicaments inhibant USP7 — les niveaux de FAN1 chutaient fortement. FAN1 devenait fortement décoré d’ubiquitine et était envoyé au protéasome, le centre de recyclage des protéines de la cellule. Bloquer le protéasome permettait de sauver FAN1, confirmant qu’USP7 protège normalement FAN1 de ce destin. L’équipe a en outre montré que seule la forme active d’USP7 pouvait retirer le type spécifique de chaîne d’ubiquitine qui signale FAN1 pour destruction. Sans USP7, FAN1 disparaît plus rapidement et ne peut plus s’accumuler efficacement au niveau des ADN endommagés où les liaisons croisées doivent être éliminées.
Conséquences pour la réparation de l’ADN et la maladie de Huntington
Lorsque les cellules étaient exposées à un médicament de chimiothérapie formant des liaisons croisées, celles dépourvues d’USP7 présentaient moins de foyers de réparation FAN1 sur l’ADN, plus de mortalité cellulaire et une plus grande sensibilité aux dommages. En situation de stress modéré, supprimer USP7 ou supprimer FAN1 provoquait une fragilité similaire, ce qui suggère que FAN1 est une cible principale d’USP7 dans cette voie de réparation. Les auteurs se sont ensuite intéressés à la maladie de Huntington, où l’expansion des répétitions CAG dans le gène huntingtine aggrave la maladie au fil du temps. Dans un modèle cellulaire rétinien humain modifié pour porter une longue répétition, la perte de FAN1 accélère la croissance des répétitions, tandis que l’inactivation d’un facteur de réparation des mésappariements la ralentit. Fait marquant, l’inhibition d’USP7 a accéléré l’expansion des répétitions CAG presque autant que la perte de FAN1, indiquant qu’USP7 freine indirectement la croissance des répétitions en stabilisant FAN1.
Pourquoi cette découverte est importante
Ce travail révèle USP7 comme un gardien clé de FAN1, reliant deux menaces majeures pour la santé du génome : les liaisons croisées de l’ADN difficiles à réparer et l’expansion incontrôlée des répétitions CAG dans la maladie de Huntington. Pour un lecteur non spécialiste, le message essentiel est que USP7 agit comme un garde du corps, protégeant FAN1 d’une destruction prématurée afin qu’il puisse maintenir la réparation de l’ADN et ralentir la dérive génétique responsable de la neurodégénérescence. Les résultats suggèrent un équilibre délicat pour des thérapies futures : bloquer USP7 pourrait rendre les cellules cancéreuses plus vulnérables à certains traitements de chimiothérapie, tandis que renforcer le partenariat USP7–FAN1 pourrait aider à stabiliser les répétitions d’ADN nuisibles dans le cerveau.
Citation: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Mots-clés: Réparation de l’ADN, stabilité du génome, maladie de Huntington, dégradation des protéines, répétitions trinucléotidiques