Clear Sky Science · nl
USP7-deubiquitinase stabiliseert FAN1 om DNA-kruislingherstel te ondersteunen en CAG-herhalingsexpansie te onderdrukken
Het beschermingsplan van onze DNA-instructies
Elke cel in ons lichaam vertrouwt op DNA als het belangrijkste instructieboek. Maar deze kwetsbare code wordt voortdurend aangevallen door chemicaliën, straling en zelfs normale celprocessen. Wanneer schade niet wordt hersteld, kan dat leiden tot kanker of hersenaandoeningen zoals de ziekte van Huntington. Deze studie onthult hoe twee cellulaire "handige helpers", eiwitten genaamd USP7 en FAN1, samenwerken om DNA te beschermen tegen een bijzonder gevaarlijke vorm van schade en om de genetische veranderingen die Huntington aandrijven te vertragen.
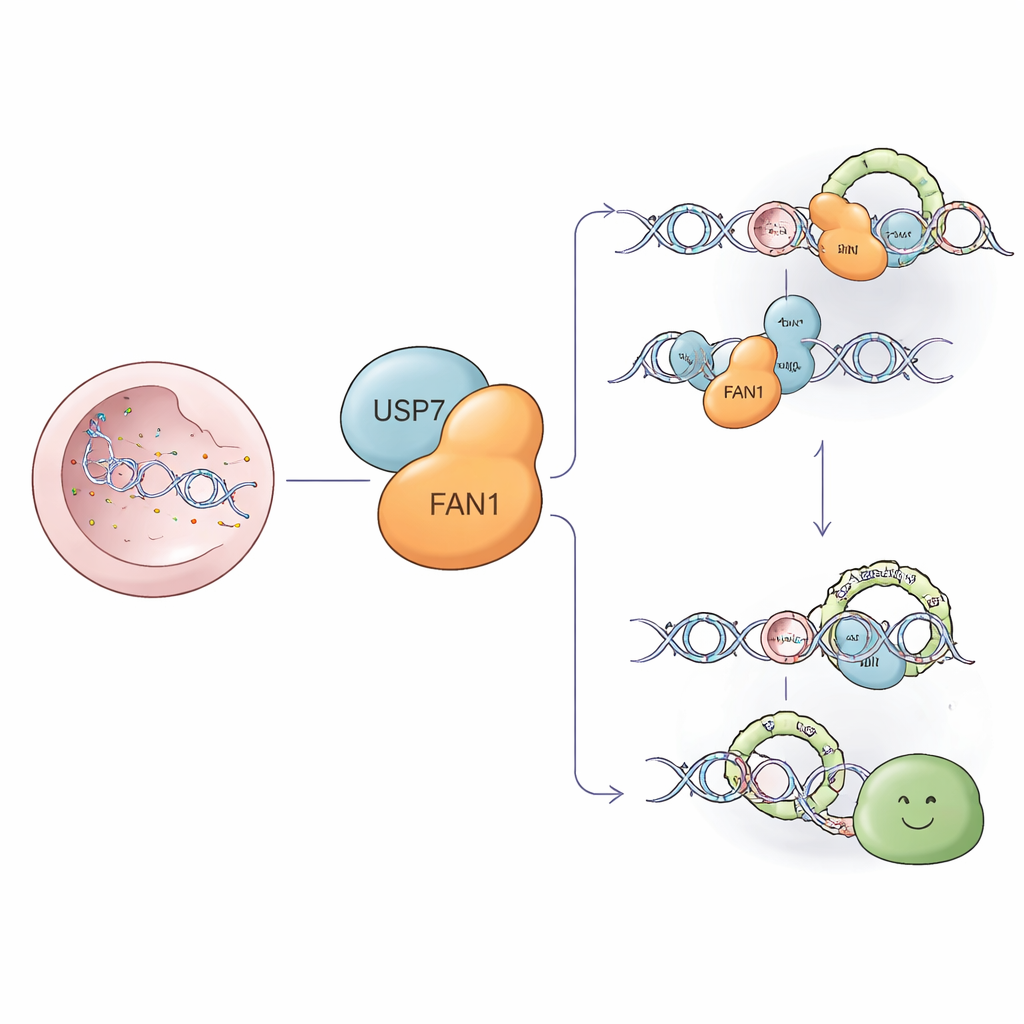
Een moleculair opruimteam voor hardnekkige DNA-schade
Een van de schadelijkste verwondingen aan DNA zijn interstrengkruislingen—moleculaire "nietjes" die de twee strengen van de dubbele helix aan elkaar vastlijmen. Deze nietjes blokkeren de machinerie die DNA kopieert en bedreigen het voortbestaan van de cel. FAN1 is een gespecialiseerd knipenzym dat rond deze nietjes kan snijden en helpt ze te verwijderen zodat herstel kan doorgaan. FAN1 knipt ook lastige extra lussen weg die ontstaan in reeksen van herhaalde DNA-letters, waaronder CAG-herhalingen in het gen dat aan Huntington gekoppeld is. FAN1 op de juiste hoeveelheid en op de juiste plaats houden is daarom cruciaal voor zowel kankerpreventie als gezonde hersenfunctie.
USP7: de lijfwacht van eiwitten
Eiwitten in cellen worden continu gemarkeerd voor afbraak met kleine moleculen genaamd ubiquitine. Die markering is als een "afvalsticker" op een eiwit zodat het cellulaire recyclingmachinerie het afbreekt. USP7 is een deubiquitinase—een enzym dat deze labels verwijdert en geselecteerde eiwitten redt van de versnipperaar. De onderzoekers gebruikten massaspectrometrie, een techniek om eiwitpartners in kaart te brengen, en ontdekten dat USP7 fysiek aan FAN1 bindt, vooral aan het flexibele N‑terminale deel van FAN1. Door zich via twee afzonderlijke oppervlakken vast te grijpen, kan USP7 FAN1 herhaaldelijk herkennen en de afbraaksignalen weghalen.
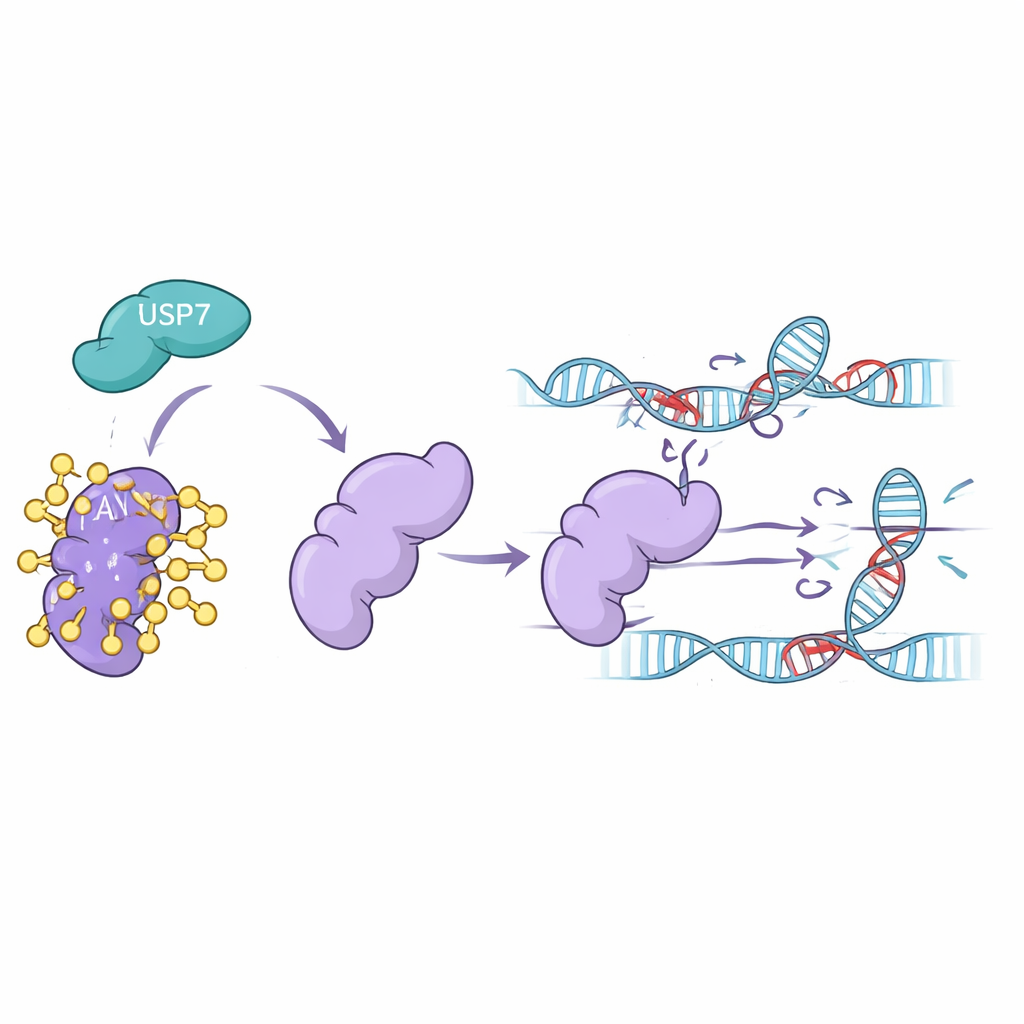
Hoe USP7 FAN1 aan het werk houdt
Laboratoriumexperimenten in menselijke cellijnen lieten zien dat wanneer USP7-niveaus werden verminderd—ofwel door het gen stil te leggen of door cellen te behandelen met USP7-blokkerende middelen—de FAN1-niveaus scherp daalden. FAN1 raakte zwaar versierd met ubiquitine en werd naar het proteasoom gestuurd, het eiwitrecyclingcentrum van de cel. Het blokkeren van het proteasoom redde FAN1, wat bevestigt dat USP7 FAN1 normaal beschermt tegen die afloop. Het team toonde verder aan dat alleen de actieve vorm van USP7 de specifieke ubiquitineketen kon verwijderen die FAN1 markeert voor afbraak. Zonder USP7 verdween FAN1 sneller en kon het niet meer effectief opstapelen op beschadigd DNA waar kruislingen verwijderd moesten worden.
Gevolgen voor DNA-reparatie en de ziekte van Huntington
Wanneer cellen werden blootgesteld aan een crosslinking chemotherapie-medicijn, vertoonden cellen zonder USP7 minder FAN1-reparatiefoci op DNA, meer celdood en grotere gevoeligheid voor schade. Bij matige stress veroorzaakte het wegnemen van USP7 of het wegnemen van FAN1 vergelijkbare kwetsbaarheid, wat suggereert dat FAN1 een belangrijk doelwit van USP7 in deze herstelroute is. De auteurs bekeken vervolgens de ziekte van Huntington, waarbij uitbreiding van CAG-herhalingen in het huntingtine-gen de aandoening in de loop van de tijd verergert. In een menselijk retinaal celmodel dat was geconstrueerd om een lange herhaling te dragen, versnelde verlies van FAN1 de uitbreiding van de herhalingen, terwijl het uitschakelen van een mismatchrepairfactor die uitbreiding vertraagde. Opvallend was dat het neerhalen van USP7 de CAG-herhalingsexpansie bijna net zo snel versnelde als het verlies van FAN1, wat aangeeft dat USP7 indirect de uitbreiding remt door FAN1 stabiel te houden.
Waarom deze ontdekking belangrijk is
Dit werk toont USP7 als een sleutelbeschermer van FAN1 en verbindt daarmee twee grote bedreigingen voor genoomgezondheid: moeilijk te herstellen DNA-kruislingen en ongecontroleerde uitbreiding van CAG-herhalingen bij de ziekte van Huntington. Voor de geïnteresseerde lezer is de kernboodschap dat USP7 functioneert als een lijfwacht die FAN1 beschermt tegen voortijdige afbraak, zodat het DNA-herstel op koers blijft en de genetische drift die neurodegeneratie aandrijft vertraagd wordt. De bevindingen suggereren een delicaat evenwicht voor toekomstige therapieën: het blokkeren van USP7 kan kankercellen gevoeliger maken voor bepaalde chemotherapieën, terwijl het versterken van het USP7–FAN1-samenwerkingsverband kan helpen schadelijke DNA-herhalingen in de hersenen te stabiliseren.
Bronvermelding: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Trefwoorden: DNA-reparatie, genoomstabiliteit, Huntington‑ziekte, proteïneafbraak, trinucleotide-herhalingen