Clear Sky Science · es
La desubiquitinasa USP7 estabiliza a FAN1 para apoyar la reparación de entrecruzamientos de ADN y suprimir la expansión de repeticiones CAG
Protegiendo el manual de instrucciones de nuestro ADN
Cada célula de nuestro cuerpo depende del ADN como su manual maestro de instrucciones. Pero este código delicado está constantemente bajo ataque por químicos, radiación e incluso por procesos celulares rutinarios. Cuando el daño no se repara, puede conducir a cáncer o a trastornos cerebrales como la enfermedad de Huntington. Este estudio revela cómo dos “manitas” celulares, proteínas llamadas USP7 y FAN1, se asocian para proteger el ADN frente a un tipo de daño particularmente peligroso y para frenar los cambios genéticos que impulsan la enfermedad de Huntington.
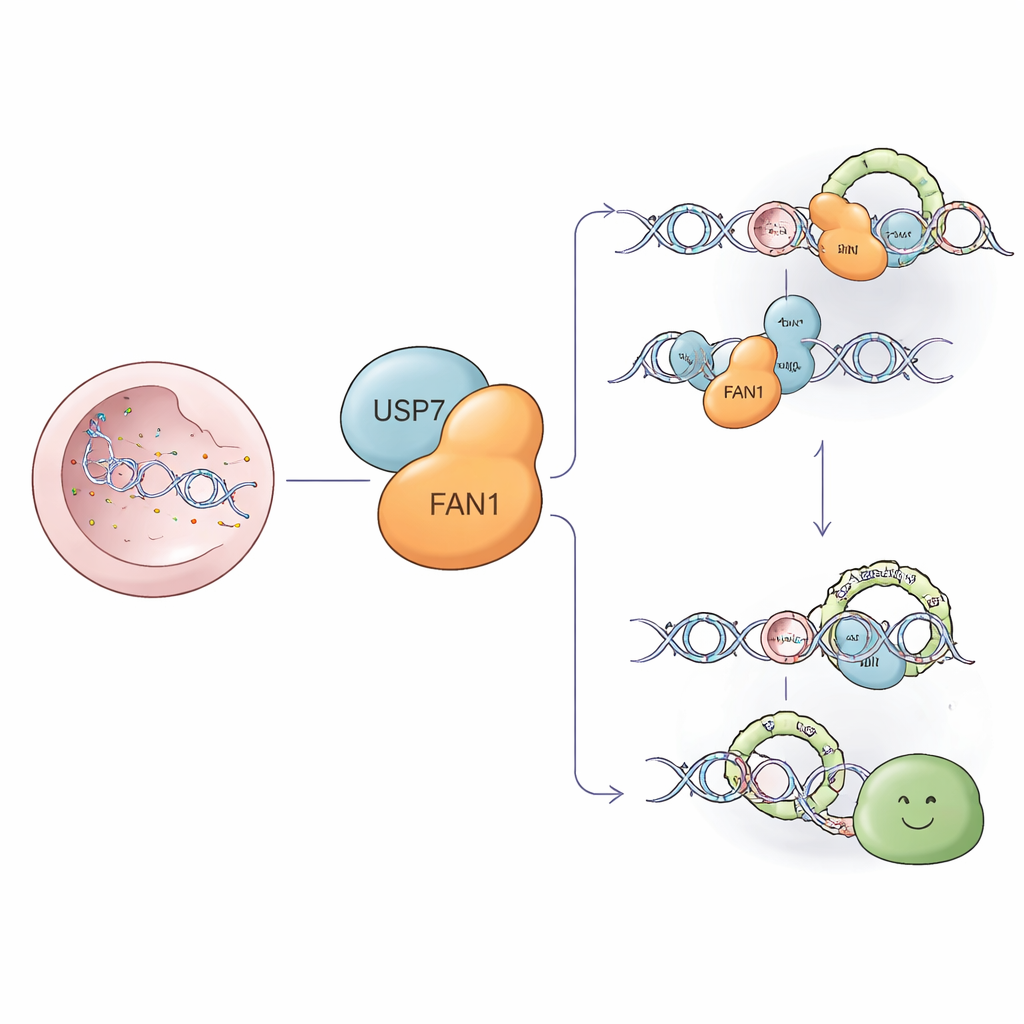
Un equipo molecular de limpieza para daños persistentes en el ADN
Algunas de las lesiones más dañinas para el ADN son los entrecruzamientos intercatenarios: “grapas” moleculares que pegan las dos hebras de la doble hélice del ADN. Estas grapas bloquean la maquinaria que copia el ADN, poniendo en riesgo la supervivencia celular. FAN1 es una enzima especializada en cortar que puede seccionar alrededor de estas grapas y ayudar a retirarlas para que la reparación pueda proseguir. FAN1 también recorta bucles extra problemáticos que se forman en tramos de letras repetidas del ADN, incluidas las repeticiones CAG en el gen vinculado a la enfermedad de Huntington. Mantener a FAN1 en el nivel y localización adecuados es, por tanto, crucial tanto para la prevención del cáncer como para el funcionamiento sano del cerebro.
USP7: el guardaespaldas de las proteínas
Las proteínas en las células están constantemente siendo marcadas para su destrucción por pequeñas moléculas llamadas ubiquitinas. Esta marcación es como poner una etiqueta de “basura” en una proteína para que la maquinaria de reciclaje celular la descomponga. USP7 es una desubiquitinasa: una enzima que elimina estas etiquetas y rescata proteínas seleccionadas del triturador. Los investigadores usaron espectrometría de masas, una técnica para catalogar socios proteicos, y descubrieron que USP7 se une físicamente a FAN1, particularmente en la región N-terminal flexible de FAN1. Al engancharse mediante dos superficies distintas, USP7 puede reconocer repetidamente a FAN1 y arrancarle las etiquetas de destrucción.
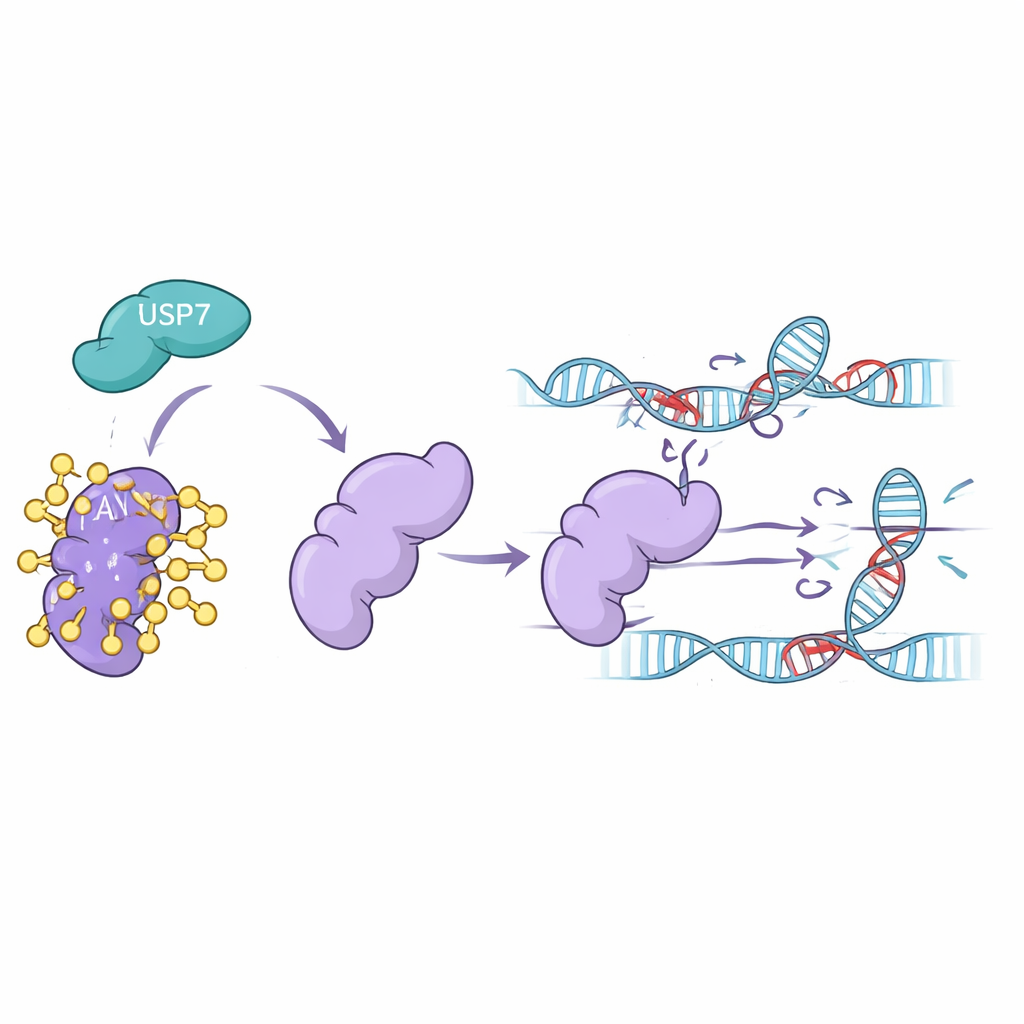
Cómo USP7 mantiene a FAN1 en el trabajo
Experimentos de laboratorio en líneas celulares humanas mostraron que cuando los niveles de USP7 se redujeron, ya sea silenciando su gen o tratando las células con fármacos que bloquean USP7, los niveles de FAN1 cayeron bruscamente. FAN1 quedó fuertemente decorada con ubiquitina y fue enviada al proteasoma, el centro de reciclaje de proteínas de la célula. Bloquear el proteasoma rescató a FAN1, confirmando que USP7 normalmente la protege de ese destino. El equipo mostró además que solo la forma activa de USP7 podía eliminar el tipo específico de cadena de ubiquitina que marca a FAN1 para su destrucción. Sin USP7, FAN1 desaparecía más rápido y ya no podía acumularse de forma eficaz en el ADN dañado donde era necesario eliminar los entrecruzamientos.
Consecuencias para la reparación del ADN y la enfermedad de Huntington
Cuando las células se expusieron a un fármaco quimioterápico que provoca entrecruzamientos, aquellas sin USP7 mostraron menos focos de reparación con FAN1 en el ADN, más muerte celular y mayor sensibilidad al daño. Bajo estrés moderado, eliminar USP7 o eliminar FAN1 causó una fragilidad similar, lo que sugiere que FAN1 es un objetivo principal de USP7 en esta vía de reparación. Los autores se centraron luego en la enfermedad de Huntington, donde la expansión de repeticiones CAG en el gen huntingtina agrava el trastorno con el tiempo. En un modelo de células retinianas humanas diseñado para portar una repetición larga, la pérdida de FAN1 aceleró el crecimiento de la repetición, mientras que desactivar un factor de reparación por desajustes lo ralentizó. De forma llamativa, reducir USP7 aceleró la expansión de las repeticiones CAG casi tanto como la pérdida de FAN1, lo que indica que USP7 restringe indirectamente el crecimiento de las repeticiones al mantener estable a FAN1.
Por qué importa este descubrimiento
Este trabajo revela a USP7 como un guardián clave de FAN1, conectando dos amenazas importantes para la salud del genoma: los entrecruzamientos de ADN difíciles de reparar y la expansión descontrolada de repeticiones CAG en la enfermedad de Huntington. Para un lector no especializado, la conclusión es que USP7 actúa como un guardaespaldas, protegiendo a FAN1 para que no sea destruida prematuramente y así pueda mantener la reparación del ADN en curso y frenar la deriva genética que impulsa la neurodegeneración. Los hallazgos sugieren un equilibrio delicado para futuras terapias: bloquear USP7 podría hacer que las células cancerosas sean más vulnerables a ciertas quimioterapias, mientras que reforzar la asociación USP7–FAN1 podría ayudar a estabilizar repeticiones de ADN dañinas en el cerebro.
Cita: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Palabras clave: Reparación del ADN, Estabilidad del genoma, Enfermedad de Huntington, Degradación de proteínas, Repeticiones trinucleotídicas