Clear Sky Science · ar
إنزيم إزالة الإيوبيكين USP7 يثبت FAN1 لدعم إصلاح الروابط المتصالبة في الدنا وكبح توسع تكرارات CAG
حماية دليل التعليمات الخاص بدنانا
تعتمد كل خلية في أجسامنا على الدنا كدليل رئيسي للتعليمات. لكن هذا الشيفرة الحساسة تتعرض باستمرار لهجمات من مواد كيميائية وإشعاع وحتى من العمليات الخلوية الروتينية. عندما لا يُصلَح الضرر، يمكن أن يؤدي ذلك إلى سرطان أو اضطرابات دماغية مثل داء هنتنغتون. تكشف هذه الدراسة كيف يتعاون "عاملان صيانيان" خلويان، بروتينان يُدعيان USP7 وFAN1، لحماية الدنا من نوع خطير من الأضرار ولإبطاء التغيرات الجينية التي تدفع داء هنتنغتون.
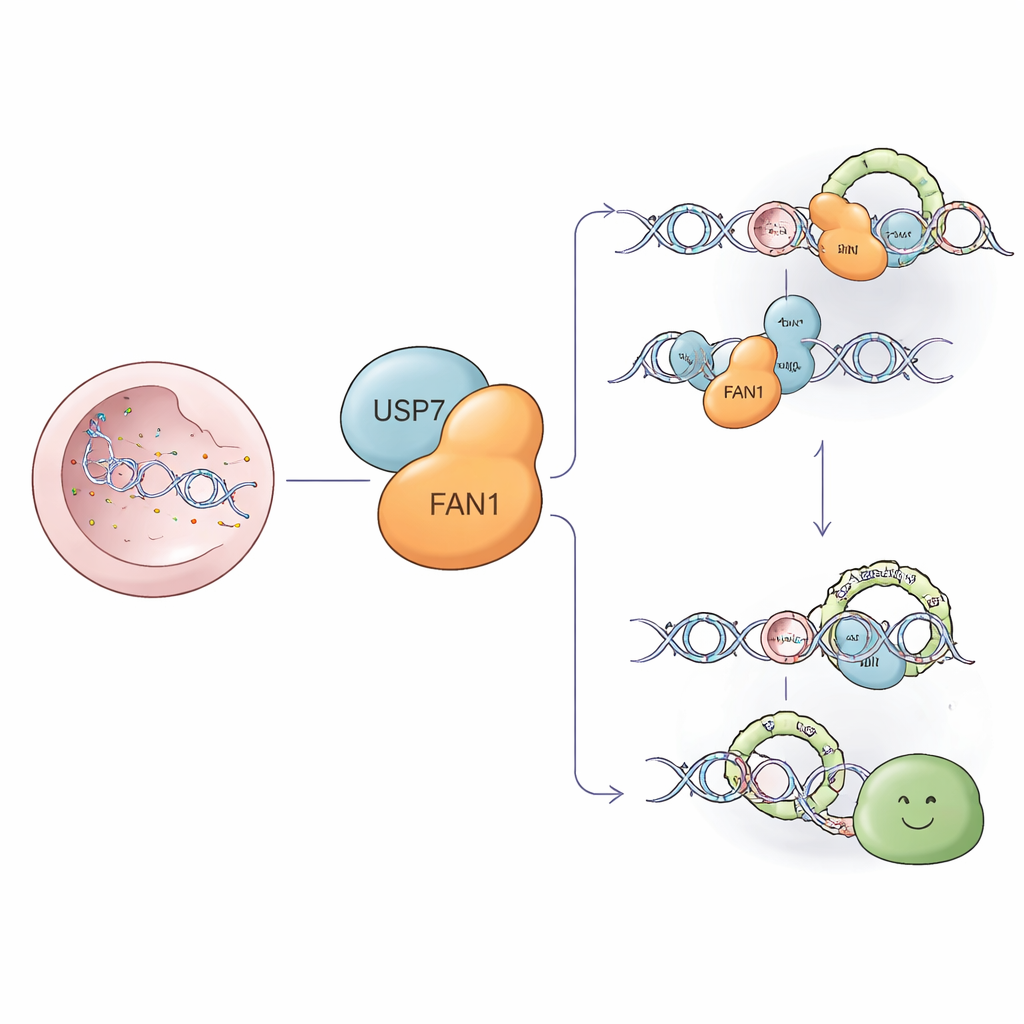
طاقم تنظيف جزيئي للأضرار العنيدة في الدنا
بعض أخطر الإصابات للدنا هي الروابط المتصالبة بين السلسلتين — "مشابك" جزيئية تلصق شِعَرتَي الحلزون المزدوج معا. هذه المشابك تعيق الآلية التي تنسخ الدنا وتهدد بقاء الخلية. FAN1 هو إنزيم قطعي متخصص يمكنه شق المنطقة حول هذه المشابك والمساعدة في إزالتها حتى يستمر الإصلاح. كما يقص FAN1 الحلقات الإضافية المزعجة التي تتكون في مناطق من الحروف المتكررة في الدنا، بما في ذلك تكرارات CAG في الجين المرتبط بداء هنتنغتون. لذا، فإن الحفاظ على مستوى FAN1 وموقعه المناسب أمر حاسم لكل من الوقاية من السرطان ووظيفة الدماغ الصحية.
USP7: حارس بدن البروتين
تُعلَّم البروتينات في الخلايا باستمرار لوضع علامة عليها للتدمير بواسطة جزيئات صغيرة تُدعى الإيوبيكين. هذا الوسم يشبه لصق ملصق "نفاية" على بروتين ليقوم جهاز إعادة التدوير الخلوي بتفكيكه. USP7 هو ديوبوبيويتينيز — إنزيم يزيل هذه العلامات وينقذ بروتينات مختارة من المفرمة. استخدم الباحثون مطياف الكتلة، تقنية لجرد شركاء البروتين، واكتشفوا أن USP7 يرتبط فيزيائيًا بـFAN1، لا سيما في المنطقة الطرفية الن‑لمسية (N‑terminal) المرنة من FAN1. عبر الالتصاق من خلال سطحين مختلفين، يمكن لـUSP7 أن يتعرف مرارًا على FAN1 ويزيل عنه ملصقات التدمير.
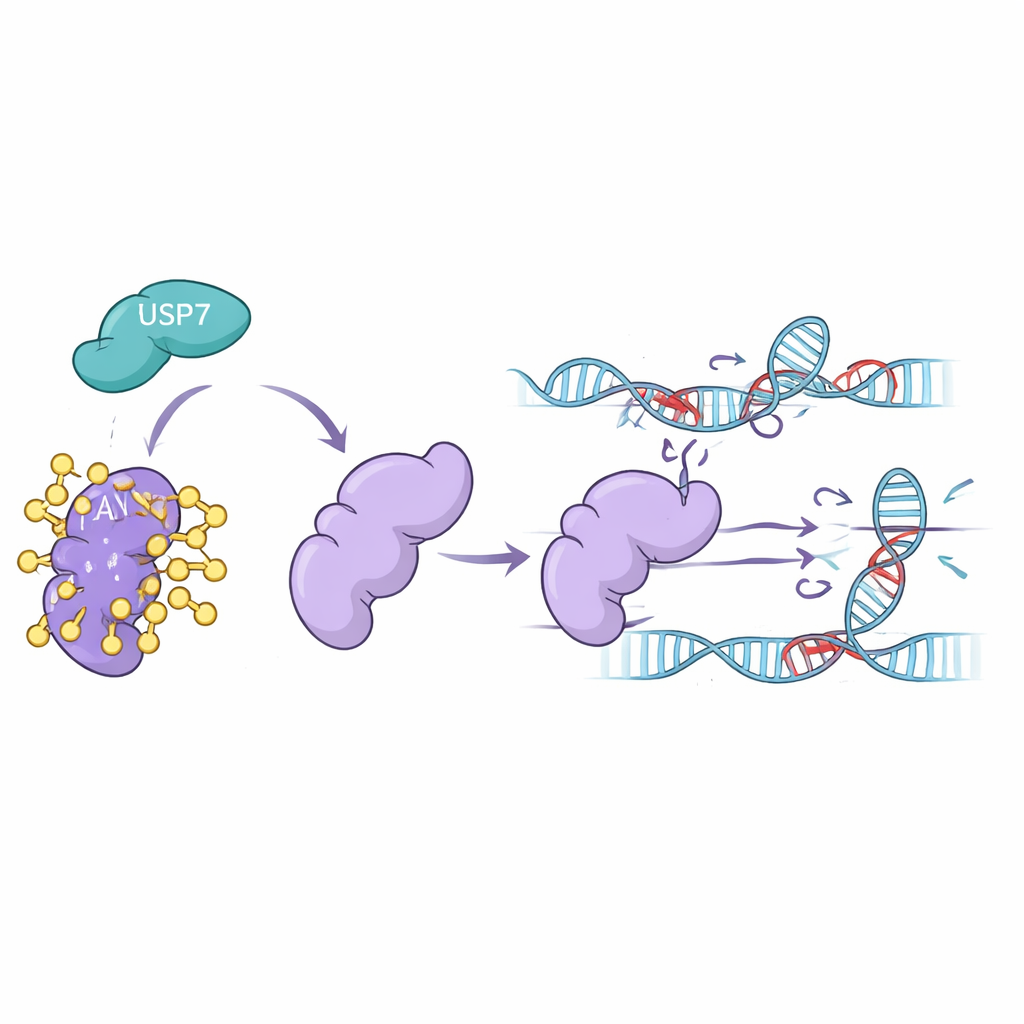
كيف يحافظ USP7 على FAN1 في موقع العمل
أظهرت تجارب مخبرية في خطوط خلايا بشرية أن تقليل مستويات USP7 — إما عن طريق إسكات الجين أو بمعالجة الخلايا بأدوية تمنع USP7 — أدى إلى انخفاض حاد في مستويات FAN1. أصبح FAN1 مُزخرفًا بإيوبيكين بكثافة وأُرسل إلى البروتِيازوم، مركز إعادة تدوير البروتينات في الخلية. إن حجب البروتِيازوم أعاد FAN1، ما يؤكد أن USP7 عادة يحمي FAN1 من هذا المصير. وأظهر الفريق كذلك أن الشكل النشط فقط من USP7 هو القادر على نزع نوع سلسلة الإيوبيكين المحددة التي تميز FAN1 للتدمير. عند غياب USP7، اختفى FAN1 بسرعة أكبر ولم يعد قادرًا على التراكم بفعالية عند مواقع الدنا المتضررة حيث يجب إزالة الروابط المتصالبة.
العواقب على إصلاح الدنا وداء هنتنغتون
عند تعريض الخلايا لدواء كيميائي مكوّن للروابط المتصالبة، أظهرت الخلايا التي تفتقد USP7 نقاط إصلاح FAN1 أقل على الدنا ومعدلات وفاة خلوية أعلى وحساسية أكبر للضرر. تحت إجهاد معتدل، تسبب إزالة USP7 أو إزالة FAN1 في ضعف مماثل، ما يشير إلى أن FAN1 هو الهدف الرئيسي لـUSP7 في هذا المسار الإصلاحي. ثم تحول المؤلفون إلى داء هنتنغتون، حيث يؤدي توسع تكرارات CAG في جين هنتنغتين إلى تفاقم الاضطراب مع مرور الوقت. في نموذج خلوي شبكي إنساني مُعد لينقِل تكرارًا طويلًا، سرّع فقدان FAN1 نمو التكرار، بينما أدى تعطيل عامل إصلاح المطابقات إلى إبطائه. بشكل لافت، أدى خفض USP7 إلى تسريع توسع تكرارات CAG تقريبًا بمقدار مشابه لفقدان FAN1، مما يشير إلى أن USP7 يقيّد نمو التكرارات بشكل غير مباشر عن طريق إبقاء FAN1 مستقرًا.
لماذا تهم هذه النتيجة
تكشف هذه الدراسة أن USP7 هو حارس رئيسي لـFAN1، وتربط تهديدين كبيرين لصحة الجينوم: الروابط المتصالبة للدنا التي يصعب إصلاحها والتوسع المتسارع لتكرارات CAG في داء هنتنغتون. للقراء غير المتخصصين، الرسالة الأساسية هي أن USP7 يعمل كحارس شخصي، يحمي FAN1 من التدمير المبكر حتى يظل قادرًا على إبقاء إصلاح الدنا على المسار الصحيح وإبطاء الانحراف الجيني الذي يدفع التنكس العصبي. تشير النتائج إلى توازن دقيق للعلاجات المستقبلية: قد يجعل حجب USP7 خلايا السرطان أكثر عرضة لأنواع معينة من العلاج الكيميائي، بينما قد يساعد تعزيز شراكة USP7–FAN1 في تثبيت تكرارات الدنا الضارة في الدماغ.
الاستشهاد: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
الكلمات المفتاحية: إصلاح الدنا, استقرار الجينوم, داء هنتنغتون, تحلل البروتين, تكرارات ثلاثية النوكليوتيد