Clear Sky Science · de
Die Deubiquitinase USP7 stabilisiert FAN1 zur Unterstützung der Reparatur von DNA-Quervernetzungen und zur Unterdrückung der CAG-Repeat-Expansion
Schutz des genetischen Handbuchs unserer DNA
Jede Zelle in unserem Körper ist auf die DNA als ihr zentrales Informationshandbuch angewiesen. Doch dieser empfindliche Code steht ständig unter Beschuss durch Chemikalien, Strahlung und sogar durch normale zelluläre Prozesse. Wenn Schäden nicht repariert werden, kann das zu Krebs oder zu Hirnerkrankungen wie der Huntington-Krankheit führen. Diese Studie enthüllt, wie zwei zelluläre „Handwerker“, die Proteine USP7 und FAN1, zusammenarbeiten, um die DNA vor einer besonders gefährlichen Schadensart zu schützen und genetische Veränderungen zu verlangsamen, die die Huntington-Krankheit vorantreiben.
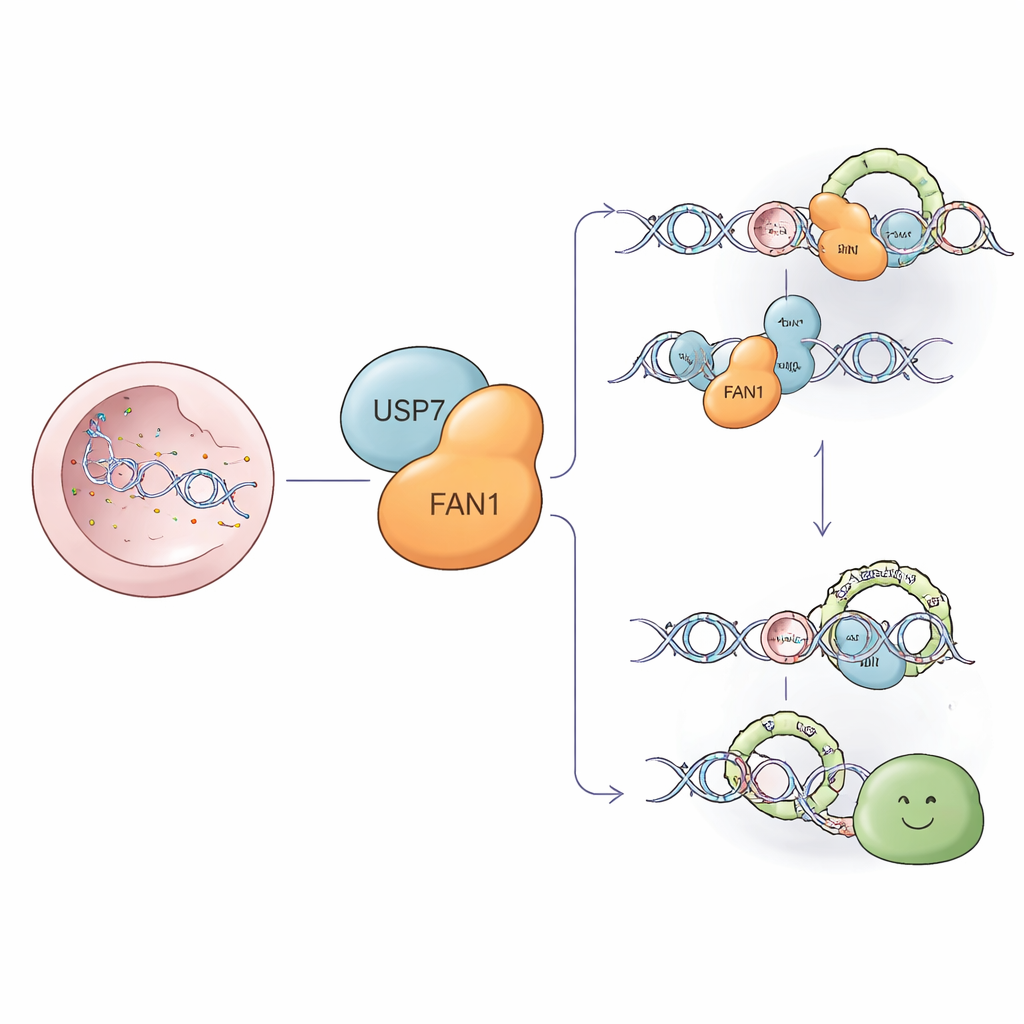
Eine molekulare Aufräumtruppe für hartnäckige DNA-Schäden
Zu den schädlichsten Verletzungen der DNA gehören intersträngige Quervernetzungen — molekulare „Heftklammern“, die die beiden Stränge der DNA-Doppelhelix zusammenkleben. Diese Heftklammern blockieren die Maschinerie, die DNA kopiert, und gefährden so das Überleben der Zelle. FAN1 ist ein spezialisiertes Schneideenzym, das um diese Heftklammern herum schneiden und deren Entfernung ermöglichen kann, sodass die Reparatur fortschreiten kann. FAN1 kürzt außerdem störende zusätzliche Schleifen, die sich in Abschnitten mit wiederholten DNA-Basen bilden, einschließlich der CAG-Repeats im Gen, das mit der Huntington-Krankheit verknüpft ist. FAN1 auf dem richtigen Niveau und am richtigen Ort zu halten, ist daher entscheidend sowohl zur Krebsprävention als auch für eine gesunde Gehirnfunktion.
USP7: der Bodyguard des Proteins
Proteine in Zellen werden ständig mit kleinen Molekülen namens Ubiquitin markiert, um sie zum Abbau freizugeben. Diese Markierung ist wie ein „Müll“-Aufkleber auf einem Protein, damit die zellulären Recycling-Maschinerien es abbauen. USP7 ist eine Deubiquitinase — ein Enzym, das diese Markierungen entfernt und ausgewählte Proteine vor dem Schredder rettet. Die Forschenden nutzten Massenspektrometrie, eine Technik zur Auflistung von Proteinpartnern, und entdeckten, dass USP7 physisch an FAN1 bindet, insbesondere an die flexible N-terminale Region von FAN1. Indem es über zwei unterschiedliche Oberflächen andockt, kann USP7 FAN1 wiederholt erkennen und die Abbausignale entfernen.
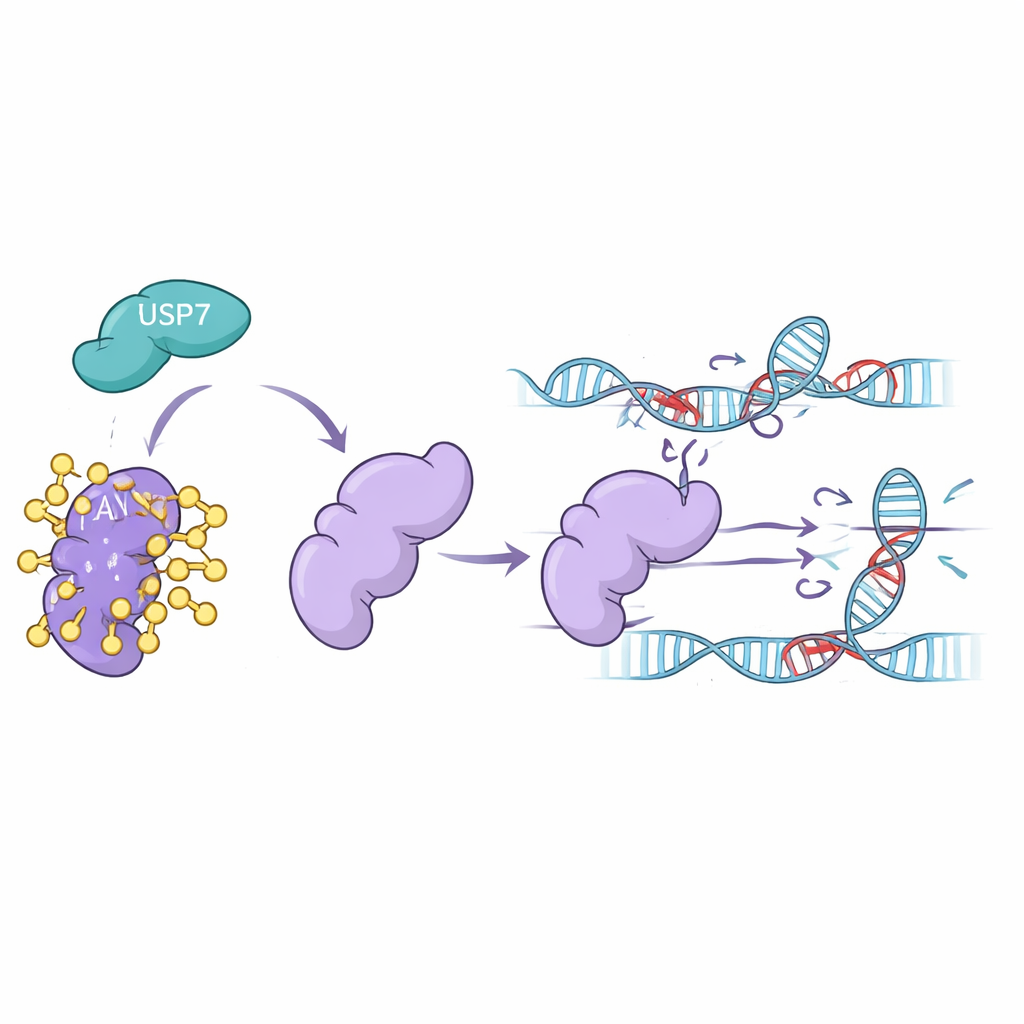
Wie USP7 FAN1 im Dienst hält
Laborversuche in menschlichen Zelllinien zeigten, dass bei reduzierten USP7-Spiegeln — entweder durch Stilllegung seines Gens oder durch Behandlung der Zellen mit USP7-blockierenden Wirkstoffen — die FAN1-Mengen stark abnahmen. FAN1 wurde reichlich mit Ubiquitin dekoriert und zum Proteasom geschickt, dem Proteinrecycling-Zentrum der Zelle. Das Blockieren des Proteasoms rettete FAN1, was bestätigte, dass USP7 FAN1 normalerweise vor diesem Schicksal schützt. Das Team zeigte weiter, dass nur die aktive Form von USP7 die spezifische Ubiquitin-Kettenart entfernen konnte, die FAN1 für den Abbau markiert. Ohne USP7 verschwand FAN1 schneller und konnte sich nicht mehr wirksam an beschädigter DNA ansammeln, wo Quervernetzungen entfernt werden müssen.
Folgen für DNA-Reparatur und Huntington-Krankheit
Wurden Zellen einem quervernetzenden Chemotherapie-Wirkstoff ausgesetzt, zeigten jene ohne USP7 weniger FAN1-Reparaturfoci auf der DNA, mehr Zelltod und eine größere Empfindlichkeit gegenüber Schäden. Unter moderatem Stress führten das Entfernen von USP7 oder von FAN1 zu ähnlicher Fragilität, was nahelegt, dass FAN1 ein Hauptziel von USP7 in diesem Reparaturweg ist. Die Autorinnen und Autoren wandten sich dann der Huntington-Krankheit zu, bei der die Expansion von CAG-Repeats im Huntingtin-Gen die Erkrankung im Verlauf verschlechtert. In einem humanen Netzhaut-Zellmodell mit einer langen Repeat-Sequenz beschleunigte der Verlust von FAN1 das Repeat-Wachstum, während die Deaktivierung eines Mismatch-Reparaturfaktors es verlangsamte. Bemerkenswerterweise beschleunigte das Herunterregulieren von USP7 die CAG-Repeat-Expansion fast so stark wie der Verlust von FAN1, was darauf hindeutet, dass USP7 indirekt das Repeat-Wachstum einschränkt, indem es FAN1 stabil hält.
Warum dieser Befund wichtig ist
Diese Arbeit macht USP7 als wichtigen Wächter von FAN1 sichtbar und verknüpft damit zwei große Gefahren für die Genomgesundheit: schwer zu reparierende DNA-Quervernetzungen und die unkontrollierte Expansion von CAG-Repeats bei der Huntington-Krankheit. Für eine allgemeine Leserschaft lautet die Kernbotschaft, dass USP7 wie ein Bodyguard wirkt, der FAN1 vor vorzeitigem Abbau schützt, damit es die DNA-Reparatur auf Kurs halten und die genetische Drift, die zur Neurodegeneration beiträgt, verlangsamen kann. Die Befunde deuten auf ein empfindliches Gleichgewicht für künftige Therapien hin: Die Blockade von USP7 könnte Krebszellen gegenüber bestimmten Chemotherapien angreifbarer machen, während die Stärkung der USP7–FAN1-Partnerschaft schädliche DNA-Repeats im Gehirn stabilisieren könnte.
Zitation: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Schlüsselwörter: DNA-Reparatur, Genomstabilität, Huntington-Krankheit, Proteinabbau, Trinukleotid-Wiederholungen