Clear Sky Science · it
La deubiquitinasi USP7 stabilizza FAN1 per supportare la riparazione degli incroci di DNA e sopprimere l’espansione dei ripetuti CAG
Proteggere il manuale d’istruzioni del nostro DNA
Ogni cellula del nostro corpo si affida al DNA come a un manuale d’istruzioni fondamentale. Ma questo codice delicato è costantemente preso di mira da sostanze chimiche, radiazioni e persino dai normali processi cellulari. Quando i danni non vengono riparati, possono sfociare in tumori o in disturbi neurologici come la malattia di Huntington. Questo studio svela come due “manovali” cellulari, proteine chiamate USP7 e FAN1, collaborino per proteggere il DNA da un tipo di danno particolarmente pericoloso e per rallentare i cambiamenti genetici che alimentano la malattia di Huntington.
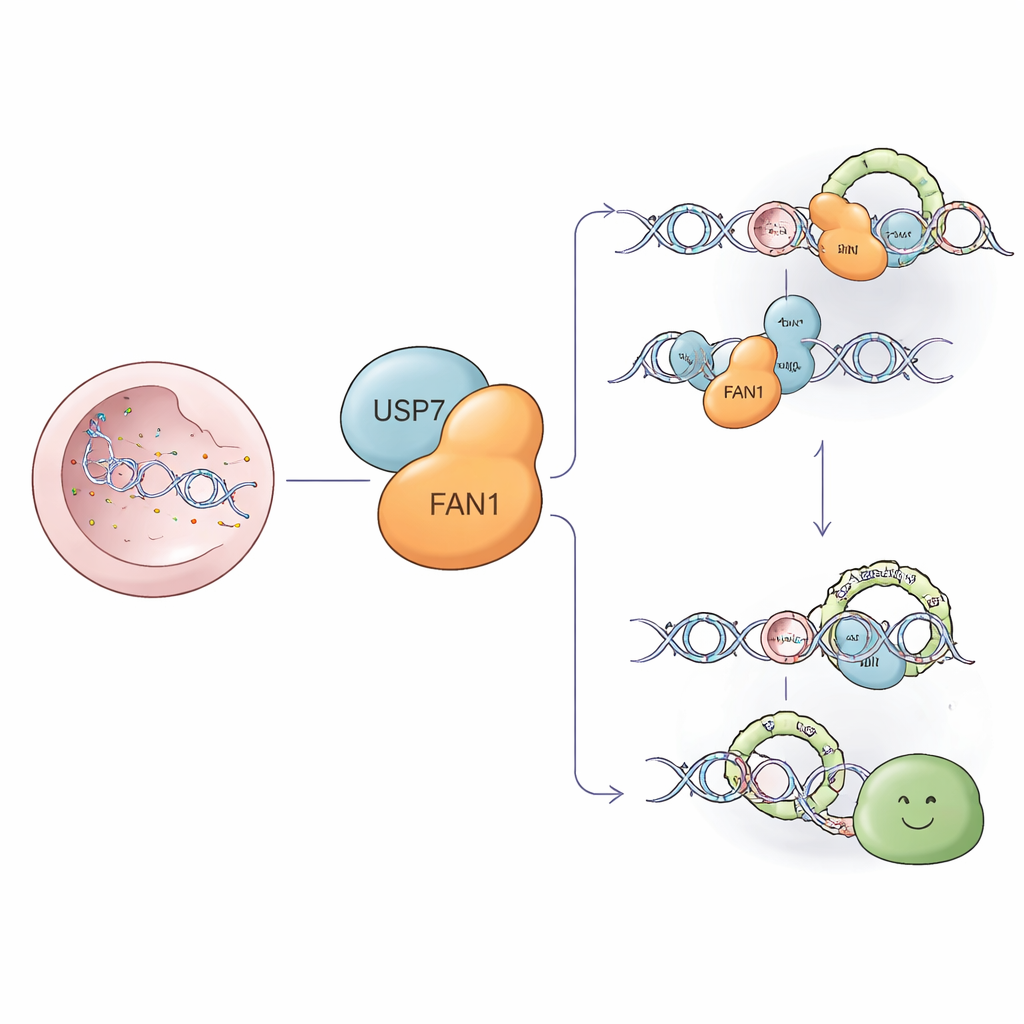
Una squadra molecolare per ripulire danni ostinati al DNA
Alcuni dei danni più dannosi al DNA sono gli incroci tra filamenti—una sorta di “graffette” molecolari che incollano insieme i due filamenti della doppia elica. Queste graffette bloccano le macchine che duplicano il DNA, mettendo a rischio la sopravvivenza cellulare. FAN1 è un’endonucléasi specializzata che può tagliare intorno a queste graffette e contribuire alla loro rimozione in modo che la riparazione possa procedere. FAN1 elimina anche anse extra problematiche che si formano in tratti di DNA ripetuti, comprese le ripetizioni CAG nel gene associato alla malattia di Huntington. Mantenere FAN1 al livello giusto e nel luogo giusto è quindi cruciale sia per la prevenzione del cancro sia per il corretto funzionamento del cervello.
USP7: la guardia del corpo delle proteine
Le proteine nelle cellule vengono costantemente taggate per la distruzione da piccole molecole chiamate ubiquitina. Questo marchio è come un’etichetta “rifiuto” che segnala alla macchina riciclatrice cellulare di degradare la proteina. USP7 è una deubiquitinasi—un enzima che rimuove questi tag e salva determinate proteine dalla triturazione. I ricercatori hanno usato la spettrometria di massa, una tecnica per mappare i partner proteici, e hanno scoperto che USP7 si lega fisicamente a FAN1, in particolare alla regione N-terminale flessibile di FAN1. Agganciandosi attraverso due superfici distinte, USP7 può riconoscere ripetutamente FAN1 e rimuovere i marchi di distruzione.
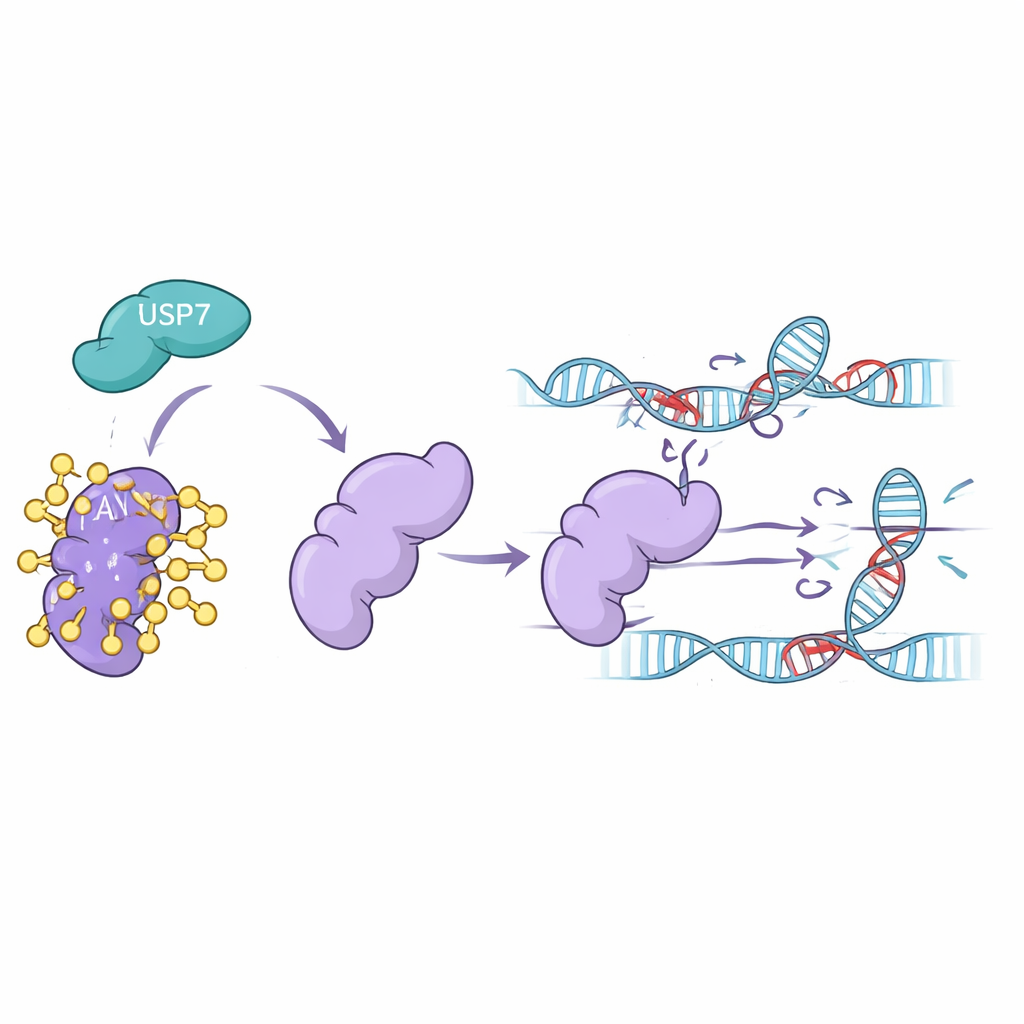
Come USP7 mantiene FAN1 operativo
Esperimenti di laboratorio in linee cellulari umane hanno mostrato che quando i livelli di USP7 erano ridotti—sia silenziando il suo gene sia trattando le cellule con farmaci che inibiscono USP7—i livelli di FAN1 calavano drasticamente. FAN1 veniva pesantemente decorato con ubiquitina e inviato al proteasoma, il centro di riciclaggio delle proteine della cellula. Bloccare il proteasoma ha salvato FAN1, confermando che USP7 normalmente protegge FAN1 da questo destino. Il gruppo ha inoltre dimostrato che solo la forma attiva di USP7 poteva rimuovere un particolare tipo di catena di ubiquitina che segnala FAN1 per la distruzione. Senza USP7, FAN1 scompariva più rapidamente e non riusciva più ad accumularsi efficacemente nei punti di DNA danneggiato dove gli incroci dovevano essere rimossi.
Conseguenze per la riparazione del DNA e la malattia di Huntington
Quando le cellule sono state esposte a un farmaco che crea incroci chimici nel DNA, quelle prive di USP7 mostravano meno foci riparativi di FAN1 sul DNA, maggiore morte cellulare e maggiore sensibilità al danno. In condizioni di stress moderato, rimuovere USP7 o eliminare FAN1 causava una fragilità simile, suggerendo che FAN1 è un bersaglio principale di USP7 in questa via di riparazione. Gli autori si sono poi concentrati sulla malattia di Huntington, dove l’espansione delle ripetizioni CAG nel gene huntingtina peggiora il disturbo nel tempo. In un modello cellulare retinico umano ingegnerizzato per portare una lunga ripetizione, la perdita di FAN1 accelerava la crescita della ripetizione, mentre disabilitare un fattore della riparazione degli errori di appaiamento la rallentava. Colpisce che il silenziamento di USP7 accelerasse l’espansione delle ripetizioni CAG quasi quanto la perdita di FAN1, indicando che USP7 limita indirettamente la crescita delle ripetizioni mantenendo stabile FAN1.
Perché questa scoperta è importante
Questo lavoro rivela USP7 come guardiano chiave di FAN1, collegando due grandi minacce alla salute del genoma: gli incroci di DNA difficili da riparare e l’espansione incontrollata delle ripetizioni CAG nella malattia di Huntington. Per il lettore non specialista, il messaggio principale è che USP7 agisce come una guardia del corpo, proteggendo FAN1 dalla distruzione prematura in modo che possa mantenere la riparazione del DNA e rallentare la deriva genetica che guida la neurodegenerazione. I risultati suggeriscono un equilibrio delicato per future terapie: bloccare USP7 potrebbe rendere le cellule tumorali più vulnerabili a certe chemioterapie, mentre rafforzare la partnership USP7–FAN1 potrebbe aiutare a stabilizzare le ripetizioni dannose nel cervello.
Citazione: Collotta, G., Gatti, M., Ungureanu, IM. et al. USP7 deubiquitinase stabilizes FAN1 to support DNA crosslink repair and suppress CAG repeat expansion. Nat Commun 17, 3551 (2026). https://doi.org/10.1038/s41467-026-70051-9
Parole chiave: Riparazione del DNA, stabilità del genoma, Malattia di Huntington, degradazione proteica, ripetizioni trinucleotidiche