Clear Sky Science · pl
LRG1 pochodzące z hepatocytów przygotowuje wątrobę na przerzuty i osłabia immunoterapię
Dlaczego ta praca ma znaczenie dla pacjentów z rakiem
Rak często wraca nie w narządzie pierwotnym, lecz w odległych miejscach, takich jak wątroba, a gdy to nastąpi, terapie stają się znacznie mniej skuteczne. Badanie to ujawnia, w jaki sposób wątroba jest dyskretnie „przygotowywana” z wyprzedzeniem, by przyjąć krążące komórki nowotworowe, oraz dlaczego guzy, które rozprzestrzeniają się do wątroby, często odporne są na nowoczesne leki immunoterapeutyczne. Wskazując pojedyncze białko wytwarzane przez wątrobę — LRG1 — jako kluczowy przełącznik w tym procesie, praca sugeruje nowe sposoby przewidywania, zapobiegania i lepszego leczenia przerzutów do wątroby.
Sygnał ostrzegawczy we krwi
Lekarze od dawna zauważali, że nowotwory takie jak jelita grubego, trzustki i żołądka często dają przerzuty do wątroby, ale brakowało dobrych narzędzi do przewidywania, kto jest najbardziej narażony. Badacze przeanalizowali próbki krwi pacjentów z tymi nowotworami i stwierdzili, że osoby, które już miały przerzuty do wątroby, miały znacznie wyższe poziomy białka o nazwie LRG1 we krwi. Co jeszcze ważniejsze, wśród osób z wczesnym stadium choroby i bez wykrywalnego rozsiewu, te, które później rozwinęły przerzuty do wątroby, już przy rozpoznaniu miały podwyższone LRG1 i miały tendencję do wcześniejszego nawrotu. W kilku modelach mysich odzwierciedlających raka u ludzi poziom LRG1 we krwi wzrastał na tygodnie przed pojawieniem się widocznych guzów wątroby, wyznaczając tzw. fazę „przed‑przerzutową”, gdy narząd jest przekształcany, aby sprzyjać przyszłemu wzrostowi guza. 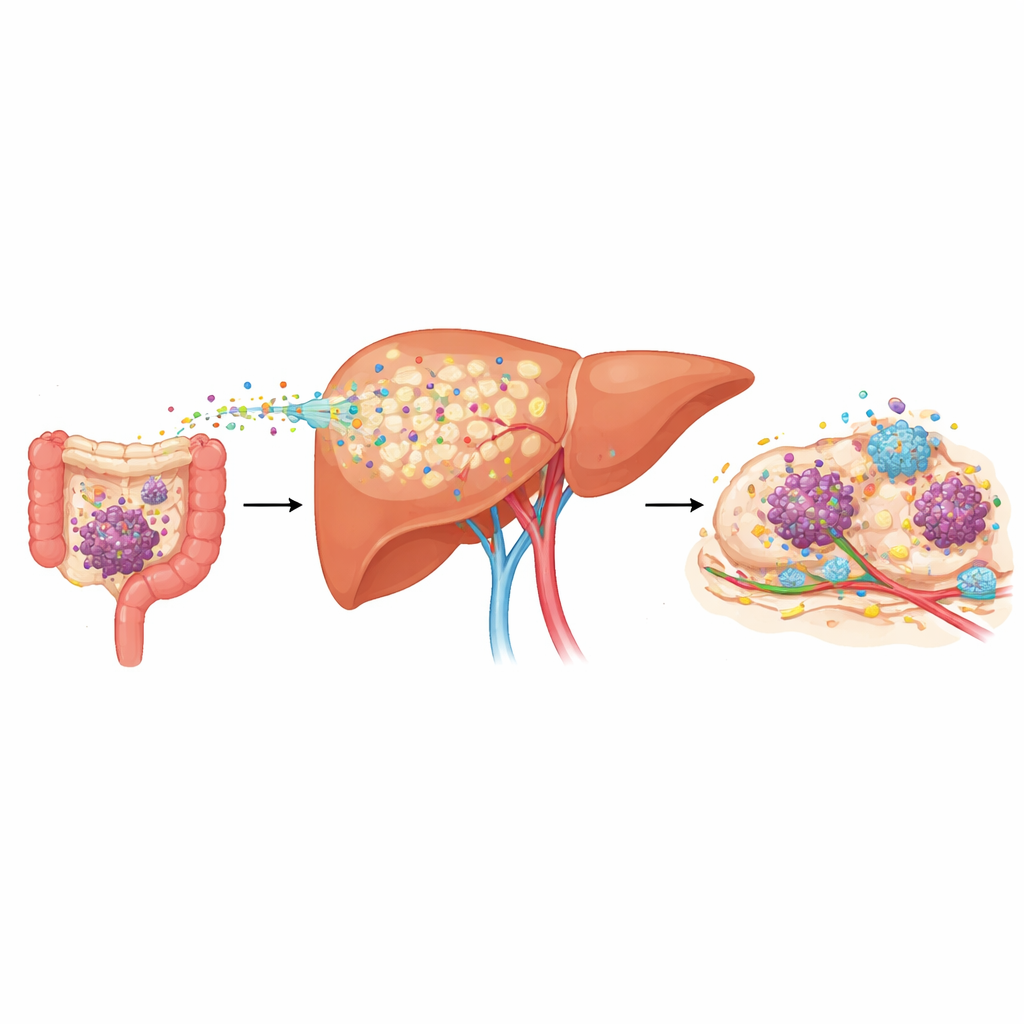
Wątroba to nie tylko bierna ofiara
Aby ustalić, skąd pochodzi ten wzrost LRG1, zespół przebadał wiele narządów i typów komórek u myszy z guzami. Wątroba wyróżniała się jako dominujące źródło, a w jej obrębie zwykłe komórki wątroby (hepatocyty) wytwarzały znacznie więcej LRG1 niż komórki odpornościowe czy śródbłonkowe naczyń krwionośnych. Gdy naukowcy zastosowali inżynierię genetyczną, aby usunąć gen Lrg1 jedynie w hepatocytach, poziomy LRG1 we krwi ledwie wzrastały w przebiegu choroby, a zwierzęta rozwijały znacznie mniej i mniejsze przerzuty do wątroby. W rzeczywistości, gdy przerzuty do wątroby były inicjowane w sposób zwykle prowadzący do dużego obciążenia chorobowego, usunięcie LRG1 pochodzącego z hepatocytów dramatycznie zmniejszyło zarówno liczbę miejsc przerzutowych, jak i ich rozmiar, pokazując, że to wytwarzane przez wątrobę białko jest potężnym ułatwiaczem rozsiewu.
Przeprogramowanie immunologicznego krajobrazu wątroby
Następne pytanie brzmiało: jak LRG1 zmienia zdrową wątrobę w żyzną ziemię dla raka. Przy użyciu sekwencjonowania pojedynczych komórek badacze zmapowali dziesiątki tysięcy indywidualnych komórek wątroby z myszy zdrowych i z guzami. W wątrobach wystawionych na wpływ odległego guza zaobserwowano napływ pewnych białych krwinek tłumiących odporność, szczególnie neutrofili i powiązanych komórek mieloidalnych, podczas gdy pomocne komórki T i komórki dendrytyczne malały lub ulegały wyczerpaniu. Gdy LRG1 nie było obecne w hepatocytach, to przesunięcie w kierunku środowiska immunosupresyjnego zostało w dużej mierze odwrócone. Zespół odkrył, że LRG1 bezpośrednio aktywuje neutrofile do uwalniania kleistych, przypominających sieć struktur znanych jako neutrofilowe sieci zewnątrzkomórkowe (NETy). Te sieci z DNA tworzą się w naczyniach krwionośnych wątroby, chwytając krążące komórki nowotworowe i pomagając im się zakotwiczyć, przeżyć i rosnąć. Rozkład NETów za pomocą enzymu lub wyczerpanie neutrofili ostro redukowało przerzuty do wątroby i w dużej mierze niwelowało przewagę nadawaną przez LRG1, łącząc ten mechanizm bezpośrednio z rozsiewem guza.
Jak zapalenie w guzach komunikuje się z wątrobą
Co powoduje, że hepatocyty zwiększają produkcję LRG1? Badacze pokazali, że nie jest to bezpośredni kontakt z komórkami guza, lecz sygnały zapalne krążące we krwi. Spośród wielu kandydatów zapalny przekaźnik IL‑6 okazał się kluczowym sprawcą: dodanie IL‑6 do komórek wątroby w hodowli silnie indukowało LRG1, podczas gdy blokada IL‑6 lub jego receptora temu zapobiegała. U myszy poziomy IL‑6 wzrastały wraz z LRG1 podczas fazy przed‑przerzutowej, a sztuczne zwiększenie IL‑6 w wątrobie podnosiło produkcję LRG1 i przyspieszało przerzuty — chyba że hepatocyty nie zawierały LRG1. Dalsze analizy wskazały makrofagi — komórki odpornościowe ukształtowane przez rosnący guz — jako główne źródło IL‑6 w wątrobie, ujawniając łańcuch komunikacji: zapalenie guza aktywuje makrofagi, makrofagi uwalniają IL‑6, IL‑6 instruuje hepatocyty do wydzielania LRG1, a LRG1 następnie przebudowuje immunologiczne i naczyniowe środowisko wątroby na korzyść przyszłych komórek nowotworowych. 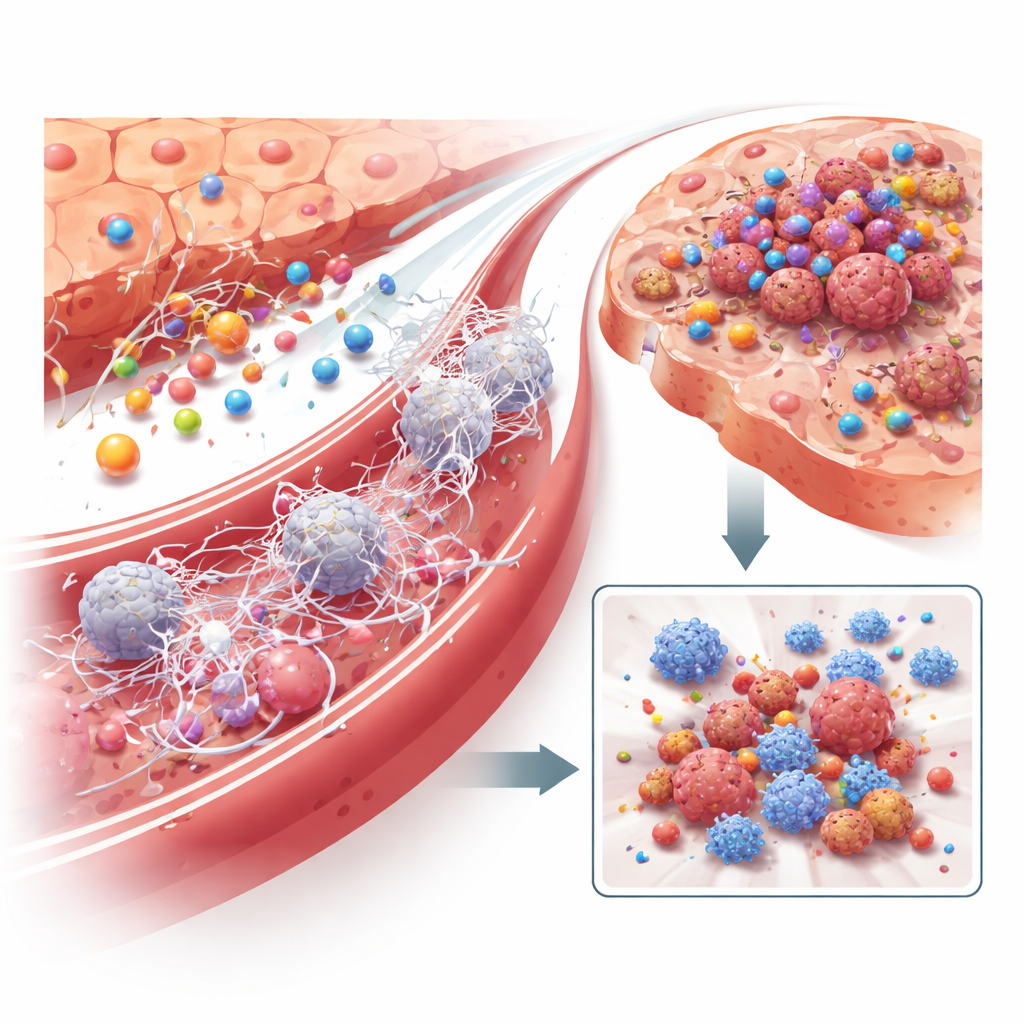
Przekształcanie wrogo nastawionego siedliska z powrotem w przyjazne
Ponieważ LRG1 znajduje się w tym krytycznym punkcie, badacze sprawdzili, czy jego blokada może mieć wartość terapeutyczną. U myszy z eksperymentalnie wywołanymi przerzutami do wątroby leczenie przeciwciałem przeciwko LRG1 zmniejszyło formowanie NETów i istotnie obniżyło liczbę oraz rozmiar guzów wątroby. Podejście terapii genowej, które selektywnie uciszało Lrg1 w hepatocytach, przyniosło podobne korzyści. Co ważne, wiadomo, że przerzuty wątroby osłabiają działanie leków przeciwko punktom kontrolnym immunologicznym, takich jak przeciwciała przeciw PD‑1. Gdy naukowcy połączyli blokadę LRG1 z terapią anty‑PD‑1 w modelu guza wątroby, guzy zmniejszały się znacznie bardziej niż przy którymkolwiek z pojedynczych leczeń, a agresywne komórki odpornościowe (limfocyty CD8) stawały się liczniejsze i bardziej skuteczne w zabijaniu komórek nowotworowych. To sugeruje, że celowanie w LRG1 może przekształcić immunologicznie „zimne” przerzuty wątroby w „cieplejsze”, które lepiej reagują na immunoterapię.
Co to oznacza dla przyszłej opieki
Podsumowując, praca ta ujawnia, że wątroba jest aktywnie przygotowywana przez odległe guzy, by stać się bezpiecznym schronieniem dla komórek nowotworowych, i że LRG1 pochodzące z hepatocytów jest kluczowym przekaźnikiem w tym procesie. Pomiar LRG1 we krwi mógłby pomóc zidentyfikować pacjentów o wysokim ryzyku rozsiewu do wątroby zanim pojawią się przerzuty, podczas gdy leki blokujące LRG1 lub jego upstreamowy sygnał IL‑6 mogłyby zarówno zapobiegać przerzutom do wątroby, jak i uczynić istniejące zmiany bardziej podatnymi na atak immunologiczny. Chociaż odkrycia te dotyczą na razie głównie badań na myszach i próbkach pacjentów, a nie jeszcze badań klinicznych, wskazują obiecującą nową strategię: zamiast czekać i leczyć przerzuty po ich powstaniu, możemy prewencyjnie zdejmować „wycieraczkę powitalną”, którą wątroba rozwija dla raka.
Cytowanie: Long, G., Cheng, B., Jiang, Y. et al. Hepatocyte-derived LRG1 primes the liver for metastasis and impairs immunotherapy. Cell Mol Immunol 23, 560–574 (2026). https://doi.org/10.1038/s41423-026-01408-9
Słowa kluczowe: przerzuty do wątroby, LRG1, mikrośrodowisko immunologiczne, neutrofilowe sieci zewnątrzkomórkowe, immunoterapia raka